Mi az Evista?
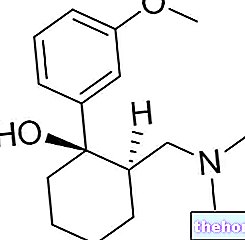
Az Evista egy gyógyszer, amely hatóanyagként raloxifen -hidrokloridot tartalmaz. Fehér, ovális tabletta (60 mg) formájában kapható.
Milyen betegségek esetén alkalmazható az Evista?
Az Evistát a csontritkulás (betegség, amely a csontokat törékennyé teszi) kezelésére és megelőzésére használják nőknél a menopauza után. Az Evistáról kimutatták, hogy jelentősen csökkenti a csigolyatöréseket, de nem csökkenti a csípő (csípő) töréseket.).
A gyógyszer csak receptre kapható.
Hogyan kell alkalmazni az Evistát?
Az ajánlott adag felnőtt nők és idős nők számára napi egy tabletta étkezés közben vagy attól függetlenül. A kalcium- és D -vitamin -kiegészítőket általában azoknak a nőknek ajánlják, akiknek csökkent a kalciumbevitelük. Az Evista hosszú távú használatra készült.
Hogyan fejti ki hatását az Evista?
Osteoporosis akkor fordul elő, ha nem termelnek elegendő új csontot a természetes fogyasztás pótlására. A csontok fokozatosan elvékonyodnak és törékennyé válnak, és hajlamosabbak a törésre (törések). A csontritkulás gyakoribb a posztmenopauzás nőknél. Amikor a női hormon ösztrogén szintje csökken: az ösztrogén lelassul csökkenti a csontok lebomlását, és kevésbé hajlamosak a törésekre.
Az Evista hatóanyaga, a raloxifen, szelektív ösztrogénreceptor -modulátor (SERM), és az ösztrogénreceptor (az ösztrogénreceptorokat stimuláló anyag) agonistájaként hat a szervezet egyes szöveteiben. A raloxifen ugyanolyan hatással van a csontokra, mint az ösztrogén, de nincs hatással a mellre vagy a méhre.
Milyen módszerekkel vizsgálták az Evistát?
Az Evistát négy fő vizsgálatban tanulmányozták az osteoporosis kezelésében és megelőzésében.
Három osteoporosismegelőzési vizsgálatban 1764 nő vett részt, akik két évig Evistát vagy placebót (hatóanyag nélküli kezelést) szedtek. Ezekben a vizsgálatokban a csontsűrűséget mérték. A negyedik vizsgálatban az Evista hatásait összehasonlították az Evista hatásával. csontritkulás kezelésében 7705 nőnél négy éven keresztül. A hatékonyság fő mértéke azon nők száma volt, akik csigolyatörést szenvedtek a vizsgálat során.
Milyen előnyei voltak az Evista alkalmazásának a vizsgálatok során?
Az Evista hatékonyabb volt a placebónál az osteoporosis megelőzésében és kezelésében.
A csontritkulás megelőzésében az Evistát kapó nők két év alatt 1,6% -os csípő- és gerinccsontsűrűség -növekedésről számoltak be, míg azok, akik placebót kaptak, 0,8% -os csökkenésről számoltak be.
A csontritkulás kezelésében az Evista hatékonyabb volt a placebónál a csigolyatörések számának csökkentésében. Négy év alatt a placebóval összehasonlítva az Evista 46% -kal csökkentette a csigolyatörések számát a csontritkulásban szenvedő nőknél és 32% -kal a csontritkulással összefüggő nőknél. törés jelenlétével. Az Evista nem mutatott hatást a csípőtáji törésekre.
Milyen kockázatokkal jár az Evista alkalmazása?
Az Evista leggyakoribb mellékhatásai (10 beteg közül több mint 1-nél fordul elő) az értágulat (hőhullámok) és az influenzaszerű tünetek. Az Evista alkalmazásakor jelentett mellékhatások teljes listáját lásd a betegtájékoztatóban!
Az Evista nem alkalmazható olyan nőknél, akik:
- Képes vagyok gyermekeket szülni;
- - véralvadási problémái vannak vagy voltak, beleértve a mélyvénás trombózist és a tüdőembóliát (vérrögök a tüdőben);
- - májbetegsége, súlyos veseproblémái vannak, megmagyarázhatatlan méhvérzés vagy méhnyálkahártya -rák (a méhnyálkahártya rákja).
Az Evista nem alkalmazható olyan személyeknél, akik túlérzékenyek (allergiásak) a raloxifenre vagy a készítmény bármely más összetevőjére.
Miért engedélyezték az Evista forgalomba hozatalát?
Az emberi felhasználásra szánt gyógyszerek bizottsága (CHMP) arra a következtetésre jutott, hogy az Evista hatékonynak bizonyult a csontritkulás megelőzésében és kezelésében, nincs hatással a mellre és a méhre. A bizottság úgy határozott, hogy az Evista előnyei meghaladják a kockázatokat a menopauza utáni nők csontritkulásának kezelésében és megelőzésében.
Egyéb információ az Evistáról:
1998. augusztus 5 -én az Európai Bizottság kiadta az Európai Unió egész területén érvényes "Evista" forgalomba hozatali engedélyét. A "forgalomba hozatali engedélyt" 2003. augusztus 5 -én és 2008. augusztus 5 -én megújították. A forgalomba hozatali engedély jogosultja a Daiichi Sankyo Europe GmbH .
Az Evista EPAR teljes verziójáért kattintson ide.
Az összefoglaló utolsó frissítése: 01-2009.
Az ezen az oldalon közzétett Evista -raloxifen -hidrokloridra vonatkozó információk elavultak vagy hiányosak lehetnek. Ezen információk helyes használatához tekintse meg a Jogi nyilatkozat és a hasznos információk oldalt.