Hatóanyagok: razagilin
AZILECT 1 mg tabletta
Indikációk Miért használják az Azilect -et? Mire való?
Az AZILECT -et a Parkinson -kór kezelésére használják. A Levodopa -val (egy másik Parkinson -kór kezelésére használt gyógyszer) együtt vagy anélkül is alkalmazható.
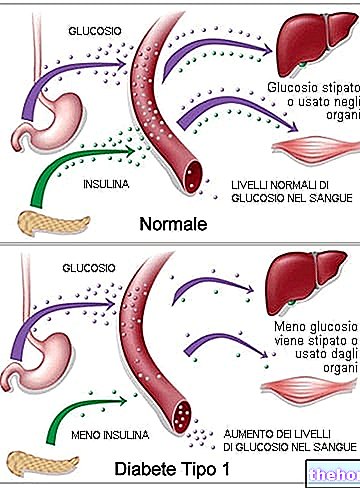
Parkinson -kór esetén a dopaminerg sejtek elvesztése az agy bizonyos területein fordul elő. A dopamin egy agyi anyag, amely a mozgás szabályozásáért felelős. Az AZILECT segít növelni és fenntartani az agy dopaminszintjét.
Ellenjavallatok Az Azilect nem alkalmazható
Ne szedje az AZILECT -et:
- ha allergiás (túlérzékeny) a razagilinre vagy az AZILECT egyéb összetevőjére.
- ha súlyos májelégtelenségben szenved.
Ne szedje az alábbi gyógyszereket az AZILECT -szel együtt:
- monoamin-oxidáz (MAO) inhibitorok (antidepresszánsként, Parkinsin-betegség kezelésére vagy bármely más javallatra), beleértve a vény nélkül kapható gyógyszereket és természetes termékeket, például az orbáncfüvet.
- petidin (erős fájdalomcsillapító).
Az AZILECT -kezelés befejezése után várjon legalább 14 napot, mielőtt elkezdené a MAO -gátlókkal vagy petidinnel történő kezelést.
Az alkalmazással kapcsolatos óvintézkedések Mit kell tudnia az Azilect szedése előtt
Az AZILECT fokozott elővigyázatossággal alkalmazható
- Enyhe vagy közepesen súlyos májműködési zavar esetén.
- Bármilyen bőrváltozás gyanúja esetén forduljon orvosához.
Gyermekek
Az AZILECT alkalmazása 18 év alatti betegeknél nem ajánlott.
Kölcsönhatások Mely gyógyszerek vagy élelmiszerek módosíthatják az Azilect hatását
Feltétlenül tájékoztassa kezelőorvosát vagy gyógyszerészét a jelenleg vagy nemrégiben szedett egyéb gyógyszereiről, beleértve a vény nélkül kapható készítményeket is, valamint ha dohányzik vagy abba kívánja hagyni a dohányzást.
Mielőtt az alábbi gyógyszereket az AZILECT -nel együtt szedné, kérje ki kezelőorvosa tanácsát:
- egyes antidepresszánsok (szelektív szerotonin -visszavétel -gátlók, szelektív szerotonin- és noradrenalin -visszavétel -gátlók, triciklusos vagy tetraciklusos antidepresszánsok)
- a ciprofloxacin antibiotikum, amelyet fertőzések kezelésére használnak
- dextrometorfán, köhögés elleni gyógyszer
- szimpatomimetikumok, mint például a szemcseppekben, orr- és orális dekongesztánsokban, valamint efedrint vagy pszeudoefedrint tartalmazó hideggyógyszerekben.
Kerülje az AZILECT és fluoxetint vagy fluvoxamint tartalmazó antidepresszánsok együttes alkalmazását Az AZILECT -kezelés megkezdése előtt várjon legalább öt hetet a fluoxetin -kezelés abbahagyása után.
A fluoxetin- vagy fluvoxamin -kezelés megkezdése előtt várjon legalább 14 napot az AZILECT -kezelés abbahagyása után.
Tájékoztassa kezelőorvosát, ha Ön, családja vagy gondozói észreveszik, hogy szokatlan magatartást tanúsít, ami miatt nem tud ellenállni a késztetésnek, késztetésnek vagy vágynak, hogy bizonyos tevékenységeket végezzen, amelyek veszélyesek vagy ártalmasak Önre vagy másokra. Az AZILECT -et és / vagy más Parkinson -kór kezelésére használt gyógyszereket szedő betegeknél olyan viselkedést figyeltek meg, mint a kényszer, a megszállott gondolatok, a szerencsejáték -függőség, a túlköltekezés. . Előfordulhat, hogy orvosának módosítania kell az adagot vagy abba kell hagynia a kezelést
Az AZILECT egyidejű bevétele étellel és itallal
Az AZILECT étkezés közben vagy attól függetlenül is bevehető.
Figyelmeztetések Fontos tudni, hogy:
Terhesség és szoptatás
Mielőtt bármilyen gyógyszert elkezdene szedni, kérjen tanácsot orvosától vagy gyógyszerészétől.
A készítmény hatásai a gépjárművezetéshez és gépek kezeléséhez szükséges képességekre
Nem végeztek vizsgálatokat a gépjárművezetéshez és gépek kezeléséhez szükséges képességekre gyakorolt hatásokról. Vezetés és gépek kezelése előtt kérje ki orvosa tanácsát.
Adagolás, az alkalmazás módja és ideje Az Azilect alkalmazása: Adagolás
Az AZILECT -et mindig az orvos által elmondottaknak megfelelően szedje. Ha kétségei vannak, forduljon orvosához vagy gyógyszerészéhez.
Az AZILECT szokásos adagja 1 db 1 mg -os tabletta szájon át, naponta egyszer. Az AZILECT étkezés közben vagy attól függetlenül is bevehető.
Túladagolás Mi a teendő, ha túl sok Azilect -et vett be?
Ha az előírtnál több AZILECT -et vett be
Ha úgy gondolja, hogy az előírtnál több AZILECT tablettát vett be, azonnal forduljon orvosához vagy gyógyszerészéhez. Vigye magával az AZILECT buborékcsomagolást / palackot, hogy megmutassa orvosának vagy gyógyszerészének.
Ha elfelejtette bevenni az AZILECT -et
Ne vegyen be kétszeres adagot a kihagyott tabletta pótlására. A következő adagot a szokásos időben vegye be, amikor ideje bevenni.
Ha idő előtt abbahagyja az AZILECT szedését
Ha bármilyen további kérdése van az AZILECT alkalmazásával kapcsolatban, kérdezze meg kezelőorvosát vagy gyógyszerészét.
Mellékhatások Melyek az Azilect mellékhatásai?
Mint minden gyógyszer, az AZILECT is okozhat mellékhatásokat, amelyek azonban nem mindenkinél jelentkeznek.
A következő nemkívánatos hatásokat jelentették placebo-kontrollos klinikai vizsgálatokban.
A lehetséges mellékhatások gyakoriságát az alábbiakban felsorolva határozzuk meg:
- Nagyon gyakori (10 beteg közül több mint 1 -nél fordul elő)
- Gyakori (100 betegből 1-10)
- Nem gyakori (1000 betegből 1-10)
- Ritka (10 000 betegből 1-10)
- Nagyon ritka (10 000 betegből kevesebb mint 1 -nél fordul elő)
- Nem ismert (a gyakoriság a rendelkezésre álló adatokból nem állapítható meg).
Nagyon gyakori:
- Rendellenes mozgások (diszkinézia)
- fejfájás.
Gyakori:
- hasi fájdalom
- esik
- allergia,
- láz
- influenza szindróma (influenza)
- általános rossz közérzet (rossz közérzet)
- nyaki fájdalom
- mellkasi fájdalom (angina pectoris)
- vérnyomáscsökkenés álló helyzetben, olyan tünetekkel együtt, mint a szédülés / szédülés (ortosztatikus hipotenzió)
- csökkent étvágy
- székrekedés
- száraz száj
- hányinger és hányás
- puffadás
- a vérvizsgálati eredmények eltérései (leukopenia)
- ízületi fájdalom (arthralgia)
- mozgásszervi fájdalom
- ízületi gyulladás (ízületi gyulladás)
- a kézizom zsibbadása és gyengesége (carpalis alagút szindróma)
- testtömegvesztés
- rendellenes álmok
- izomkoordinációs nehézség (egyensúlyzavarok)
- depresszió
- szédülés
- elhúzódó izomösszehúzódások (dystonia)
- orrfolyás (nátha)
- bőrirritáció (dermatitisz)
- bőrpír
- vörös szemek (kötőhártya -gyulladás)
- vizeletürítés.
Ritka:
- stroke (cerebrovascularis stroke)
- Szívroham (miokardiális infarktus)
- hólyagosodás a bőrön (vesiculobullous erythema).
Ezenkívül a placebo-kontrollos klinikai vizsgálatokban a betegek körülbelül 1% -ánál jelentettek bőrrákot. Tudományos bizonyítékok arra utalnak, hogy a Parkinson-kór, és nem egy adott gyógyszer, magasabb bőrrák kockázatával jár (nem csak a melanoma) a bőr megváltozik az orvosától.
A Parkinson -kór olyan tünetekkel jár, mint hallucinációk és zavartság. A forgalomba hozatalt követő tapasztalatok szerint ezeket a tüneteket az AZILECT -tel kezelt Parkinson -kórban szenvedő betegeknél is megfigyelték.
Volt olyan eset, amikor a betegek egy vagy több gyógyszert szedtek a Parkinson -kór kezelésére, de nem tudtak ellenállni a késztetésnek, a vágynak vagy a kísértésnek, hogy olyan cselekvést hajtsanak végre, amely ártalmas lehetett önmagukra vagy másokra. Ezeket a viselkedést impulzusnak nevezik. A következő viselkedéseket figyelték meg az AZILECT -et és / vagy más Parkinson -kór kezelésére szolgáló gyógyszereket szedő betegeknél:
- Rögeszmés gondolatok vagy impulzív viselkedések.
- Erős impulzus a túlzott szerencsejátékra a súlyos személyes vagy családi következmények ellenére.
- Megváltozott vagy megnövekedett szexuális érdeklődés és magatartások, amelyek önmagukat vagy másokat érintik, például a szexuális vágy növekedése. - Ellenőrizhetetlen és túlzott kiadások vagy vásárlások.
Tájékoztassa kezelőorvosát, ha ezen viselkedésmódok bármelyike előfordul; megvitatja a tünetek kezelésének vagy csökkentésének módjait.
Ha bármely mellékhatás súlyossá válik, vagy ha a betegtájékoztatóban felsorolt mellékhatásokon kívül egyéb tünetet észlel, kérjük, értesítse orvosát vagy gyógyszerészét.
Lejárat és megőrzés
Az AZILECT -et gyermekek elől elzárva tartandó!
A dobozon, üvegen vagy dobozon feltüntetett lejárati idő után ne alkalmazza az AZILECT -et. A lejárati idő a hónap utolsó napjára vonatkozik.
Legfeljebb 25 ° C -on tárolandó.
A gyógyszereket nem szabad a szennyvízzel vagy a háztartási hulladékkal együtt megsemmisíteni. Kérdezze meg gyógyszerészét, hogy mit tegyen a már nem használt gyógyszereivel. Ez elősegíti a környezet védelmét.
Mit tartalmaz az AZILECT?
- A készítmény hatóanyaga a razagilin. Minden tabletta 1 mg razagilint tartalmaz (mezilát formájában).
- Egyéb összetevők: mannit, vízmentes kolloid szilícium -dioxid, kukoricakeményítő, előzselatinizált kukoricakeményítő, sztearinsav, talkum.
Milyen az AZILECT külleme és mit tartalmaz a csomagolás?
Az AZILECT fehér, törtfehér tabletta formájában kapható, kerek, lapos és metszett szélű, egyik oldalán sima, a másik oldalon "GIL" és "1" dombornyomással.
A tabletták 7, 10, 28, 30, 100 és 112 tablettát tartalmazó csomagolásban vagy 30 tablettát tartalmazó palackokban kaphatók.
Nem feltétlenül mindegyik kiszerelés kerül kereskedelmi forgalomba.
Forrás betegtájékoztató: AIFA (Olasz Gyógyszerügynökség). A tartalom 2016 januárjában jelent meg. A jelenlévő információk nem feltétlenül naprakészek.
A legfrissebb verzióhoz való hozzáféréshez ajánlatos az AIFA (Olasz Gyógyszerügynökség) webhelyét elérni. Jogi nyilatkozat és hasznos információk.
01.0 A GYÓGYSZER MEGNEVEZÉSE
AZILECT 1 MG TABLETTA
02.0 MINŐSÉGI ÉS MENNYISÉGI ÖSSZETÉTEL
1 mg razagilin (mezilát) tablettánként.
A segédanyagok teljes listáját lásd a 6.1 pontban.
03.0 GYÓGYSZERFORMA
Tabletta.
Fehér vagy törtfehér tabletta, kerek, lapos és metszett szélű, egyik oldalán sima, a másik oldalon "GIL" és "1" dombornyomással.
04.0 KLINIKAI INFORMÁCIÓK
04.1 Terápiás javallatok
Az AZILECT a Parkinson-kór kezelésére javallt mind monoterápiaként (levodopa nélkül), mind kombinált terápiaként (levodopával) olyan betegeknél, akiknél a dózis végén ingadozik.
04.2 Adagolás és alkalmazás
Adagolás
A razagilint szájon át, 1 mg -os adagban, naponta egyszer, levodopával vagy anélkül adják be.
Éhgyomorra vagy teli gyomorra is bevehető.
Idősek: Idős betegeknél nincs szükség az adag módosítására.
Gyermekpopuláció: Az Azilect alkalmazása gyermekeknél és serdülőknél nem javasolt a biztonságosságra és a hatásosságra vonatkozó adatok hiánya miatt.
Májelégtelenségben szenvedő betegek: Súlyos májelégtelenségben szenvedő betegeknél a razagilin alkalmazása ellenjavallt (lásd 4.3 pont). Legyen óvatos, ha enyhe májelégtelenségben szenvedő betegeknél razagilin -kezelést kezd.
Veseelégtelenségben szenvedő betegek: Veseelégtelenségben szenvedő betegeknél nincs szükség az adag módosítására.
04.3 Ellenjavallatok
A készítmény hatóanyagával vagy bármely segédanyagával szembeni túlérzékenység (lásd 6.1 pont).
Egyidejű kezelés más monoamin-oxidáz (MAO) inhibitorokkal (beleértve a vény nélkül kapható gyógyszereket és természetes termékeket, például orbáncfüvet) vagy petidinnel (lásd 4.5 pont). Várjon legalább 14 napot a kezelés abbahagyása között. Razagilinnel és a kezelés megkezdésével MAO -gátlókkal vagy petidinnel.
A razagilin alkalmazása ellenjavallt súlyos májelégtelenségben szenvedő betegeknél.
04.4 Különleges figyelmeztetések és a használathoz szükséges óvintézkedések
Kerülje a razagilin és a fluoxetin vagy a fluvoxamin együttes alkalmazását (lásd 4.5 pont). A razagilin -kezelés megkezdése előtt várjon legalább öt hetet a fluoxetin -kezelés abbahagyása után. Várjon legalább 14 napot a razagilin -kezelés abbahagyása és a fluoxetin- vagy fluvoxamin -kezelés megkezdése között.
Impulzus -szabályozó rendellenességek (ICD -k) fordulhatnak elő dopamin agonistákkal és / vagy dopaminerg kezeléssel kezelt betegeknél. Hasonló jelentések érkeztek a razagilinnel kezelt betegeknél a forgalomba hozatalt követően az impulzus-szabályozási rendellenességekről (ICD-kről). A betegeket rendszeresen ellenőrizni kell az impulzus-szabályozó rendellenességek kialakulása szempontjából. A betegeknek és gondozóiknak tisztában kell lenniük az impulzus-szabályozási zavarok viselkedési tüneteivel, amelyek razagilinnel kezelt betegeknél figyeltek meg, beleértve a kényszereket, a megszállott gondolatokat, a kóros szerencsejátékot, a fokozott libidót, a hiperszexualitást, az impulzív viselkedést és a kényszeres költekezést vagy vásárlást.
Mivel a razagilin fokozza a levodopa hatásait, a levodopa mellékhatásai fokozódhatnak, és a már meglévő diszkinézia súlyosbodhat. A levodopa adagjának csökkentése javíthatja ezt a mellékhatást.
Beszámoltak vérnyomáscsökkentő hatásokról, amikor a razagilint levodopával együtt alkalmazzák. A Parkinson -kórban szenvedő betegek különösen érzékenyek a hipotenzió mellékhatásaira a járási problémák miatt.
A razagilin és a dextrometorfán vagy a szimpatomimetikumok egyidejű alkalmazása, beleértve az orr- és orális dekongesztánsokat, valamint a megfázás kezelésére használt efedrint vagy psudoefedrint tartalmazó gyógyszereket, nem ajánlott (lásd 4.5 pont).
A razagilin klinikai fejlesztési programja során néhány melanoma esetet figyeltek meg, amelyek a razagilinnel való esetleges összefüggésre utalhatnak. Az összegyűjtött adatok azt mutatják, hogy a Parkinson -kór, és nem egy adott gyógyszer, magasabb bőrrák (nem csak melanoma) kockázatával jár. Bőrkárosodás gyanúja esetén forduljon szakemberhez.
Legyen óvatos a razagilin -kezelés megkezdésekor enyhe májelégtelenségben szenvedő betegeknél.
Kerülje a razagilin alkalmazását mérsékelt májelégtelenségben szenvedő betegeknél .. Ha enyhe vagy közepesen súlyos májelégtelenség alakul ki, hagyja abba a razagilin -kezelést (lásd 5.2 pont).
04.5 Kölcsönhatások más gyógyszerekkel és más interakciók
A nem szelektív MAO-gátlók és más gyógyszerek között számos ismert kölcsönhatás ismert.
A razagilint nem szabad más MAO-gátlókkal együtt alkalmazni (beleértve a vény nélkül kapható gyógyszereket és természetes termékeket, például az orbáncfüvet), mivel fennáll a "nem szelektív MAO-gátlás és a rohamok kialakulásának veszélye." 4.3. szakasz).
Súlyos mellékhatásokat jelentettek a petidin és a MAO-gátlók, valamint egy másik szelektív MAO-B-gátló együttes alkalmazása esetén. A razagilin és a petidin egyidejű alkalmazása ellenjavallt (lásd 4.3 pont).
A MAO -gátlók és szimpatomimetikus gyógyszerek egyidejű alkalmazása gyógyszerkölcsönhatási jelenségeket eredményezett. Ezért, tekintettel a razagilin MAO -gátló aktivitására, a razagilin és a szimpatomimetikumok, például az orrnyálkahártya -csökkentőkben, valamint az efedrint vagy psudoefedrint tartalmazó orális és hideg gyógyszerekben való egyidejű alkalmazás ( lásd 4.4 pont).
Gyógyszerkölcsönhatásokról számoltak be dextrometorfán és nem szelektív MAO-gátlók egyidejű alkalmazásakor. Ezért a razagilin MAO -gátló hatása miatt a razagilin és a dextrometorfán egyidejű alkalmazása nem javasolt (lásd 4.4 pont).
Kerülje a razagilin és fluoxetin vagy fluvoxamin együttes alkalmazását (lásd 4.4 pont).
A razagilin és a szelektív szerotonin -újrafelvétel -gátlók (SSRI -k) / szelektív szerotonin- és noradrenalin -újrafelvétel -gátlók (SNRI -k) egyidejű alkalmazásáról a klinikai vizsgálatok során lásd a 4.8 pontot.
Súlyos mellékhatásokról számoltak be SSRI -k, SNRI -k, triciklusos és tetraciklikus antidepresszánsok és MAO -gátlók egyidejű alkalmazásakor.
A levodopa klinikailag szignifikáns hatásáról a razagilin clearance -re nem számoltak be Parkinson -kórban szenvedő betegeknél, akik krónikus kezelésben részesültek levodopával kombinált gyógyszerként.
Oktatás in vitro az anyagcseréről kimutatták, hogy a citokróm P4501A2 (CYP1A2) a fő enzim, amely felelős a razagilin metabolizmusáért. A razagilin és a ciprofloxacin (CYP1A2 inhibitor) egyidejű alkalmazása 83% -kal növelte a razagilin AUC értékét. A razagilin és a teofillin (a CYP1A2 szubsztrátja) egyidejű alkalmazása nem volt hatással a két termék farmakokinetikájára. Ezért az erős CYP1A2 inhibitorok megváltoztathatják a razagilin plazmaszintjét, ezért óvatosan kell alkalmazni őket.
Dohányzó betegeknél fennáll annak a kockázata, hogy a razagilin plazmaszintje csökken a CYP1A2 metabolizáló enzim indukciója miatt.
Oktatás in vitro kimutatta, hogy az 1 mcg / ml razagilin-koncentráció (ami megegyezik az átlagos Cmax times 5,9-8,5 ng / ml 160-szoros szintjével Parkinson-kórban szenvedő betegeknél 1 mg razagilin többszöri adagja után) nem gátolta a citokróm P450 CYP1A2, CYP2A6 izoenzimeket , CYP2C9, CYP2C19, CYP2D6, CYP2E1, CYP3A4 és CYP4A. Ezek az eredmények azt mutatják, hogy a razagilin terápiás koncentrációja nem valószínű, hogy jelentősen befolyásolná ezen enzimek szubsztrátjait.
A razagilin és az entakapon egyidejű alkalmazása 28% -kal növelte a razagilin orális clearance-ét.
A tiramin / razagilin kölcsönhatás: öt tiramin -stimulációs vizsgálat eredményei (önkénteseken és Parkinson -kórban szenvedő betegeknél), valamint az étkezés utáni napi vérnyomásmérés adatai (464 betegnél, akik 0,5 mg / nap vagy 1 mg / nap razagilint vagy placebót kaptak, kombinált terápiaként levodopával) hat hónapig, a tiraminra vonatkozó korlátozások nélkül), valamint a tiramin és a razagilin közötti kölcsönhatásról szóló jelentések hiánya a tiramin korlátlan klinikai vizsgálataiban azt jelzi, hogy a razagilin biztonságosan és étrendi korlátozások nélkül alkalmazható a tiraminra vonatkozóan.
04.6 Terhesség és szoptatás
Klinikai adatok nem állnak rendelkezésre a razagilin terhesség alatti alkalmazásáról.). Óvatosság szükséges a gyógyszer terhes nőknek történő felírásakor.
A kísérleti adatok azt mutatják, hogy a razagilin gátolja a prolaktin szekréciót, és így gátolhatja a laktációt.
Nem ismert, hogy a razagilin kiválasztódik -e az anyatejbe. Különös figyelmet kell fordítani a gyógyszer szoptató nőknek történő beadására.
04.7 Hatások a gépjárművezetéshez és gépek kezeléséhez szükséges képességekre
A gépjárművezetéshez és gépek kezeléséhez szükséges képességeket nem vizsgálták.
A betegeket figyelmeztetni kell a gépek, beleértve a gépjárműveket, használatának kockázatára, amíg meg nem győződnek arról, hogy az Azilect nincs hatással képességeikre.
04.8 Nemkívánatos hatások
A razagilin klinikai fejlesztési programjában összesen 1361 beteg kapott 3076,4 betegévet razagilinnel. A kettős-vak, placebo-kontrollos vizsgálatokban 529 beteget 212 betegévvel egyenlő 1 mg / nap razagilinnel kezeltek, és 539 beteget 213 betegévvel placebót kaptak.
Monoterápia
Az alábbiakban felsoroljuk azokat a mellékhatásokat, amelyeket magasabb gyakorisággal jelentettek a placebo-kontrollos vizsgálatokban 1 mg razagilinnel kezelt betegeknél (razagilin csoport n = 149, placebo csoport n = 151).
A mellékhatásokat, amelyek legalább 2% -os eltérést mutatnak a placebótól, jelentették dőlt
A zárójelben lévő szám (a betegek% -a) jelzi a mellékhatások előfordulását a razagilin és a placebo csoportban.
A mellékhatásokat a gyakoriság szerint rangsorolták a következő konvenciók szerint: nagyon gyakori (> 1/10), gyakori (> 1/100 - 1/1 000 - 1/10 000 -
Fertőzések és fertőzések
Gyakori: influenza (4,7% vs. 0,7%)
Jó-, rosszindulatú és nem meghatározott daganatok (beleértve a cisztákat és polipokat)
Gyakori: bőrrák (1,3% vs. 0,7%)
A vér és a nyirokrendszer zavarai
Gyakori: leukopenia (1,3% vs. 0%)
Az immunrendszer zavarai
Gyakori: allergiás reakciók (1,3% vs. 0,7%)
Anyagcsere- és táplálkozási rendellenességek
Nem gyakori: csökkent étvágy (0,7% vs. 0%)
Pszichiátriai rendellenességek
Gyakori: depresszió (5,4% vs. 2%), hallucinációk (1,3% vs. 0,7%)
Idegrendszeri betegségek
Nagyon gyakori: migrén (14,1% vs. 11,9%)
Nem gyakori: cerebrovaszkuláris stroke (0,7% vs. 0%)
Szembetegségek
Gyakori: kötőhártya -gyulladás (2,7% vs. 0,7%)
Fül- és labirintuszavarok
Gyakori: szédülés (2,7% vs 1,3%)
Szív patológiák
Gyakori: angina pectoris (1,3% vs. 0%)
Nem gyakori: miokardiális infarktus (0,7% vs. 0%)
Légzőrendszeri, mellkasi és mediastinalis betegségek
Gyakori: rhinitis (3,4% vs. 0,7%)
Emésztőrendszeri betegségek
Gyakori: puffadás (1,3% vs. 0%)
A bőr és a bőr alatti szövet betegségei
Gyakori: dermatitis (2,0% vs. 0%)
Nem gyakori: vesiculobullous erythema (0,7% vs. 0%)
A csont -izomrendszer és a kötőszövet betegségei
Gyakori: mozgásszervi fájdalom (6,7% vs. 2,6%), nyaki fájdalom (2,7% vs. 0%), ízületi gyulladás (1,3% vs. 0,7%)
Vese- és húgyúti betegségek
Gyakori: vizeletürítés (1,3% vs. 0,7%)
Általános betegségek és az alkalmazás helyén fellépő állapotok
Gyakori: láz (2,7% vs 1,3%), rossz közérzet (2% vs. 0%)
Társulási terápia
Az alábbiakban azokat a mellékhatásokat figyelték meg, amelyek nagyobb gyakorisággal fordultak elő placebo-kontrollos vizsgálatokban, 1 mg razagilint kapó betegeknél (razagilin-csoport n = 380, placebo-csoport = 388). A zárójelben lévő szám (a betegek% -a) jelzi a mellékhatások előfordulását a razagilin és a placebo csoportban.
A mellékhatásokat, amelyek legalább 2% -os eltérést mutatnak a placebótól, jelentették dőlt.
A mellékhatásokat a gyakoriság szerint rangsorolták a következő konvenciók szerint: nagyon gyakori (> 1/10), gyakori (> 1/100 - 1/1 000 - 1/10 000 -
Jó-, rosszindulatú és nem meghatározott daganatok (beleértve a cisztákat és polipokat)
Nem gyakori: bőr melanoma (0,5% vs. 0,3%)
Anyagcsere- és táplálkozási rendellenességek
Gyakori: csökkent étvágy (2,4% vs. 0,8%)
Pszichiátriai rendellenességek
Gyakori: hallucinációk (2,9% vs 2,1%), kóros álmok (2,1% vs. 0,8%)
Nem gyakori: zavartság (0,8% vs 0,5%)
Idegrendszeri betegségek
Nagyon gyakori: diszkinézia (10,5% vs 6,2%)
Gyakori: dystonia (2,4% vs. 0,8%), carpal tunnel szindróma (1,3% vs. 0%), egyensúlyzavarok (1,6% vs. 0,3%)
Nem gyakori: cerebrovascularis stroke (0,5% vs. 0,3%)
Szív patológiák
Nem gyakori: angina pectoris (0,5% vs. 0%)
Érpatológiák
Gyakori: ortosztatikus hipotenzió (3,9% vs. 0,8%)
Emésztőrendszeri betegségek
Gyakori: hasi fájdalom (4,2% vs 1,3%), székrekedés (4,2% vs 2,1%), hányinger és hányás (8,4% vs 6,2%), szájszárazság (3,4% vs 1,8%)
A bőr és a bőr alatti szövet betegségei
Gyakori: bőrkiütés (1,1% vs. 0,3%)
A csont -izomrendszer és a kötőszövet betegségei
Gyakori: arthralgia (2,4% vs 2,1%), nyaki fájdalom (1,3% vs 0,5%)
Diagnosztikai tesztek
Gyakori: testtömeg csökkenés (4,5% vs. 1,5%)
Sérülés, mérgezés és a trauma okozta szövődmények
Gyakori: esés (4,7% vs. 3,4%)
A Parkinson -kór olyan tünetekkel jár, mint hallucinációk és zavartság. A forgalomba hozatalt követő tapasztalatok szerint ezeket a tüneteket Parkinson -kórban szenvedő, razagilinnel kezelt betegeknél is észlelték.
Súlyos mellékhatások előfordulása ismert SSRI-k, SNRI-k, triciklusos és tetraciklusos antidepresszánsok és MAO-gátlók egyidejű alkalmazásakor. A forgalomba hozatalt követő tapasztalatok szerint szerotonin-szindróma eseteiről számoltak be, amelyek izgatottsággal, zavartsággal, merevséggel járnak., Láz és myoclonus olyan betegeknél, akiket antidepresszánsokkal / SNRI -kkel egyidejűleg razagilinnel kezeltek.
A razagilin klinikai vizsgálatai során a fluoxetin vagy fluvoxamin és a razagilin egyidejű alkalmazása nem volt megengedett, de a következő antidepresszánsok alkalmazása engedélyezett a következő dózisokban: amitriptilin ≤ 50 mg naponta, trazodon ≤ 100 mg naponta, citalopram ≤ 20 mg naponta, szertralin ≤ 100 mg naponta és paroxetin ≤ 30 mg naponta. A razagilin klinikai programja során nem jelentettek szerotonin -szindróma eseteket, amelyben 115 beteget kezeltek egyidejűleg razagilinnel és triciklusos szerekkel, 141 beteget pedig razagilinnel és SSRI / SNRI -vel.
A forgalomba hozatalt követő tapasztalatok szerint a razagilint kapó betegeknél emelkedett vérnyomásról számoltak be, beleértve ritka hipertóniás krízis eseteket is, amelyek ismeretlen mennyiségű, tiraminban gazdag ételeket fogyasztottak.
A szimpatomimetikus gyógyszerek egyidejű alkalmazásakor gyógyszerkölcsönhatásokról számoltak be MAO -gátlókkal.
A forgalomba hozatalt követő tapasztalatok szerint emelkedett vérnyomásról számoltak be egy olyan betegnél, aki a razagilin-kezelés során tetrahidrozolin-hidroklorid szemészeti vazokonstriktort is alkalmazott.
Az impulzusvezérlés zavarai
A dopamin agonistákkal és / vagy más dopaminerg kezelésekkel kezelt betegeknél kóros szerencsejáték, fokozott libidó, hiperszexualitás, kényszeres vásárlás vagy vásárlás, binge evés és kényszeres evés fordulhat elő. Hasonló képet észleltek az impulzus -szabályozási zavarokról, amelyek kényszereket, rögeszmés gondolatokat is tartalmaztak és impulzív viselkedés (lásd 4.4 pont).
04.9 Túladagolás
Túladagolás: Az Azilect 3 mg és 100 mg közötti dózisban történő túladagolása után jelentett tünetek közé tartozott a diszfória, a hipománia, a hipertóniás válság és a szerotonin -szindróma.
A túladagolás a MAO-A és a MAO-B jelentős gátlásával járhat.
Egészséges önkénteseket 20 mg / nap termékkel kezeltek egyszeri dózissal végzett vizsgálatban, vagy 10 mg / nap 10 napos vizsgálatban. A megfigyelt mellékhatásokat enyhe vagy mérsékeltnek minősítették, és nem kapcsolódtak a razagilin -kezeléshez. Szív- és érrendszeri mellékhatásokról (beleértve a magas vérnyomást és a poszturális hipotenziót) számoltak be a dózist emelő vizsgálatban krónikus levodopa-kezelésben részesülő betegeknél, akik 10 mg / nap razagilint kaptak, és eltűntek a kezelés abbahagyásakor.
Nincs specifikus ellenszer. Túladagolás esetén figyelje a betegeket, és "megfelelő tüneti és támogató terápiával" avatkozzon be.
05.0 FARMAKOLÓGIAI TULAJDONSÁGOK
05.1 Farmakodinámiás tulajdonságok
Farmakoterápiás csoport: parkinsonizmus elleni gyógyszerek, monoamin -oxidáz inhibitorok -B
ATC kód: N04BD02
A cselekvés mechanizmusa:
A razagilin erőteljes és visszafordíthatatlan szelektív MAO-B-gátlónak bizonyult, ami az extracelluláris dopaminszint növekedéséhez vezethet a striatumban. A dopaminszint emelkedése és ennek következtében a dopaminerg aktivitás növekedése felelős lehet a razagilinnel a motoros diszfunkció dopaminerg alapú modelljeiben megfigyelt jótékony hatásokért.
Az 1-aminoindán a razagilin fő aktív metabolitja, és nem MAO-B inhibitor.
Klinikai vizsgálatok:
A razagilin hatékonyságát három vizsgálat eredményei dokumentálták: monoterápia az I. vizsgálatban és kombinált terápia a II. És III.
Monoterápia:
Az I. vizsgálatban 404 beteget randomizáltak és 26 hétig placebóval (138 beteg) 1 mg / nap razagilinnel (134 beteg) vagy 2 mg / nap razagilinnel (132 beteg) kezeltek, más aktív összehasonlító szer nélkül.
Ebben a vizsgálatban az elsődleges hatékonysági végpont az egységes Parkinson-kór-besorolási skála (UPDRS, I-III. Rész) összpontszámának a kiindulási értékhez viszonyított változása volt. A különbség a kiindulási érték és a kezelés 26. hete / kezelés vége közötti átlagos változás (LOCF, Last Observation Carried Forward) között statisztikailag szignifikáns volt (UPDRS, I -III. Rész: 1 mg razagilin esetében a placebóhoz képest -4, 2, 95% CI [-5,7 -2,7];
Társulási terápia:
A II. Vizsgálatban a betegeket randomizálták és 18 hétig placebóval (229 beteg) vagy napi 1 mg razagilinnel (231 beteg) vagy 200 mg entakaponnal (227 beteg), katechol-O-metiltranszferáz-gátlóval (COMT) kezelték. a levodopa (LD) / dekarboxiláz inhibitor tervezett adagjával. A III. Vizsgálatban a betegeket randomizálták és 26 hétig placebóval (159 beteg), 0,5 mg / nap razagilinnel (164 beteg) vagy 1 mg / nap razagilinnel (149 beteg) kezelték.
Mindkét vizsgálatban a hatékonyság fő mércéje a kiindulási és a kezelési időszak közötti változás volt a nap folyamán a "kikapcsolt" állapotban töltött órák átlagos számában (az otthon 24 órán át összeállított és minden nap előtt három napon át összeállított naplók alapján) értékelő látogatás).
A II. Vizsgálatban a "kikapcsolt" állapotban eltöltött órák átlagos különbsége a placebóhoz képest -0,78 óra, 95% -os CI [-1,18 -0,39 óra], p = 0,0001. Az entakapon csoportban megfigyelt átlagos napi "kikapcsolási" idő csökkenés (-0,80 óra, 95% CI [-1,20 -0,41], p
A másodlagos hatékonysági mérések közé tartozott a vizsgáló általános értékelése a javulás mértékéről, a napi élet tevékenységei (ADL) alskála pontszám „kikapcsolt” állapotban és az UPDRS pontszám „be” állapotban. A placebóval összehasonlítva a razagilin -kezelés eredményezte statisztikailag szignifikáns előnyben.
05,2 "Farmakokinetikai tulajdonságok
Abszorpció: A razagilin gyorsan felszívódik, és körülbelül 0,5 óra alatt éri el a plazma csúcskoncentrációját (Cmax). Az egyszeri dózisú razagilin abszolút biohasznosulása körülbelül 36%.
Az étel nem befolyásolja a razagilin Tmax-ját, bár a Cmax és az expozíció (AUC) körülbelül 60% -kal, illetve 20% -kal csökken, ha a gyógyszert magas zsírtartalmú étkezéssel együtt alkalmazzák. Az AUC lényegesen nem változik, a razagilin teli vagy üres gyomorra kell bevenni.
terjesztés: A razagilin átlagos eloszlási térfogata egyszeri dózisú intravénás injekció után 243 l. A plazmafehérjék kötődése a 14C -jelzett razagilin egyszeri orális adagja után körülbelül 60-70%.
Anyagcsere: A razagilin kiválasztása előtt a májban szinte teljes biotranszformáción megy keresztül. A razagilin fő metabolikus útjai a következők: N-dealkiláció és / vagy hidroxilezés, 1-amino-indán, 3-hidroxi-N-propargil-1-amino-indán és 3-hidroxi-1-aminoindán képződésével. A kísérletek in vitro azt jelzik, hogy a razagilin mindkét metabolikus útja a citokróm P450 rendszertől függ; A CYP1A2 a fő izoenzim, amely részt vesz a razagilin metabolizmusában. Azt is megállapították, hogy a razagilin és metabolitjai konjugációja az egyik fő eliminációs út a glükuronidok képződésével.
Kiválasztás: A 14C-vel jelölt razagilin szájon át történő beadása után a gyógyszer elsősorban a vizelettel (62,6%) és a széklettel (21,8%) ürült ki, a dózis 84,4% -ának teljes visszanyerése 38 napos időszak alatt. A razagilin kevesebb mint 1% -a változatlan gyógyszerként ürül a vizelettel.
Linearitás / nemlinearitás: A razagilin farmakokinetikája lineáris a 0,5-2 mg közötti dózisoknál. Végső felezési ideje 0,6-2 óra.
A betegek jellemzői
Májelégtelenségben szenvedő betegek: Enyhe májelégtelenségben szenvedő betegeknél az AUC 80% -kal, míg a Cmax 38% -kal emelkedett. Közepesen súlyos májkárosodásban szenvedő betegeknél az AUC és a Cmax 568% -kal, illetve 83% -kal emelkedett (lásd 4.4 pont).
Veseelégtelenségben szenvedő betegek: Az enyhe (CLcr 50-80 ml / perc) vagy közepes (CLcr 30-49 ml / perc) veseelégtelenségben szenvedő betegeknél a razagilin farmakokinetikája hasonló volt az egészségesekéhez.
05.3 A preklinikai biztonságossági adatok
A hagyományos biztonságossági, ismételt dózistoxicitási és reprodukciós toxicitási vizsgálatok alapján a nem klinikai adatok nem mutatnak különleges veszélyt az emberre.
A razagilin nem rendelkezik genotoxikus potenciállal in vivo és számos rendszerben in vitro baktériumok és / vagy hepatociták felhasználásával. Aktív metabolitok jelenlétében a razagilin a kromoszóma -rendellenességek növekedését idézi elő túlzott citotoxikus koncentrációk esetén, amelyeket a klinikai felhasználás körülményei között nem használnak fel.
A razagilin nem volt rákkeltő patkányokban, ha a szisztémás expozíció 84-339-szerese volt a várható emberi plazmakoncentrációnak 1 mg / nap dózis mellett.
Egerekben megfigyelték a kombinált bronchioláris / alveoláris adenoma és / vagy karcinóma előfordulási gyakoriságát, a szisztémás expozíció 144-213-szor nagyobb volt, mint a várható humán plazmakoncentráció 1 mg / nap dózis esetén.
06.0 GYÓGYSZERÉSZETI INFORMÁCIÓK
06.1 Segédanyagok
Mannit
Kukoricakeményítő
Előzselatinizált kukoricakeményítő
Vízmentes kolloid szilícium -dioxid
Sztearinsav
Talkum
06.2 Inkompatibilitás
Nem releváns.
06.3 Érvényességi idő
Buborékfólia: 3 év
Palackok: 3 év
06.4 Különleges tárolási előírások
Legfeljebb 25 ° C -on tárolandó.
06.5 A közvetlen csomagolás jellege és a csomag tartalma
Buborékcsomagolás: Alumínium / alumínium buborékcsomagolás, 7, 10, 28, 30, 100 vagy 112 tablettát tartalmazó csomagolásban.
Palackok: Fehér, nagy sűrűségű polietilén palack gyermekbiztonsági kupakkal vagy anélkül, 30 tablettát tartalmaz.
Nem feltétlenül mindegyik kiszerelés kerül kereskedelmi forgalomba.
06.6 Használati utasítás
Nincsenek speciális utasítások.
07.0 FORGALOMBA HOZATALI ENGEDÉLY
Teva Pharma GmbH
Graf-Arco-Str. 3
89079 Ulm
Németország
08.0 A FORGALOMBA HOZATALI ENGEDÉLY SZÁMA
EU / 1/04/304 / 001-007
036983017
036983029
036983031
036983043
036983056
036983068
036983070
09.0 Az első forgalomba hozatali engedély kiadásának időpontja
Az első engedélyezés időpontja: 2005. február 21
Az utolsó megújítás dátuma: 2009. szeptember 21
10.0 A SZÖVEG FELÜLVIZSGÁLÁSÁNAK DÁTUMA
D.CCE 2013. november