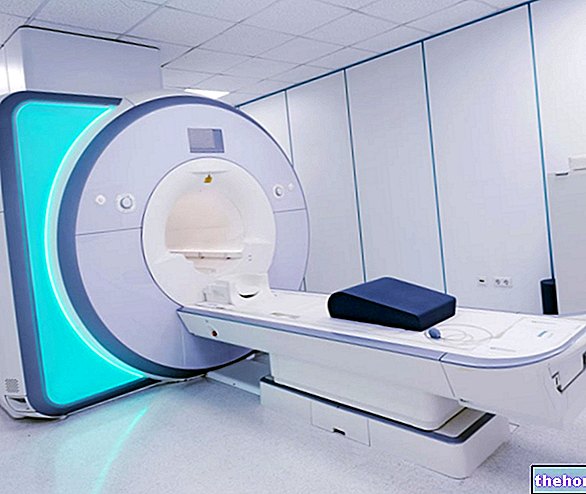
Hatóanyagok: Gestodene, Ethinylestradiol
MINULET 0,075 mg + 0,03 mg bevont tabletta
Indikációk Miért használják a Minulet -et? Mire való?
Farmakoterápiás kategória
A MINULET kombinált típusú fogamzásgátló orális alkalmazásra. Minden tabletta két különböző női hormont tartalmaz: gesztodént és etinil -ösztradiolt. Mivel a csomagolásban lévő összes tabletta ugyanazon hormonok kombinációját tartalmazza ugyanabban az adagban, a készítmény egyfázisú kombinált típusú orális fogamzásgátlónak minősül.
Terápiás javallatok
A fogamzás megelőzése.
A MINULET felírásáról szóló döntésnek figyelembe kell vennie az egyes nők jelenlegi kockázati tényezőit, különösen a vénás thromboemboliával (VTE) kapcsolatos tényezőket, valamint a MINULET -hez kapcsolódó VTE és más kombinált hormonális fogamzásgátlók (COC) kockázatának összehasonlítását. (Lásd "Ellenjavallatok", "Használati óvintézkedések" és "Különleges figyelmeztetések").
Ellenjavallatok Amikor a Minulet -et nem szabad használni
Kombinált hormonális fogamzásgátlók (COC) nem alkalmazhatók a következő esetekben.
Ha ezek jelen vannak, fontos, hogy tájékoztassa orvosát.
Vénás thromboembolia (VTE) jelenléte vagy kockázata
- Vénás thromboembolia - jelenlegi (véralvadásgátlóval) vagy korábbi VTE (pl. Mélyvénás trombózis [DVT] vagy tüdőembólia [PE])
- Ismert örökletes vagy szerzett hajlam a vénás tromboembóliára, például rezisztencia az aktivált C -fehérjével (beleértve az V. faktor Leiden -et), antitrombin III -hiány, C -fehérjehiány, S -proteinhiány
- Nagy műtét hosszan tartó immobilizációval (lásd "Használati óvintézkedések" és "Különleges figyelmeztetések" fejezetek)
- Nagy kockázata a vénás tromboembóliának több kockázati tényező jelenléte miatt (lásd "Használati óvintézkedések" és "Különleges figyelmeztetések" szakaszokat)
Artériás thromboembolia (ATE) jelenléte vagy kockázata
- Artériás thromboembolia - jelenlegi vagy korábbi artériás thromboembolia (pl. Miokardiális infarktus) vagy prodromális állapotok (pl. Angina pectoris) o cerebrovaszkuláris betegség - jelenlegi vagy korábbi stroke vagy prodromális állapotok (pl.
- Ismert örökletes vagy szerzett hajlam az artériás thromboemboliára, például hiperhomociszteinémia és antifoszfolipid antitestek (antikardiolipin antitestek, lupus antikoagulánsok)
- Fokális neurológiai tünetekkel járó migrén története
- Nagy kockázata az artériás tromboembóliának több kockázati tényező jelenléte miatt (lásd "Használati óvintézkedések" és "Különleges figyelmeztetések"), vagy olyan súlyos kockázati tényező jelenléte miatt, mint:
- • cukorbetegség érrendszeri tünetekkel
- súlyos hipertónia
- súlyos dyslipoproteinemia
- Sárgaság (a bőr sárgulása) vagy súlyos májbetegség, jelen vagy múlt.
- Korábbi vagy jelenlegi hasnyálmirigy -gyulladás, ha súlyos hipertrigliceridémiával jár együtt • Az emlő vagy a nemi szervek daganata (endometrium karcinóma), jelen vagy korábban.
- Jóindulatú vagy rosszindulatú májdaganat, jelen vagy korábbi.
- Ismeretlen eredetű hüvelyi vérzés.
- Ismert vagy feltételezett terhesség.
- Hipertónia, magas vérnyomás, magas vérnyomással kapcsolatos betegségek vagy vesebetegség.
- Ritonavirrel kombinálva.
- Túlérzékenység a hatóanyagokkal vagy bármely segédanyaggal szemben.
Ha ezen állapotok bármelyike először jelentkezik a termék használata közben, azonnal hagyja abba a szedését, és forduljon orvosához. Addig is használjon nem hormonális fogamzásgátló módszereket. Lásd még "Általános megjegyzések".
Az alkalmazással kapcsolatos óvintézkedések Mit kell tudnia a Minulet szedése előtt?
Általános megjegyzések
Ez a betegtájékoztató néhány olyan helyzetet ír le, amelyekben abba kell hagynia a készítmény szedését, vagy amelyekben a készítmény hatékonysága csökkenhet. Ilyen helyzetekben nem szabad nemi életet élni, vagy további nem hormonális fogamzásgátló óvintézkedéseket kell tennie, például óvszert vagy más gátló módszert. Ne használjon ritmus- és alaphőmérséklet-módszereket, amelyek megbízhatatlanok lehetnek, mivel a tabletta megváltoztatja a normálist a menstruációs ciklus során fellépő hőmérséklet- és nyaki nyálkahártya -változások.
A tabletta szedésének megkezdése vagy folytatása előtt ajánlatos alapos orvosi vizsgálatot végezni.
Ezenkívül ajánlatos rendszeres ellenőrző látogatásokat tenni, legalább évente egyszer, a termék használata során.
A látogatás gyakoriságát és típusát az orvos határozza meg, és különösen a vérnyomás ellenőrzésére, a mellre, a hasra és az általános nőgyógyászati vizsgálatra irányul, beleértve a Pap -tesztet és a relatív vérvizsgálatokat.
Az első utóvizsgálatot 3 hónappal a COC megkezdése után kell megtenni.
Mint minden fogamzásgátló tabletta, a MINULET sem véd a HIV -fertőzés (AIDS) vagy más nemi betegségek ellen.
A MINULET -et személyes használatra írják fel, és nem szabad, hogy egyidejűleg több ember számára elérhető legyen.
Óvintézkedések
Az alább felsorolt állapotok bármelyike fennállása esetén a kombinált tabletta alkalmazása szoros orvosi felügyeletet igényelhet, ezért a MINULET alkalmazása előtt figyelmeztetni kell kezelőorvosát a fenti állapotok bármelyikére. Orvosa javasolhat egy teljesen más (nem hormonális) fogamzásgátló módszert.
- füst;
- cukorbetegség;
- túlsúly;
- magas vérnyomás (lásd "Különleges figyelmeztetések");
- szívbillentyű hibák vagy bizonyos szívritmuszavarok;
- felületes phlebitis (vénás gyulladás);
- visszér;
- migrén (lásd "Különleges figyelmeztetések");
- depresszió (lásd "Különleges figyelmeztetések");
- epilepszia;
- a koleszterin és a trigliceridek (zsírok) jelenlegi vagy korábbi magas szintje a vérben, még a közeli családtagokban is (lásd "Különleges figyelmeztetések");
- melldarabok;
- mellrák története közeli hozzátartozóiban;
- máj- vagy epehólyag -betegség (lásd "Különleges figyelmeztetések");
- Crohn -betegség vagy fekélyes vastagbélgyulladás (krónikus gyulladásos bélbetegség);
- szisztémás lupus erythematosus (az egész test bőrét érintő betegség);
- hemolitikus-urémiás szindróma (veseelégtelenséget okozó véralvadási zavar);
- sarlósejtes vérszegénység;
- porfíria;
- jelenlegi vagy korábbi chloasma (sárgásbarna pigmentált foltok a bőrön, különösen az arcon). Ebben az esetben kerülje a napsugárzásnak vagy az ultraibolya sugaraknak való hosszú távú kitettséget;
- korábbi herpesz terhesség;
- egyes kóros állapotok, amelyeket az aktivált fehérje C -vel szembeni rezisztencia, hiperhomociszteinémia, antitrombin III hiány, fehérje C hiány, fehérje S hiány, antifoszfolipid antitest szindróma (antikardiolipin antitestek, lupus antikoaguláns) hajlamosítanak a vénás vagy artériás trombózis kialakulására;
- Sydenham chorea (központi idegrendszeri rendellenesség);
- halláskárosodás otosclerosis miatt.
Az első megjelenés, a fenti állapotok bármelyikének kiújulása vagy súlyosbodása esetén a tabletta használata során forduljon orvosához.
A Hypericum perforatum készítményeket nem szabad egyidejűleg orális fogamzásgátlókat, digoxint, teofillint, karbamazepint, fenobarbitált, fenitoint tartalmazó gyógyszerekkel együtt szedni, mivel csökkenhet az orális fogamzásgátlók, digoxin, teofillin, karbamazepin, fenobarbitál, fenitoin ( lásd az "Interakciók" részt).
Kölcsönhatások Mely gyógyszerek vagy ételek módosíthatják a Minulet hatását
Tájékoztassa kezelőorvosát vagy gyógyszerészét, hogy nemrégiben szedett egyéb gyógyszereket, beleértve a vény nélkül kapható készítményeket is.
Egyes gyógyszerek megakadályozhatják a tabletta hatékony működését. Ezek közé tartozik a primidon, fenitoin, barbiturátok, karbamazepin (epilepszia kezelésére használt gyógyszer), rifampicin (tuberkulózis kezelésére használt gyógyszer), ampicillin, tetraciklinek, griseofulvin (fertőző betegségek kezelésére használt antibiotikumok), ritonavir, modafinil, flunarizin, néhány proteáz inhibitor és nevirapin.
Más epilepszia elleni gyógyszerek (oxikarbamazepin, topiramát, felbamát) szintén valószínűleg csökkentik a tabletta hatékonyságát.
A Hypericum perforatum készítményeket nem szabad egyidejűleg alkalmazni az orális fogamzásgátlókkal, mivel a fogamzásgátlás hatékonysága csökkenhet. Nemkívánatos terhességről és a menstruációs ciklus újbóli megjelenéséről számoltak be. Ennek oka a Hypericumból származó gyógyszerek metabolizmusáért felelős enzimek indukciója. perforatum alapú készítmények. Az indukciós hatás a kezelés abbahagyása után legalább 2 hétig fennmaradhat.
Mindig tájékoztassa a tablettát felíró orvost a már szedett gyógyszereiről, és tájékoztasson minden más orvost vagy fogorvost, akik más gyógyszereket írnak fel, hogy Ön MINULET -et használ, hogy megállapíthassák, szükség van -e rá és meddig. Használjon további fogamzásgátló módszereket .
Anyagok, amelyek növelhetik a gyógyszer szérumkoncentrációját:
- atorvasztatin
- versenyképes gátlók a gasztrointesztinális falban, például aszkorbinsav (C -vitamin) és paracetamol (acetaminofen)
- a citokróm P450 3A4 izoenzimeket gátló anyagok, mint például az indinavir, flukonazol, vorikonazol és troleandomicin.
A troleandomicin fokozhatja az intrahepatikus cholestasis kockázatát a COC -k egyidejű alkalmazásakor.
Az etinil-ösztradiol befolyásolhatja más gyógyszerek anyagcseréjét a máj mikroszómális enzimeinek gátlásával vagy a máj gyógyszerkonjugációjának, különösen a glükuronokonjugációnak vagy más mechanizmusoknak a kiváltásával.
Következésképpen a plazma és a szövetek koncentrációja megemelkedhet (pl. Ciklosporin, teofillin, kortikoszteroidok) vagy csökkenhet (pl. Lamotrigin, levotiroxin, valproát).
A tabletta használata befolyásolhatja egyes vérvizsgálatok eredményét, de ezek a változások általában a normál tartományon belül vannak. Ezért tanácsos tájékoztatni a vizsgálatokat kért orvost arról, hogy Ön tablettát szed.
Figyelmeztetések Fontos tudni, hogy:
A gyógyszer laktózt és szacharózt tartalmaz, ezért cukor -intolerancia megállapítása esetén forduljon orvosához, mielőtt elkezdi szedni a gyógyszert.
Ha az alább felsorolt állapotok vagy kockázati tényezők bármelyike fennáll, a MINULET alkalmasságát meg kell beszélni a nővel.
Ezen kockázati tényezők vagy állapotok bármelyikének súlyosbodása vagy első megjelenése esetén a nőnek konzultálnia kell orvosával, hogy eldöntse, abba kell -e hagyni a MINULET alkalmazását.
Szívroham
A szívinfarktus fokozott kockázatát társították a COC -k alkalmazásával. A kockázat elsősorban a dohányosoknál vagy a szívkoszorúér -betegség egyéb kockázati tényezőivel rendelkező nőknél, például magas vérnyomás, hypercholesterinaemia, morbid elhízás, cukorbetegség. A kockázat nagyon alacsony. 30 év alatti.
A vénás thromboembolia (VTE) kockázata
Bármilyen kombinált hormonális fogamzásgátló (COC) alkalmazása a vénás thromboembolia (VTE) kockázatának növekedését eredményezi a használathoz képest. A levonorgesztrelt, norgesztimátot vagy noretiszteront tartalmazó termékek alacsonyabb VTE -kockázathoz társulnak. A MINULET kettős lehet. Az alacsonyabb VTE -kockázattal járó termékek használatától eltérő döntést csak a nővel folytatott megbeszélések után szabad meghozni, hogy megbizonyosodjon arról, hogy megérti a MINULET -hez kapcsolódó VTE kockázatát. a kockázati tényezők befolyásolják ezt a kockázatot, és azt a tényt, hogy a VTE kialakulásának kockázata a használat első évében a legmagasabb.
10 000 nő közül körülbelül 2 -nél, akik nem használnak kombinált kombinált kombinációt, és nem terhesek, VTE alakul ki egy év alatt. Egy egyedülálló nő esetében azonban a kockázat sokkal magasabb lehet, az alapul szolgáló kockázati tényezőktől függően (lásd alább).
Becslések szerint 1, 10 000 gesztodent tartalmazó CHC -t használó nő közül 9 és 12 között alakul ki VTE egy év alatt; ez körülbelül 62 nővel összehasonlítható, akik levonorgesztrelt tartalmazó CHC-t alkalmaznak.
Mindkét esetben a VTE -k száma évente kevesebb, mint a terhességben vagy a szülés utáni időszakban várható.
A VTE az esetek 1-2% -ában halálos kimenetelű lehet.
Epidemiológiai vizsgálatok kimutatták, hogy a vénás thromboembolia előfordulása az alacsony ösztrogén COC -k (COC) alkalmazóinál
Számos epidemiológiai vizsgálat során megfigyelték, hogy a nők, akik etinilösztradiolt tartalmazó kombinált orális fogamzásgátlót, többnyire 30 µg -os dózist és egy progesztint, például gesztodent használnak, nagyobb a trombózisos események és a vénás thromboembolia kockázata, mint a kombinált típusú orális fogamzásgátlót alkalmazó nőkhöz képest. kevesebb, mint 50 µg etinil -ösztradiolt és a progesztin levonorgesztrelt tartalmaz.
Más tanulmányok adatai azonban nem mutatták ezt a megnövekedett kockázatot.
Azoknál a termékeknél, amelyek 30 µg etinil -ösztradiolt és dezogesztrelt vagy gesztodent kombináltak, összehasonlítva azokkal, amelyek 50 µg -nál kevesebb etinil -ösztradiolt és levonorgesztrelt tartalmaznak, a vénás tromboembóliás események általános relatív kockázatát 1,5 és 2,0 között becsülték. A trombonikus események és a vénás thromboembolia előfordulása a levonorgesztrelt és kevesebb, mint 50 µg etinil-ösztradiolt tartalmazó kombinált orális fogamzásgátlók esetén körülbelül 20 eset 100 000 éves használat során. A MINULET esetében az incidencia körülbelül 30-40 eset 100 000 évre. azaz 10-20 további eset 100 000 nőévi felhasználásonként. Ez a szám összehasonlítható a nem használók 100 000 nőévre jutó 5-10 esetével.
A relatív kockázat hatása a további esetek számára a legnagyobb lenne az első évben, amikor egy nő először használ kombinált orális fogamzásgátlót.
Mindezt az információt figyelembe kell venni a COC felírásakor. A fogamzásgátló módszer (ek) kiválasztásának mérlegelésekor a fenti információkat mind figyelembe kell venni.
A trombózis olyan vérrögképződés, amely elzárhatja a vénás vagy artériás ereket.
Néha a lábak mély vénáit érinti (mélyvénás trombózis). Ha a vérrög leválik a vénából, amelyben létrejött, elérheti és eltömítheti a tüdő artériáit, ami az úgynevezett "tüdőembóliát" okozza. A mélyvénás trombózis ritka jelenség, és előfordulhat függetlenül attól, hogy beveszi -e a tablettát vagy sem; terhesség alatt is előfordulhat. A kockázat magasabb a tablettát szedő nőknél, mint azoknál, akik nem, de alacsonyabb, mint a terhes nőknél.
Nagyon ritka esetekben vérrögök is kialakulhatnak a szív ereiben (ahol szívrohamot okoznak) vagy az agyban (ahol agyvérzést okoznak). Nagyon ritkán jelentettek trombózist más erekben, például máj-, mesenterikus, vese- vagy retina -vénákban és artériákban a CHC -t alkalmazó betegeknél. Bizonyos esetekben a trombózis súlyos maradandó fogyatékosságot okozhat, vagy akár halálos is lehet.
A szívroham vagy a szélütés kockázata az életkorral és a füstölt cigaretták számával nő.A nők, akik szedik a tablettát, különösen a 35 év felettieknek abba kell hagyniuk a dohányzást.
Ha a vérnyomás emelkedik a tabletta használata során, szükség lehet a termék használatának abbahagyására.
Ha a trombózis lehetséges jeleit észleli, hagyja abba a tabletta szedését, és azonnal keresse fel orvosát (lásd még "Mikor kell orvoshoz fordulnia").
A VTE kockázati tényezői
A vénás tromboembóliás szövődmények kockázata a kombinált kombinált kombinációban részesülőknél jelentősen megnőhet, ha további kockázati tényezők vannak jelen, különösen, ha egynél több kockázati tényező van (lásd a táblázatot).
A MINULET ellenjavallt, ha egy nőnek számos kockázati tényezője van, amelyek növelik a vénás trombózis kockázatát (lásd "Ellenjavallatok" fejezet). Ha egy nőnek több kockázati tényezője van, lehetséges, hogy a megnövekedett kockázat nagyobb, mint az egyes tényezők összege; ebben az esetben figyelembe kell venni a VTE teljes kockázatát. Ha az előny / kockázat arány negatívnak tekinthető COC -t nem szabad felírni (lásd "Ellenjavallatok" fejezet).
Táblázat: A VTE kockázati tényezői
Nincs egyetértés a visszerek és a felszíni thrombophlebitis lehetséges szerepében a vénás trombózis kialakulásában és progressziójában.
Figyelembe kell venni a tromboembólia fokozott kockázatát a terhesség alatt, különösen a gyermekágyi időszak 6 hetes időszakában (a "Terhesség és szoptatás" témával kapcsolatos információkat lásd a "Terhesség és szoptatás" részben).
A VTE tünetei (mélyvénás trombózis és tüdőembólia)
Ha ilyen tünetek jelentkeznek, a nőknek azonnal orvoshoz kell fordulniuk, és tájékoztatniuk kell őket, hogy kombinált kombinált fogamzásgátlót szednek.
A mélyvénás trombózis (DVT) tünetei a következők lehetnek:
- a láb és / vagy a láb egyoldalú duzzanata vagy a láb vénája mentén;
- fájdalom vagy érzékenység a lábában, amely csak állva vagy járáskor érezhető;
- fokozott hőérzet az érintett lábon; vörös vagy elszíneződött bőr a lábán.
A tüdőembólia (PE) tünetei a következők lehetnek:
- hirtelen és megmagyarázhatatlan légszomj és gyors légzés;
- hirtelen köhögés, amely hemoptysissel járhat;
- éles fájdalom a mellkasban;
- súlyos szédülés vagy szédülés;
- gyors vagy szabálytalan szívverés.
Ezen tünetek némelyike (mint például a „légszomj” és a „köhögés”) nem specifikus, és előfordulhat, hogy rosszul értelmezik őket gyakoribb vagy kevésbé súlyos eseményként (pl. Légúti fertőzések).
Az erek elzáródásának egyéb jelei lehetnek: hirtelen fájdalom, duzzanat vagy az egyik végtag halványkék elszíneződése.
Ha az elzáródás a szemben történik, a tünetek a látás fájdalommentes homályosodásától a látásvesztésig terjedhetnek. Néha a látásvesztés szinte azonnal bekövetkezik.
Az artériás thromboembolia (ATE) kockázata
Az epidemiológiai vizsgálatok összefüggésbe hozták a CHC -k alkalmazását az artériás thromboembolia (miokardiális infarktus) vagy az agyi érrendszeri balesetek (pl. Átmeneti ischaemiás roham, stroke) fokozott kockázatával.
Az ATE kockázati tényezői
Az artériás tromboembóliás szövődmények vagy a cerebrovaszkuláris balesetek kockázata a kombinált kombinációban részesülő betegeknél megnő a kockázati tényezők jelenlétében (lásd a táblázatot). A MINULET ellenjavallt, ha egy nőnek van egy súlyos kockázati tényezője vagy több ATE kockázati tényezője, amelyek növelik az artériás trombózis kockázatát (lásd "Ellenjavallatok" fejezet). Ha egy nőnek több kockázati tényezője van, lehetséges, hogy a megnövekedett kockázat nagyobb, mint az egyes tényezők összege; ebben az esetben a teljes kockázatát kell figyelembe venni. Ha az előny / kockázat egyensúlyt negatívnak tekintik, COC -t nem szabad felírni (lásd "Ellenjavallatok" fejezet).
Táblázat: Az ATE kockázati tényezői
Az ATE tünetei
Ha ilyen tünetek jelentkeznek, a nőknek haladéktalanul fel kell venniük a kapcsolatot egy egészségügyi szakemberrel, és tájékoztatniuk kell őket, hogy kombinált kombinált gyógyszert szednek.
Az agyi érrendszeri baleset tünetei a következők lehetnek:
- hirtelen az arc, a kar vagy a láb zsibbadása vagy gyengesége, különösen a test egyik oldalán;
- hirtelen járási nehézség, szédülés, egyensúly vagy koordináció elvesztése;
- hirtelen zavartság, beszéd- vagy megértési nehézség;
- hirtelen látászavar az egyik vagy mindkét szemben;
- hirtelen, súlyos vagy elhúzódó migrén, ismeretlen ok nélkül;
- eszméletvesztés vagy ájulás rohamokkal vagy anélkül.
Az ideiglenes tünetek arra utalnak, hogy ez egy átmeneti ischaemiás roham (TIA).
A miokardiális infarktus (MI) tünetei a következők lehetnek:
- fájdalom, kellemetlen érzés, nyomás, nehézség, szorító érzés vagy teltség a mellkasban, a karban vagy a mellkas alatt;
- a hátba, állkapocsba, torokba, karba, gyomorba sugárzó kellemetlen érzés;
- teltségérzet, emésztési zavar vagy fulladás;
- izzadás, hányinger, hányás vagy szédülés;
- extrém gyengeség, szorongás vagy légszomj;
- gyors vagy szabálytalan szívverés.
Orvosi vizsgálatok / látogatások
Mielőtt elkezdené vagy folytatná a MINULET használatát, fel kell venni a teljes kórtörténetet (beleértve a családi anamnézist is), és ki kell zárni a terhességet. Meg kell mérni a vérnyomást, és el kell végezni az ellenjavallatok alapján végzett klinikai vizsgálatot (lásd "Ellenjavallatok" fejezetet). ) és figyelmeztetések (lásd "Használati óvintézkedések" és "Különleges figyelmeztetések" fejezeteket). Fontos felhívni a nők figyelmét a vénás vagy artériás trombózisra vonatkozó információkra, beleértve a MINULET -hez társuló kockázatot más kombinált kombinált kombinációkkal összehasonlítva, a VTE és az ATE tüneteit, az ismert kockázati tényezőket és a trombózis gyanúja esetén teendőket.
A nőt arra is figyelmeztetni kell, hogy figyelmesen olvassa el a betegtájékoztatót, és kövesse annak tanácsait. A vizsgálatok gyakoriságának és típusának megállapított iránymutatásokon kell alapulnia, és azokat az egyes nőkhöz kell igazítani.
A nőket tájékoztatni kell, hogy a hormonális fogamzásgátlók nem védenek a HIV -fertőzések (AIDS) és más nemi betegségek ellen.
Daganatok
Az emlőrák diagnosztizálása valamivel gyakoribb a tablettát használó nőknél, mint azoknál a nőknél, akik nem. Az emlőrák -diagnózisok számának enyhe növekedése fokozatosan eltűnik a kezelés abbahagyását követő 10 év során. Az emlőrák kialakulásának kockázati tényezői közé tartozik a növekvő életkor, a családtörténet, az elhízás, a nulliparitás és az idősebb kor az első teljes terhesség alatt.
A tablettát szedő nőknél jóindulatú májdaganatról és még ritkábban rosszindulatú májdaganatról számoltak be. Az ilyen daganatok belső vérzést okozhatnak. Erős hasi fájdalom esetén azonnal forduljon orvosához.
A méhnyakrák legfontosabb kockázati tényezője a tartós humán papillomavírus fertőzés.
A méhnyakrák (méhnyak) gyakoribbak azoknál a nőknél, akik hosszú ideig használják a tablettát.
Máj funkció
A májműködés akut vagy krónikus zavarai miatt a COC -kezelés felfüggesztése szükségessé válhat, amíg a májfunkciós paraméterek normalizálódnak.
Azok a nők, akiknek kórtörténetében COC-vel összefüggő epepangás van, vagy akiknél epepangás alakul ki terhesség alatt, nagyobb valószínűséggel tapasztalják ezt az állapotot a COC-k alkalmazása során.
Ezeket a betegeket gondosan ellenőrizni kell, és ha az állapot megismétlődik, a COC -t abba kell hagyni.
A májműködés akut vagy krónikus zavarai miatt szükség lehet a COC -kezelés abbahagyására mindaddig, amíg a májfunkció normalizálódik.
A COC-k alkalmazása során májsejt-károsodást jelentettek. A gyógyszerrel kapcsolatos hepatocellularis károsodás korai diagnózisa csökkentheti a hepatotoxicitás súlyosságát a gyógyszer abbahagyásakor. Ha májfunkció-károsodást diagnosztizálnak, a betegeknek abba kell hagyniuk a COC szedését, nem hormonális fogamzásgátló módszert kell alkalmazniuk, és konzultálniuk kell orvosukkal.
Szem sérülések
Retina trombózis eseteiről számoltak be a COC -k alkalmazása során. Ha megmagyarázhatatlan részleges vagy teljes látásvesztés, proptosis vagy diplopia megjelenése, papilláris ödéma vagy a retina érrendszeri elváltozásai jelentkeznek, a COC alkalmazását abba kell hagyni, és azonnal kivizsgálják.
Migrénes fejfájás
A migrén megjelenése vagy súlyosbodása, vagy fejfájás kialakulása, amelynek jellegzetessége ismétlődő, tartós és súlyos, olyan helyzeteket jelent, amelyek megkövetelik a COC abbahagyását és az ok felmérését.
A COC -t szedő migrénes (különösen aurás migrénes) nőknél fokozott a stroke kockázata (lásd "Ellenjavallatok").
Angioödéma
Az exogén ösztrogének kiválthatják vagy súlyosbíthatják az angioödéma tüneteit, különösen örökletes angioödémában szenvedő nőknél.
Hatások a lipid- és szénhidrát -anyagcserére
Glükóz intoleranciáról számoltak be COC -t alkalmazó betegeknél. Bár a COC -k befolyásolhatják a perifériás inzulinrezisztenciát és glükóztoleranciát, nincs bizonyíték arra, hogy kombinált orális fogamzásgátlót alkalmazó betegeknél szükség van az adagolás módosítására. Mindazonáltal a cukorbetegségben szenvedő vagy glükóz intoleranciában szenvedő betegeket gondosan ellenőrizni kell a COC szedése során (lásd "Használati óvintézkedések").
A COC szedése során egyes nőknél változhatnak a lipidértékek. Nem hormonális fogamzásgátló módszert kell alkalmazni azoknál a nőknél, akiknél a diszlipidémia nem kontrollált. A kombinált orális fogamzásgátlót alkalmazó nők kis hányadánál tartós hipertrigliceridémia fordulhat elő. A megnövekedett plazma trigliceridszint a COC -használóknál hasnyálmirigy -gyulladáshoz és egyéb szövődményekhez vezethet.
Az ösztrogén növeli a nagy sűrűségű plazma lipoproteint (HDL-koleszterint), míg a HDL-koleszterin csökkenéséről számoltak be számos progesztogén esetében.
Egyes progesztogének növelhetik az alacsony sűrűségű lipoprotein (LDL) koncentrációt, és megnehezíthetik a hiperlipidémia szabályozását.
A kombinált orális fogamzásgátló hatása az egyes ösztrogén- és progesztogén adagok hatása közötti egyensúlytól, valamint a fogamzásgátlóban alkalmazott progesztogének jellegétől és teljes mennyiségétől függ. Mindkét hormon tartalmát figyelembe kell venni a kombinált orális fogamzásgátló kiválasztása.
A hiperlipidémia miatt kezelt nőket gondosan figyelemmel kell kísérni, ha COC -t választanak.
Folsavszint
A szérum folsav szintje csökkenthető kombinált orális fogamzásgátló kezeléssel. Ennek klinikai jelentősége lehet, ha a nő nem sokkal a COC abbahagyása után teherbe esik.
Vérnyomás
Az orális fogamzásgátlók alkalmazása ellenjavallt magas vérnyomású, magas vérnyomással vagy vesebetegségben szenvedő, vagy korábban magas vérnyomásban szenvedő nőknél. Bár sok COC -t szedő nőnél kismértékű vérnyomásemelkedésről számoltak be, klinikailag jelentős vérnyomás -emelkedés ritkán fordul elő. A COC -kezelés és a magas vérnyomás közötti összefüggést nem állapították meg, azonban ha klinikailag szignifikáns magas vérnyomás jelentkezik a COC alkalmazása során, az orvosnak elővigyázatosságból abba kell hagynia a COC szedését, és kezelnie kell a beteget. "Hypertonia.
Az érzelmi szféra zavarai
Azoknak a nőknek, akik COC-k szedése alatt mentális depresszióban szenvednek, abba kell hagyniuk a kezelést, és alternatív fogamzásgátló módszert kell alkalmazniuk annak megállapítására, hogy ez a tünet a kábítószerrel kapcsolatos-e. A depresszióban szenvedő és orális fogamzásgátlót szedő nőket gondosan figyelemmel kell kísérni, és abba kell hagyni, ha súlyos depresszió lép fel.
Szabálytalan vérzés
Rendellenes vérzés (pecsételő vagy intermenstruációs vérzés) fordulhat elő bármilyen COC szedése közben, különösen a kezelés első hónapjaiban. Ezért az esetleges szabálytalan hüvelyi vérzések értékelése csak a körülbelül 3 kezelési ciklusos rendeződési fázis után van értelme.
Ha a rendszertelen vérzés továbbra is fennáll, vagy a korábban rendszeres ciklusok után következik be, akkor nem hormonális etiológiát kell mérlegelni, és megfelelő diagnosztikai intézkedéseket kell alkalmazni, beleértve a curettage-t, hogy kizárják a rosszindulatú betegséget vagy a terhességet.
Néhány nőnél a tablettamentes időszak alatt nem fordulhat elő elvonási vérzés. Ha a COC-t az "Adagolás, az alkalmazás módja és ideje" pontban leírtak szerint vették be, nem valószínű, hogy a nő terhes. A terhesség azonban nem valószínű . Ha a COC -t nem megfelelően vették be a kihagyott elvonási vérzés előtt, vagy ha két elvonási vérzés nem következett be, akkor a COC szedésének folytatása előtt ki kell zárni a terhességet. Néhány nőnél az orális fogamzásgátló abbahagyása után amenorrhoea (lehetséges ovuláció hiánya) vagy oligomenorrhoea, különösen akkor, ha ez az állapot már fennállt.
Laboratóriumi tesztek
A fogamzásgátló szteroidok alkalmazása befolyásolhatja egyes laboratóriumi vizsgálatok eredményeit, beleértve a májfunkciós vizsgálatokat (beleértve a bilirubin és az alkalikus foszfatáz csökkenését), a pajzsmirigyet (az összes T3 és T4 növekedése a TBG növekedése miatt, a szabad T3 gyanta abszorpciójának csökkenése) , mellékvese (megnövekedett plazma kortizol, megnövekedett kortizol-kötő globulin, csökkent dehidroepiandroszteron-szulfát) és vese (megnövekedett plazma kreatinin és csökkent kreatinin clearance), plazmaszint transzportfehérjék, például kortikoszteroid-kötő globulin és lipid / lipoprotein frakciók, glükóz metabolizmus, koaguláció és fibrinolízis, a szérum folsavszint csökkenése. A változások általában a normál laboratóriumi értékek tartományán belül vannak.
Terhesség és szoptatás
A MINULET nem alkalmazható ismert vagy feltételezett terhesség esetén. Ha terhesség következik be a COC alkalmazása során, a kezelést abba kell hagyni. Nincs meggyőző bizonyíték arra vonatkozóan, hogy a COC -ben lévő ösztrogének és progesztogének károsíthatják a magzatot, ha a fogamzásgátlás véletlenül következik be a COC kombinált alkalmazása során (lásd "Ellenjavallatok").
A szülés utáni időszakban a tromboembólia fokozott kockázatát figyelembe kell venni a "MINULET újraindításakor" (lásd az "Adagolás, az alkalmazás módja és ideje", "Az alkalmazással kapcsolatos óvintézkedések" és "Különleges figyelmeztetések" fejezeteket).
A MINULET nem ajánlott szoptatás alatt.
Gyermekgyógyászati felhasználás
A COC -k biztonságosságát és hatásosságát reproduktív korú nőknél állapították meg.Ezeknek a gyógyszereknek a használata a menstruáció előtt nem javasolt.
Geriatriai használat
A COC -k nem javallottak a posztmenopauzás nőknél.
Hatások a gépjárművezetéshez és gépek kezeléséhez szükséges képességekre
A MINULET -et nem vizsgálták a gépjárművezetéshez és gépek kezeléséhez szükséges képességekre gyakorolt hatása miatt.
MIKOR KONZULTENI AZ ORVOSÁVAL
Időszakos ellenőrzések
A tabletta használata közben az orvos felkéri a beteget, hogy rendszeresen ellenőrizze, általában évente.
A lehető leghamarabb keresse fel orvosát:
- ha bármilyen változást észlel egészségi állapotában, különösen a betegtájékoztatóban leírtakkal kapcsolatban (lásd még "Ellenjavallatok" és "Használattal kapcsolatos óvintézkedések". Ne felejtse el a közeli családtagokra vonatkozó hivatkozásokat);
- ha csomót érez a mellében;
- ha más gyógyszereket kell alkalmazni (lásd még "Interakciók");
- ha immobilizált vagy műteni kell (legalább négy héttel előtte konzultáljon orvosával);
- ha súlyos és szokatlan hüvelyi vérzése van;
- ha kihagyott egy tablettát a használat első hetében, és az elfelejtést megelőző hét napban nemi életet folytatott;
- ha két egymást követő ciklusban nincs menstruációja, vagy ha terhességet gyanít, ne kezdjen új csomagot orvosa engedélye nélkül.
Hagyja abba a tabletták szedését, és azonnal forduljon orvosához, ha a trombózis lehetséges jeleit észleli:
- hirtelen kezdődő köhögés;
- súlyos fájdalom a mellkasban, amely a bal karba sugározhat;
- hirtelen légszomj;
- szokatlan, súlyos, hosszan tartó fejfájás vagy migrénes roham;
- részleges vagy teljes látásvesztés vagy kettős látás;
- homályos beszéd vagy képtelenség beszélni;
- hirtelen változások a hallásban, az illatban és az ízben;
- szédülés vagy ájulás; • bármely testrész gyengesége vagy zsibbadása;
- súlyos hasi fájdalom;
- súlyos fájdalom vagy duzzanat az egyik lábában;
A fenti helyzeteket és tüneteket a betegtájékoztató más szakaszai illusztrálják és részletesebben kifejtik.
Adagolás és alkalmazás A Minulet használata: Adagolás
Hogyan kell szedni a MINULET -et?
A MINULET csomag 21 tablettát tartalmaz. Egy tablettát naponta 21 egymást követő napon kell bevenni, majd 7 napos szünetet kell tartani. Az első tablettát az 1-es jelzésű naptárcsomagolásból (a "START" szó mellett) kell kivenni. A következő tabletta másnap kell venni a közeli dobozból, a nyilak számozását és irányát követve.
Szúrja át a buborékfóliát azon a napon, amikor elkezdi szedni a tablettákat.
A hét ugyanaz a napja jelenti a következő csomag kezdő napját; ezenkívül a hét ugyanazon napját jelenti, amikor az 1., 8. és 15. tablettát veszik be. Ez segít ellenőrizni és megbizonyosodni arról, hogy helyesen vette be a tablettákat.
A tablettákat rágás nélkül kell lenyelni, rendszeresen, lehetőleg mindig ugyanabban az időben, lehetőleg az esti étkezés után.
A későbbi ciklusok
Miután mind a 21 tablettát bevette, hagyja abba a szedését 7 napig.Ezen 7 nap alatt vérzést tapasztal, általában 2-3 nappal az utolsó tabletta bevétele után. A következő MINULET -csomagot a 8. napon kezdje el, még akkor is, ha a vérzés még mindig tart. Ez azt jelenti, hogy a MINULET második csomagját pontosan ugyanazon a napon kezdik el használni, mint az első csomagot, négy héttel korábban.
Az első csomag kezdete
Az előző hónapban nem volt hormonális fogamzásgátló.
A MINULET szedését a ciklus első napján, azaz a menstruáció első napján kezdje el, az 1 -es számmal jelölt tabletta bevételével (lásd a "Hogyan kell szedni a MINULET -et" című részt). A menstruáció második és ötödik napja között is elkezdheti ciklus, de ebben az esetben kiegészítő fogamzásgátló módszert (gátló módszer) kell alkalmazni a tabletták bevételének első hét napjában az első ciklusban.
Váltás egy másik "kombinált típusú" tablettáról.
A MINULET szedését az előző fogamzásgátló utolsó tablettája utáni napon kezdheti el (azaz szünet nélkül). Ha az előző fogamzásgátló csomag inaktív tablettákat is tartalmaz, a MINULET -et az utolsó aktív tabletta utáni napon veheti be (ha kétségei vannak , kérdezze meg orvosát). Később is el lehet kezdeni, de soha nem az előző fogamzásgátló tablettamentes intervallumát követő napon (vagy az utolsó inaktív tabletta utáni napon).
Váltás csak progesztogént tartalmazó tablettáról (minipillum).
Bármelyik napon abbahagyhatja a minipill szedését, és másnap ugyanabban az időben elkezdheti szedni a MINULET -et. Azonban a tabletták bevételének első hét napján használjon kiegészítő fogamzásgátló módszert (gátló módszer) közösülés során.
Injekcióról, implantátumról vagy méhen belüli fogamzásgátlóról való váltás.
Kezdje el a MINULET használatát azon a napon, amikor a következő, csak progesztogént tartalmazó készítmény injekció esedékes, vagy azon a napon, amikor eltávolítják a csak progesztogént tartalmazó implantátumot vagy a csak progesztogént tartalmazó méhen belüli eszközt. szexelni.
Szülés után.
A tabletta szülés utáni megkezdését az orvosnak kell meghatároznia. Ő dönti el, hogy a 21. és 28. nap közötti időszakban, vagy később kezdi -e a kezelést. Utóbbi esetben célszerű további gátló módszert alkalmazni a MINULET tabletta szedésének első 7 napjában. Ha azonban időközben szexuális kapcsolat történt, ki kell zárni a terhességet, vagy meg kell várni az első menstruációt, mielőtt ténylegesen elkezdené a MINULET szedését.
Ha szoptat, és MINULET -et szeretne szedni, először beszéljen kezelőorvosával.
Spontán vagy indukált abortusz után.
Kövesse orvosa receptjét.
Munkaviszony megszüntetése
A MINULET alkalmazását bármikor abbahagyhatja. Ha nem szeretne teherbe esni, konzultáljon orvosával a fogamzásgátlás egyéb módszereiről.
Ha abba akarja hagyni a MINULET használatát, mert anyaságot szeretne, akkor beszéljen kezelőorvosával, ebben az esetben általában tanácsos megvárni, amíg a menstruációja ismét rendszeres lesz, mielőtt teherbe esne.
MIT TEGYEN, HA ...
elfelejtette bevenni a tablettákat
- Ha kevesebb, mint 12 óra telt el a szokásos bevitel óta, a tabletta megbízhatósága megmarad. Vegye be az elfelejtett tablettát, amint eszébe jut, és folytassa a szokásos módon.
- Ha több mint 12 óra telt el a szokásos bevitel időpontja óta, vagy ha nem vett be 2 vagy több tablettát, a tabletta megbízhatósága csökkenhet. Minél nagyobb az egymás után elfelejtett tabletták száma, annál nagyobb a kockázata annak, hogy a fogamzásgátló hatás csökken. Kövesse az alábbi utasításokat (lásd még az alábbi ábrát).
Egynél több elfelejtett tabletta egy csomagban
Forduljon orvosához.
Egy tabletta elfelejtett az első héten
Vegye be a tablettát, amint eszébe jut (még akkor is, ha ez két tabletta egyidejű bevételét jelenti), és folytassa a szokásos módon. Használjon további fogamzásgátló módszereket (gátló módszer) a következő 7 napban.
Ha a felejtést megelőző héten szexuális kapcsolatra került sor, fennáll a terhesség lehetősége. Azonnal értesítse orvosát.
A második héten elfelejtett bevenni egy tablettát
Vegye be az elfelejtett tablettát, amint eszébe jut (még akkor is, ha ez két tabletta egyidejű bevételét jelenti), és folytassa a szokásos módon. A tabletta megbízhatósága megmarad, további fogamzásgátló intézkedésekre nincs szükség.
Egy tabletta elfelejtett a harmadik héten
Az alábbi alternatívák egyike választható, további fogamzásgátló óvintézkedések nélkül.
- Vegye be az elfelejtett tablettát, amint eszébe jut (még akkor is, ha ez két tabletta egyidejű bevételét jelenti), és folytassa a szokásos módon. Indítsa el az új csomagot, amint az aktuális befejeződött, és nincs különbség a két csomag között. Elvonási vérzés nem fordulhat elő, amíg a második csomag be nem fejeződik, de intermenstruális vérzés (foltosodás) előfordulhat a bevétel napjai alatt.
- Hagyja abba a tabletta szedését a jelenlegi csomagolásból, tartsa be a 7 napos vagy annál rövidebb intervallumot (a kimaradt tabletta napját is számolja), és folytassa új csomagolással. Ha ezt az alternatívát választja, az új csomagot mindig ugyanazon a napon kezdheti el, amelyen általában elkezdi.
Ha elfelejtett bevenni egy vagy több tablettát, és nincs menstruációja az első tablettamentes időszakban, lehetséges, hogy terhes. Az új csomagolás megkezdése előtt konzultáljon orvosával.
Hányás és / vagy hasmenés esetén
Ha hányás vagy hasmenés jelentkezik a MINULET bevételét követő 4 órán belül, a hatóanyag felszívódása hiányos lehet. Mintha elfelejtette volna a tablettát. A fentiekben leírtak szerint új csomagolású tablettákat kell használni, ezért kövesse az utasításokat az elfelejtett tabletta esetén.
Váratlan vérzés esetén
Minden orális fogamzásgátlónál hüvelyi vérzés léphet fel a menstruáció közötti szedés első hónapjaiban.Általában a rendszertelen vérzés eltűnik, amint a szervezet megszokta a tablettát (általában körülbelül 3 feltételezési ciklus után). Mindig tanácsos konzultálni orvosával, de különösen akkor, ha ezek a vérzések továbbra is fennállnak, intenzívebbé válnak vagy időnként megismétlődnek.
Kimaradt menstruáció esetén
Ha minden tablettát helyesen vett be, hányás nem következett be, vagy más gyógyszert nem szedtek, akkor nagyon valószínűtlen, hogy terhes. Folytassa a termék szokásos használatát.
Ha a menstruációja nem fordul elő kétszer egymás után, akkor lehetséges, hogy terhes. Azonnal forduljon orvosához. Ne kezdje el az új csomagolást, amíg orvosa kizárta a terhességet.
Túladagolás Mi a teendő, ha túl sok Minulet -t vett be?
A kombinált orális fogamzásgátló túladagolásának tünetei felnőtteknél és gyermekeknél: hányinger, mellkasi szorítás, zavartság, hasi fájdalom, álmosság / fáradtság, elvonási vérzés.
Nincsenek specifikus ellenszerek, és minden további kezelésnek tüneti jellegűnek kell lennie.
A MINULET túlzott adagjának véletlen lenyelése / bevétele esetén azonnal értesítse orvosát, vagy menjen a legközelebbi kórházba.
Ha bármilyen további kérdése van a MINULET alkalmazásával kapcsolatban, kérdezze meg kezelőorvosát vagy gyógyszerészét.
Mellékhatások Melyek a Minulet mellékhatásai?
Mint minden MINULET gyógyszer, ez is okozhat mellékhatásokat, amelyek azonban nem mindenkinél jelentkeznek.
Ha bármilyen mellékhatást észlel, különösen, ha azok súlyosak és tartósak, vagy megváltozott az egészségi állapota, amelyet úgy gondol, hogy a tabletta okozhat, forduljon orvosához.
A kombinált orális fogamzásgátlót alkalmazó nők esetében fokozott a vénás thromboembolia (VTE) kockázata. A COC -k közötti kockázatkülönbségekre vonatkozó információkért lásd a Különleges figyelmeztetések részt.
Súlyos mellékhatások
A tabletták használatával kapcsolatos súlyos reakciókat és a kapcsolódó tüneteket, amelyek a kezelés abbahagyását írják le, szintén a "Használati óvintézkedések" fejezetben találja: "Trombózis" és "Daganatok":
- artériás thromboemboliás balesetek (különösen miokardiális infarktus, cerebrovaszkuláris baleset, átmeneti ischaemiás roham);
- vénás thromboemboliás balesetek (phlebitis, tüdőembólia);
- magas vérnyomás, koszorúér -betegség;
- hiperlipidémia (hipertrigliceridémia és / vagy hiperkoleszterinémia)
- súlyos mastodynia, jóindulatú mastopathia;
- intenzív és szokatlan fejfájás, migrén, szédülés, látásváltozások;
- az epilepszia súlyosbodása;
- májsejtes karcinóma, kolesztatikus sárgaság;
- chloasma;
- látóideggyulladás, a retina vaszkuláris trombózisa
Néhány mellékhatás leírása
Fokozott kockázat:
- artériás és vénás trombotikus és tromboembóliás események, beleértve a miokardiális infarktust, a stroke -ot, az átmeneti iszkémiás rohamokat, a vénás trombózist és a tüdőembóliát, és ezt a kockázatot részletesebben tárgyalja a "Használati óvintézkedések" és "Különleges figyelmeztetések" szakaszokban;
- méhnyak intraepithelialis neoplasia és méhnyakrák;
- mellrák diagnosztizálása.
- jóindulatú májdaganatok (pl. fokális nodularis hyperplasia, máj adenoma)
További információkért olvassa el a betegtájékoztató ezeket a részeit, és azonnal forduljon orvosához.
Egyéb mellékhatások
A következő mellékhatásokat jelentették a tablettát szedő nőknél:
A leggyakoribb szövődmények:
- mellfeszülés, megnagyobbodás, fájdalom és váladék
- fejfájás, migrén
- változások a szexuális vágyban, depressziós hangulat, ingerlékenység
- intolerancia a kontaktlencsékkel szemben
- hányinger, rossz közérzet
- idegesség
- változások a hüvelyi váladékban
- folyadékretenció / ödéma
- testtömegváltozások (növekedés vagy csökkenés), étvágyváltozások (növekedés vagy csökkenés)
- túlérzékenységi reakciók
- oligomenorrhea, amenorrhoea, dysmenorrhoea
- intermenstruációs vérzés
- hüvelygyulladás, beleértve a candidiasisot is
Ritka szövődmények:
- hányás, hasi fájdalom és hasi görcsök
- depresszió
- bőrbetegségek (akne, alopecia, seborrhea, hypertrichosis, kiütés, nodosum erythema, erythema multiforme)
- túlérzékenységi reakciók, beleértve nagyon ritka csalánkiütéses eseteket, angioödémát és súlyos légzési és keringési tünetekkel járó reakciókat; a szisztémás lupus erythematosus súlyosbodása
- a visszerek súlyosbodása
- dagadt érzés
- hasnyálmirigy -gyulladás
- ischaemiás colitis
- epeúti lithiasis
- gyulladásos bélbetegség (Crohn -betegség, fekélyes vastagbélgyulladás)
- a szérum folsavszint csökkenése.
A COC-k súlyosbíthatják a már meglévő epehólyag-betegséget, és felgyorsíthatják e betegség kialakulását korábban tünetmentes nőknél.
A betegtájékoztatóban található utasítások betartása csökkenti a nemkívánatos hatások kockázatát.
Mellékhatások bejelentése
Ha Önnél bármilyen mellékhatás jelentkezik, tájékoztassa erről kezelőorvosát vagy gyógyszerészét. Ez a betegtájékoztatóban fel nem sorolt bármilyen lehetséges mellékhatásra is vonatkozik. A nemkívánatos hatások közvetlenül a nemzeti bejelentési rendszeren keresztül is bejelenthetők a www.agenziafarmaco.gov.it/it/responsabili címen. A mellékhatások bejelentésével Ön is hozzájárulhat ahhoz, hogy több információ álljon rendelkezésre a gyógyszer biztonságosságáról. "
Lejárat és megőrzés
Lásd a csomagoláson feltüntetett lejárati dátumot.
FIGYELEM: NE HASZNÁLJA A GYÓGYSZERET A CSOMAGOLÁSON feltüntetett lejárati idő után.
A feltüntetett lejárati idő az ép csomagolású termékre vonatkozik, helyesen tárolva.
Különleges tárolási előírások
Legfeljebb 25 ° C -on tárolandó.
A gyógyszereket nem szabad a szennyvízzel vagy a háztartási hulladékkal együtt megsemmisíteni. Kérdezze meg gyógyszerészét, hogy mit tegyen a már nem használt gyógyszereivel. Ez elősegíti a környezet védelmét.
A gyógyszer gyermekektől elzárva tartandó!
Összetétel és gyógyszerforma
Fogalmazás
Minden bevont tabletta tartalma: Hatóanyagok: 0,075 mg gesztodén; 0,03 mg etinilösztradiol.
Segédanyagok: laktóz, kukoricakeményítő, povidon 25 000, nátrium -kalcium -edetát, magnézium -sztearát, szacharóz, 700 000 povidon, makrogol 6000, kalcium -karbonát, talkum, montán -sav etilénglikol -észtere (E viasz).
Gyógyszerészeti forma és tartalom
Bevonatos tabletta szájon át.
Kartondoboz, amely 1, 21 bevont tablettát tartalmazó naptárcsomagot tartalmaz.
Forrás betegtájékoztató: AIFA (Olasz Gyógyszerügynökség). A tartalom 2016 januárjában jelent meg. A jelenlévő információk nem feltétlenül naprakészek.
A legfrissebb verzióhoz való hozzáféréshez ajánlatos az AIFA (Olasz Gyógyszerügynökség) webhelyét elérni. Jogi nyilatkozat és hasznos információk.
01.0 A GYÓGYSZER MEGNEVEZÉSE
MINULET 0,075 MG + 0,03 MG bevont tabletta
02.0 MINŐSÉGI ÉS MENNYISÉGI ÖSSZETÉTEL
Minden bevont tabletta tartalmaz:
Hatóanyagok: gesztodén 0,075 mg; 0,03 mg etinilösztradiol.
A segédanyagok teljes listáját lásd a 6.1 pontban.
03.0 GYÓGYSZERFORMA
Bevonatos tabletta szájon át.
04.0 KLINIKAI INFORMÁCIÓK
04.1 Terápiás javallatok
A fogamzás megelőzése.
04.2 Adagolás és alkalmazás
FELVÉTELI MÓDSZER
A MINULET csomag 21 tablettát tartalmaz. Naponta egy tablettát kell bevenni 21 egymást követő napon keresztül, majd 7 napon keresztül fel kell függeszteni a bevételt.
A következő tablettát másnap kell bevenni a közeli dobozból, a nyilak irányát követve: így napról napra könnyen ellenőrizhető, hogy a tablettát bevette -e vagy sem.
A tablettákat rágás nélkül kell lenyelni, minden nap, lehetőleg ugyanabban az időben, lehetőleg az esti étkezés után.
Mind a 21 tabletta bevétele után hagyja abba a szedését 7 napig.
Az elvonási vérzés általában 2-3 nappal az utolsó tabletta bevétele után kezdődik, és előfordulhat, hogy nem fejeződik be a következő csomag megkezdése előtt.
Minden következő csomagolás a tablettamentes szünet utáni napon kezdődik.
Ez azt jelenti, hogy a MINULET második csomagját pontosan ugyanazon a napon kezdik el használni, mint az első csomagot, négy héttel korábban.
HOGYAN KEZDJE A KEZELÉSET MINULETTEL?
Az előző hónapban nem volt hormonális fogamzásgátló kezelés
A MINULET tabletta szedését a természetes menstruációs ciklus 1. napján (azaz a menstruáció első napján) kell kezdeni. A MINULET -et a ciklus 2. és 5. napja között is el lehet kezdeni, de ebben az esetben az első ciklusban is javasolt a nem hormonális fogamzásgátló módszer (pl. óvszer vagy spermicid) alkalmazása a MINULET tabletta szedésének első hét napjában.
Váltás másik kombinált orális fogamzásgátlóra
A MINULET első tablettáját lehetőleg az előző fogamzásgátló utolsó aktív tabletta utáni napján, vagy legkésőbb a szokásos tablettamentes szünetet követő napon, vagy az előző orális fogamzásgátló utolsó placebo-tabletta utáni napon vegye be.
Váltás csak progesztogént tartalmazó fogamzásgátlóról (minipillum, implantátum, méhen belüli eszköz, injekcióhoz előkészítve)
Bármikor megváltoztatható, ha a minipilliből érkezik, és a MINULET bevételét a következő napon kell megkezdeni. Implantátum esetén a MINULET bevételét a csak progesztogént tartalmazó implantátummal azonos napon kell elkezdeni vagy a csak progesztogént tartalmazó méhen belüli eszközt eltávolítják, vagy csak progesztogént tartalmazó injekciós készítmény esetén a következő injekció beadásának napján. Mindezekben az esetekben a nőt nem hormonális fogamzásgátló használatáról is tanácsolni kell támogatási módszer a MINULET tabletta szedésének első hét napján.
Az első trimeszter abortusz után
A MINULET -kezelést azonnal el lehet kezdeni további fogamzásgátló intézkedések nélkül.
Szülés vagy második trimeszter abortusz után
Mivel a közvetlen szülés utáni időszak a thromboembolia fokozott kockázatával jár, a nem szoptató anyáknál vagy a második trimeszterben történt abortusz után a MINULET-et nem szabad korábban, mint a szülés utáni 21-28. Napon elkezdeni. hormonális fogamzásgátló módszer a MINULET tabletta szedésének első hét napjában. Ha azonban a közösülés időközben bekövetkezett, a MINULET tényleges megkezdése előtt ki kell zárni a terhességet, vagy meg kell várni az első menstruációt (lásd 4.4 "Tromboembólia" és 4.6 pont).
A TABLETTA SZABÁLYTALAN FELVÉTELE
A fogamzásgátló hatás csökkenhet, ha elfelejtette bevenni a tablettákat, különösen, ha az elfelejtés a kezelési ciklus első napjaiban következik be.
Ha a tabletta bevételének késése kevesebb, mint 12 óra a szokásos időponttól, a fogamzásgátló védelem nem csökken.Az elfelejtett tablettát az elfelejtett tabletta után kell bevenni, és a következő tablettákat a szokásos időben kell bevenni.
Ha bármelyik tabletta bevételének késése több mint 12 óra a szokásos időponttól, vagy ha nem vett be 2 vagy több tablettát, akkor a fogamzásgátló védelem már nem biztosított. Következésképpen az alábbi javaslatok adhatók a napi gyakorlatban.
Első hét
Az utolsó kihagyott tablettát azonnal vegye be, amint észreveszi az elfelejtett tablettát, még akkor is, ha ez azt jelenti, hogy két tablettát kell bevennie ugyanazon a napon. Ezenkívül a következő 7 napban nem hormonális fogamzásgátló módszert (pl. Óvszert) kell alkalmazni. . Ha az előző héten szexuális kapcsolatra került sor, akkor figyelembe kell venni a terhesség lehetőségét. Minél nagyobb a kihagyott tabletták száma és minél rövidebb a tablettamentes intervallum, annál nagyobb a terhesség kockázata.
Második hét
Az utolsó kihagyott tablettát azonnal vegye be, amint észreveszi az elfelejtett tablettát, még akkor is, ha ez két tabletta egyidejű bevételét jelenti. . Nem szükséges semmilyen fogamzásgátló módszer alkalmazása , feltéve, hogy az első elfelejtett tablettát megelőző 7 napban a tablettákat helyesen vették be; ha azonban nem, vagy ha egynél több elfelejtett tabletta van, javasoljuk további óvintézkedések alkalmazását 7 napig.
Harmadik hét
Tekintettel a tablettamentes intervallum közelségére, a fogamzásgátlás csökkenésének kockázata nagyobb. A tabletták szedésének megváltoztatása azonban továbbra is megakadályozhatja a fogamzásgátló védelem csökkenését. Ezért nincs szükség további fogamzásgátló módszerek alkalmazására az alábbi két lehetőség egyikének alkalmazása esetén sem, amennyiben az összes tablettát helyesen vették be az első kihagyott tablettát megelőző 7 napban. Ellenkező esetben javasoljuk, hogy kövesse a két lehetőség közül az elsőt, és további óvintézkedéseket tegyen a következő 7 napban.
1. Az utolsó kihagyott tablettát azonnal vegye be, amint észreveszi az elfelejtett tablettát , még akkor is, ha ez két tabletta bevételét jelenti ugyanazon a napon. A következő tablettákat a szokásos időben kell bevenni. . A következő csomagot az előző csomag befejezése után azonnal el kell kezdeni, azaz a két csomag közötti tablettamentes intervallum betartása nélkül. Ebben az esetben nem valószínű, hogy a második csomag vége előtt elvonási vérzés következik be; azonban a tabletták, foltosodás vagy áttöréses vérzés léphet fel.
2. Azt is javasolhatják, hogy hagyja abba a tabletta szedését a jelenlegi csomagolásból, ezért tartsa be a legfeljebb 7 napos pirulamentes intervallumot, beleértve azokat is, amelyekben a tablettákat kihagyták, majd folytassa a tablettamentes időközökkel. új csomagolás.
Ha a tablettákat kihagyták, és az első rendszeres tablettamentes időszakban nem jelentkezik elvonási vérzés, mérlegelni kell a terhesség folytatódásának lehetőségét.
AJÁNLÁSOK HAJTÁS ÉS / VAGY FEJLESZTÉS ESETÉN
Ha hányás vagy hasmenés jelentkezik a tabletta bevételét követő 4 órán belül, akkor a tabletták felszívódása hiányos lehet. A fentiekben leírtak szerint új csomagolású tablettákat kell használni. Lásd az új csomagolás "Szabálytalan tablettabevitel" című fejezetében ismertetett ajánlásokat.
04.3 Ellenjavallatok
A kombinált orális fogamzásgátlók nem alkalmazhatók a következő esetekben:
• túlérzékenység a hatóanyagokkal vagy bármely segédanyaggal szemben
• artériás thromboemboliás balesetek vagy artériás thromboemboliás patológia a történelemben (különösen miokardiális infarktus, cerebrovascularis baleset)
• vénás tromboembóliás balesetek vagy vénás tromboembóliás megbetegedések (mélyvénás trombózis, tüdőembólia), kiváltó okokkal vagy anélkül
• a trombózis jelenlegi vagy korábbi prodroma (például átmeneti ischaemiás roham, angina pectoris)
• kardiovaszkuláris rendellenességek: magas vérnyomás, magas vérnyomás, hipertóniával vagy vesebetegséggel kapcsolatos betegségek, koszorúér -betegség, valvulopathia, ritmuszavarok, amelyek vérrögképződést okozhatnak
• örökletes vagy szerzett hajlam vénás vagy artériás trombózisra
• fejfájás fokális neurológiai tünetekkel, például aurával
• cukorbetegség, amelyet mikro- vagy makroangiopátia bonyolít
• érrendszeri eredetű szemészeti patológia
• súlyos májbetegség, akár jelenlegi, akár korábbi, amíg a májfunkciós értékek normalizálódnak
• jelenlegi vagy korábbi hasnyálmirigy -gyulladás, ha súlyos hipertrigliceridémiával jár
• máj- vagy jelenlegi májdaganatok, jóindulatúak vagy rosszindulatúak
• a nemi szervek (endometrium karcinóma) vagy az emlő, ha hormonfüggő, ismert vagy feltételezett malignus patológiái
• kolesztatikus sárgaság terhesség alatt vagy sárgaság a COC -k korábbi használatával összefüggésben
• ismeretlen hüvelyi vérzés
• ismert vagy feltételezett terhesség
• a ritonavirrel való kapcsolat.
A vénás vagy artériás trombózis egy vagy több kockázati tényezőjének jelenléte ellenjavallatot jelenthet a használathoz (lásd 4.4 pont). Ha ezen állapotok bármelyike először jelentkezik az orális fogamzásgátló alkalmazása során, a készítmény szedését le kell állítani azonnal.
04.4 Különleges figyelmeztetések és a használathoz szükséges óvintézkedések
ORVOSI VIZSGÁLAT
A COC-kezelés megkezdése vagy újbóli beadása előtt alapos személyes és családi kórtörténetet és fizikai fizikális vizsgálatot kell végezni (beleértve a vérnyomás meghatározását is), amint azt az "Ellenjavallatok" szakaszok (4.3. Pont) és a "Különleges figyelmeztetések" jelzik; A fizikális vizsgálatot legalább évente meg kell ismételni a COC -kezelés alatt, PAP -ot kell végezni, ha a betegnek szexuális tevékenysége van / volt, vagy másképpen jelezték. A rendszeres orvosi értékelés is fontos, mivel egyes ellenjavallatok (például átmeneti iszkémiás roham stb.) Vagy kockázati tényezők (például "vénás vagy artériás trombózis családtörténete") először jelenhetnek meg kombinált orális alkalmazásakor. fogamzásgátló. Ezen értékelések gyakoriságát és típusát egyedileg a betegre kell szabni, de általában különös figyelmet kell fordítani a vérnyomásra, a mellre, a májra, a végtagokra, a hasra és a medencére, beleértve a méhnyak citológiáját (PAP teszt) és a kapcsolódó laboratóriumi vizsgálatokat.
Az első utóvizsgálatot 3 hónappal a COC kezdete után kell megtenni. Az első látogatáskor szükséges és a fent leírt vizsgálatokat minden éves látogatáskor el kell végezni.
A nőket figyelmeztetni kell arra, hogy az orális fogamzásgátlók nem védenek a HIV -fertőzés (AIDS) vagy más nemi betegségek ellen.
KÜLÖN FIGYELMEZTETÉSEK
A dohányzás növeli a szív- és érrendszeri mellékhatások kockázatát a COC -k használatával. Ez a kockázat az életkor előrehaladtával és a füstölt cigaretták számával (15 vagy több cigaretta naponta) növekszik, és a nőknél hangsúlyosabb. 35 év felett A COC -t használó nőknek határozottan tanácsolni kell, hogy ne dohányozzanak.
A MINULET ezért laktózt tartalmaz Nem alkalmazható örökletes galaktóz intoleranciában, Lapp laktáz hiányban vagy glükóz / galaktóz felszívódási zavarban szenvedő betegeknél.
A MINULET szacharózt tartalmaz, és nem alkalmas örökletes fruktóz intoleranciában, glükóz / galaktóz malabszorpciós szindrómában vagy szacharáz-izomaltáz hiányban szenvedőknek.
TROMBOEMBOLICUS ZAVAROK ÉS EGYÉB Kardiovaszkuláris problémák
Szívroham
A szívinfarktus fokozott kockázatát társították a COC -k alkalmazásával. A kockázat elsősorban a dohányosoknál vagy a szívkoszorúér -betegség egyéb kockázati tényezőivel rendelkező nőknél, például magas vérnyomás, hypercholesterinaemia, morbid elhízás, cukorbetegség. A kockázat nagyon alacsony. 30 év alatti.
Artériás és vénás thromboemboliás betegség kockázata
A COC -k felírása előtt szisztematikus kutatást kell végezni az artériás és vénás thromboemboliás betegség kockázati tényezőinek jelenlétéről, és figyelembe kell venni az ellenjavallatokat és a használati óvintézkedéseket.
A terápiát abba kell hagyni, ha a közelgő szövődmények figyelmeztető tünetei jelentkeznek: szokatlanul erős fejfájás, látászavarok, emelkedett vérnyomás, phlebitis és tüdőembólia klinikai tünetei.
Az ösztrogénnek és a progesztogénnek való expozíció lehető legnagyobb mértékű korlátozása a helyes terápiás gyakorlat elveivel összhangban történik. Bármely ösztrogén-progesztogén kombináció esetén az előírt adagolási rendnek olyannak kell lennie, amely a legalacsonyabb mennyiségű hatékony ösztrogént és progesztogént tartalmazza, alacsony kompatibilitással sikertelenség és a páciens egyéni igényei szerint Azok a nők, akik először használnak COC -t, 50 mg -nál kevesebb ösztrogént tartalmazó készítményeket kell felírniuk.
A vénás thromboembolia (VTE) kockázata
Bármely kombinált orális fogamzásgátló alkalmazása megnövekedett kockázattal jár a vénás trombotikus események és a tromboembóliás események, mint például a mélyvénás trombózis és a tüdőembólia, összehasonlítva a nem alkalmazással. A megnövekedett kockázat a használat első évében a legnagyobb a nőknél, akik először kezdenek el COC -t. Ez a megnövekedett kockázat azonban alacsonyabb, mint a terhességgel összefüggő trombotikus események és vénás thromboembolia kockázata, amely 100 000 terhesre számítva 60 esetben nő éves.A vénás thromboembolia az esetek 1-2% -ában halálos kimenetelű.
Epidemiológiai vizsgálatok kimutatták, hogy a vénás thromboembolia előfordulása az alacsony ösztrogén COC -k (COC) alkalmazóinál
Számos epidemiológiai vizsgálat kimutatta, hogy az etinilösztradiolt tartalmazó kombinált orális fogamzásgátlók - többnyire 30 mikrogramm dózisban - és egy progesztin, például gesztodén használóinak megnövekedett a trombotikus események és a vénás thromboembolia kockázata azokhoz a nőkhöz képest, akik kombinált orális fogamzásgátlót alkalmaznak. mcg etinilösztradiolt és a progesztint, a levonorgesztrelt.
Néhány további vizsgálat adatai azonban nem mutatták ezt a megnövekedett kockázatot.
Azoknál a termékeknél, amelyek 30 mikrogramm etinilösztradiolt és dezogesztrelt vagy gesztodent kombinációban tartalmaznak, összehasonlítva azokkal, amelyek kevesebb mint 50 mikrogramm etinilösztradiolt és levonorgesztrelt tartalmaznak, a vénás tromboembóliás események relatív kockázatát 1,5 és 2,0 között becsülték.A trombotikus események és a vénás thromboembolia előfordulási gyakorisága 50 mcg-nál kisebb levonorgesztrelt és etinilösztradiolt tartalmazó kombinált orális fogamzásgátlók esetén körülbelül 20 eset 100 000 nőévenként. 30 mcg etinil-ösztradiolt tartalmazó, dezogesztrelt vagy gesztodent L. tartalmazó készítmények esetén az incidencia körülbelül 30- 40 eset 100 000 nőévre, azaz 10-20 további eset 100 000 nőévre. Ez az adat összehasonlítható a nem használók 100 000 nőévre jutó 5-10 esetével. A relatív kockázat hatása a további esetek számára a legnagyobb lenne az első évben, amikor egy nő először használ kombinált orális fogamzásgátlót.
Mindezt az információt figyelembe kell venni a gyógyszer felírása során. A fogamzásgátló módszer (ek) kiválasztásának mérlegelésekor a fenti információkat mind figyelembe kell venni.
Rendkívül ritkán számoltak be más érrendszeri területek trombózisáról, pl. Máj-, mesenterikus, vese- vagy retina artéria vagy véna a COC -t szedő nőknél. Nincs egyetértés abban, hogy ezen események előfordulása összefüggésben áll a kombinált orális fogamzásgátlók alkalmazásával.
A vénás vagy artériás trombózis tünetei a következők lehetnek: fájdalom és / vagy duzzanat az egyik lábban; hirtelen súlyos fájdalom a mellkasban, függetlenül attól, hogy a bal karba sugárzik -e vagy sem; hirtelen légszomj; hirtelen kezdődő köhögés; szokatlan, súlyos, hosszan tartó fejfájás; hirtelen részleges vagy teljes látásvesztés; diplopia; homályos beszéd vagy afázia; szédülés; összeomlás fokális rohamokkal vagy anélkül; gyengeség vagy kifejezett zsibbadás, amely hirtelen érinti a test egyik oldalát vagy részét; motoros zavarok; akut has.
A tromboembólia (vénás és / vagy artériás) kockázata az alábbiakkal nő:
- életkor;
- dohányzási szokás;
- elhízás (testtömeg -index 30 kg / m2 felett);
- diszlipoproteinémia;
- magas vérnyomás;
- szívbillentyű -hiba;
- pitvarfibrilláció;
- hosszan tartó immobilizáció, nagy műtét, bármilyen lábműtét vagy súlyos trauma. Ilyen körülmények között ajánlott a kombinált orális fogamzásgátló szedését abbahagyni (elektív műtét esetén, amely növeli a trombózis kockázatát) legalább 4 héttel a műtét előtt, és legkorábban 2 héttel a teljes gyógyulás után folytatni.
- nemrégiben született szülés vagy a második trimeszterben történt abortusz: mivel a szülés utáni időszak a tromboembólia fokozott kockázatával jár, a szoptatás utáni időszakban legkorábban 28 nappal kell elkezdeni a COC-t olyan nőknél, akik nem szoptatnak, vagy a terhesség második trimeszterében .
Artériás trombózis és thromboembolia
A COC -k alkalmazása növeli az artériás trombotikus és thromboemboliás epizódok kockázatát.
A jelentett epizódok közé tartozik a szívinfarktus és az agyi érrendszeri események (ischaemiás és vérzéses stroke, átmeneti ischaemiás roham). A retina érrendszeri trombózisával kapcsolatos információkért lásd a "Szemkárosodások" részt.
A trombotikus és thromboemboliás artériás események kockázata tovább nő azokban a nőkben, akik mögöttes kockázati tényezőkkel rendelkeznek.
Óvatosan kell eljárni, amikor COC -t írnak fel olyan nőknek, akiknél trombotikus és thromboemboliás epizódok kockázati tényezői vannak.
• Nincs egyetértés a visszerek és a felszíni thrombophlebitis lehetséges szerepében a vénás thromboemboliában.
• Figyelembe kell venni a tromboembólia kockázatát a szülés utáni időszakban (információkért lásd 4.6 pont).
• A keringési rendellenességekkel összefüggő egyéb betegségek közé tartozik a diabetes mellitus, a szisztémás lupus erythematosus, a hemolitikus urémiás szindróma, a krónikus gyulladásos bélbetegség (Crohn -betegség és fekélyes vastagbélgyulladás) és a sarlósejtes vérszegénység.
A migrén gyakoriságának vagy súlyosságának növekedése egy kombinált kombinált orális fogamzásgátló alkalmazása során (ami a cerebrovaszkuláris esemény prodromális lehet) lehet az oka annak, hogy azonnal abba kell hagyni a COC szedését.
A biokémiai tényezők, amelyek örökletes vagy szerzett vénás vagy artériás trombózis hajlamra utalhatnak, a következők: aktivált fehérje C -rezisztencia, hiperhomociszteinémia, antitrombin III -hiány, fehérje C -hiány, fehérje S -hiány, antifoszfolipid antitest szindróma (antikardiolipin antitestek, lupus antikoaguláns).
A kockázat / haszon arány mérlegelésekor az orvosoknak szem előtt kell tartaniuk, hogy egy klinikai állapot megfelelő kezelése csökkentheti a kapcsolódó trombózis kockázatát, és hogy a terhességgel kapcsolatos kockázat magasabb, mint a COC -k alkalmazásával összefüggésben.
RÁKOK
A reproduktív szervek és az emlő karcinóma
A méhnyakrák legfontosabb kockázati tényezője a tartós humán papillomavírus fertőzés.
A méhnyakrák (méhnyak intraepithelialis neoplasia és invazív méhnyakrák) fokozott kockázatáról számoltak be néhány epidemiológiai vizsgálatban nőknél, akik hosszú távú COC-kezelést kaptak; azonban még mindig nincs egyetértés abban, hogy ez a megállapítás mennyiben tulajdonítható a szexuális viselkedés és más tényezők, például az emberi papilloma vírus (HPV) miatti zavaró hatásoknak.
Az emlőrák kialakulásában szerepet játszó kockázati tényezők közé tartozik a növekvő életkor, a családtörténet, az elhízás, a nulliparitás és az előrehaladott életkor az első teljes terhesség alatt.
54 epidemiológiai vizsgálat metaanalízise azt találta, hogy a jelenleg COC-t használó nőknél kissé megnövekszik az emlőrák relatív kockázata (RR = 1,24), és hogy a megnövekedett kockázat fokozatosan eltűnik a 10 éves időszak alatt. Mivel a mellrák ritka a 40 év alatti nők körében, a kombinált orális fogamzásgátlót szedő vagy nemrég szedő nőknél diagnosztizált emlőrákok száma alacsony az emlőrák kockázatához képest.
Nem diagnosztizált rendellenes genitális vérzés esetén megfelelő diagnosztikai intézkedések szükségesek.
Máj neoplasia
A COC -t szedő nőknél ritkán jelentettek jóindulatú májdaganatokat és még ritkábban rosszindulatú májdaganatokat. Izolált esetekben ezek a daganatok életveszélyes intraabdominális vérzést okoztak. Ha a kombinált orális fogamzásgátlót szedő nőnél erős felső hasi fájdalom, májnagyobbodás vagy hasi vérzésre utaló jelek alakulnak ki, a diagnózis felállításakor figyelembe kell venni a májrák lehetőségét.
MÁS FELTÉTELEK
Cerebrovascularis betegség
Bebizonyosodott, hogy a COC -k növelik a cerebrovascularis epizódok (trombotikus és vérzéses stroke) kockázatát. A kockázat nagyobb a 35 év feletti hipertóniás nők és a dohányosok körében.
Kimutatták, hogy a magas vérnyomás mind a fogamzásgátló, mind a nem fogamzásgátló nők kockázati tényezője mindkét típusú stroke esetében, míg a dohányzás növeli a vérzéses stroke kockázatát.
Máj funkció
A májműködés akut vagy krónikus zavarai miatt a COC -kezelés felfüggesztése szükségessé válhat, amíg a májfunkció markerei normalizálódnak.
Azok a nők, akiknek kórtörténetében COC-vel összefüggő epepangás van, vagy nők, akiknél epepangás alakul ki terhesség alatt, nagyobb valószínűséggel tapasztalják ezt az állapotot a COC-k alkalmazása során. Ezeket a COC-t szedő betegeket gondosan ellenőrizni kell, és ha a cholestasis kiújul, a kombinált orális fogamzásgátlót fel kell függeszteni.
A májműködés akut és krónikus zavarai miatt szükség lehet a COC -kezelés abbahagyására mindaddig, amíg a májfunkció normalizálódik.
Szem sérülések
Retina trombózis eseteiről számoltak be a COC -k alkalmazása során. Ha megmagyarázhatatlan részleges vagy teljes látásvesztés, proptosis vagy diplopia megjelenése, papilláris ödéma vagy a retina érrendszeri elváltozásai jelentkeznek, a COC alkalmazását abba kell hagyni, és azonnal kivizsgálják.
Migrénes fejfájás
A migrén megjelenése vagy súlyosbodása, vagy fejfájás kialakulása, amelynek jellegzetessége ismétlődő, tartós és súlyos, olyan helyzeteket jelent, amelyek megkövetelik a COC abbahagyását és az ok felmérését.
A COC -t szedő migrénes (különösen aurás migrénes) nőknél fokozott a stroke kockázata (lásd 4.3 pont).
Angioödéma
Az exogén ösztrogének kiválthatják vagy súlyosbíthatják az angioödéma tüneteit, különösen örökletes angioödémában szenvedő nőknél.
Hatások a lipid- és szénhidrát -anyagcserére
Glükóz intoleranciáról számoltak be COC -t alkalmazó betegeknél. Bár a COC -k befolyásolhatják a perifériás inzulinrezisztenciát és glükóztoleranciát, nincs bizonyíték arra, hogy kombinált orális fogamzásgátlót alkalmazó betegeknél szükség van az adagolás módosítására. A cukorbetegségben vagy glükóz intoleranciában szenvedő betegeket azonban gondosan ellenőrizni kell a COC szedése során (lásd 4.4 pont „Különleges figyelmeztetések és az alkalmazással kapcsolatos óvintézkedések”).
A nők kis százaléka tapasztal változást a lipidértékekben kombinált orális fogamzásgátló szedése során. Azoknál a nőknél, akiknek diszlipidémiája nem kontrollált, nem hormonális fogamzásgátló módszert kell figyelembe venni. fogamzásgátló. A megnövekedett plazma trigliceridszint a COC -használóknál hasnyálmirigy -gyulladáshoz és egyéb szövődményekhez vezethet.
Az ösztrogén növeli a nagy sűrűségű plazma lipoproteint (HDL-koleszterint), míg a HDL-koleszterin csökkenéséről számoltak be számos progesztogén esetében.
Egyes progesztogének növelhetik az alacsony sűrűségű lipoprotein (LDL) koncentrációt, és megnehezíthetik a hiperlipidémia szabályozását.
A kombinált orális fogamzásgátló hatása az ösztrogén és a progesztin dózisai közötti egyensúlytól, valamint a fogamzásgátlóban alkalmazott progesztogén jellegétől és teljes mennyiségétől függ. Az orális fogamzásgátló kiválasztásakor mindkét hormon tartalmát figyelembe kell venni . kombinálva.
A hiperlipidémia miatt kezelt nőket gondosan figyelemmel kell kísérni, ha COC -t választanak.
Folsavszint
A szérum folsav szintje csökkenthető kombinált orális fogamzásgátló kezeléssel. Ennek klinikai jelentősége lehet, ha a nő nem sokkal a COC abbahagyása után teherbe esik.
Folyadékvisszatartás
A COC -t óvatosan kell előírni olyan nőknek, akiknek egészségi állapotát súlyosbíthatja a folyadékvisszatartás.
Vérnyomás
Az orális fogamzásgátlók alkalmazása ellenjavallt magas vérnyomásban, magas vérnyomásban vagy vesebetegségben szenvedő vagy magas vérnyomásban szenvedő nőknél (lásd 4.3 pont).
Bár sok COC -t szedő nőnél kismértékű vérnyomásemelkedésről számoltak be, klinikailag jelentős vérnyomás -emelkedés ritkán fordul elő. A COC -használat és a magas vérnyomás közötti összefüggést nem állapították meg. Azonban, ha klinikailag jelentős magas vérnyomás jelentkezik a COC alkalmazása során, az orvosnak elővigyázatosságból abba kell hagynia a COC szedését, és kezelnie kell a hypertoniát.
A bél patológiái
Crohn -betegségről és fekélyes vastagbélgyulladásról számoltak be kombinált orális fogamzásgátlók alkalmazásával kapcsolatban.
Az érzelmi szféra zavarai
Azoknál a nőknél, akiknél jelentős mentális depresszió uralkodik a COC szedése közben, fel kell függeszteniük a kezelést, és alternatív fogamzásgátló módszert kell alkalmazniuk annak megállapítására, hogy ez a tünet gyógyszerhez köthető-e. A depresszióban szenvedő és orális fogamzásgátlót szedő nőket gondosan ellenőrizni kell, és a kezelést le kell állítani, ha súlyos depresszió lép fel.
Szabálytalan vérzés
Rendellenes vérzés (pecsételő vagy intermenstruációs vérzés) fordulhat elő bármilyen COC szedése közben, különösen a kezelés első hónapjaiban. Ezért az esetleges szabálytalan hüvelyi vérzések értékelése csak a körülbelül 3 kezelési ciklusos rendeződési fázis után van értelme.
Ha a rendszertelen vérzés továbbra is fennáll, vagy a korábban rendszeres ciklusok után következik be, akkor nem hormonális etiológiát kell mérlegelni, és megfelelő diagnosztikai intézkedéseket kell alkalmazni, beleértve a curettage-t, hogy kizárják a rosszindulatú betegséget vagy a terhességet.
Néhány nőnél a tablettamentes időszak alatt nem fordulhat elő elvonási vérzés. Ha a COC-t a 4.2 pontban leírtak szerint vették be, nem valószínű, hogy terhes. , a terhességet ki kell zárni, mielőtt folytatni kell a COC szedését.
Chloasma időnként előfordulhat COC -k szedése közben, különösen olyan nőknél, akiknek kórelőzményében chloasma gravidarum szerepel; a chloasma -hajlamos betegeknek kerülniük kell a napsugárzást vagy az ultraibolya sugárzást.
Az alább felsorolt állapotok kialakulásáról vagy súlyosbodásáról mind a terhesség alatt, mind a COC -k szedése során beszámoltak; azonban nincs meggyőző bizonyíték ezen állapotok és a COC -k közötti összefüggésre: sárgaság és / vagy viszketés kolesztázisból, epekőképződés, porfíria, szisztémás lupus erythematosus, ureemiás-hemolitikus szindróma, Sydenham-féle chorea, herpes gestationis, halláskárosodás otosclerosis miatt.
Gyermekgyógyászati felhasználás
A COC -k biztonságosságát és hatékonyságát reproduktív korú nőknél állapították meg, ezeknek a gyógyszereknek a menarche előtti alkalmazása ellenjavallt.
Geriatriai használat
A COC -k nem javallottak a posztmenopauzás nőknél.
A HATÉKONYSÁG CSÖKKENTÉSE VAGY VESZTÉSE
A fogamzásgátlók hatékonysága csökkenhet, ha elfelejtette bevenni a tablettákat (lásd 4.2 pont „Szabálytalan tabletta szedése”), hányás és / vagy hasmenés esetén (lásd 4.2. más gyógyszereket egyidejűleg (lásd 4.5 pont).
A Hypericum perforatum készítményeket nem szabad egyidejűleg orális fogamzásgátlókat, digoxint, teofillint, karbamazepint, fenobarbitált, fenitoint tartalmazó gyógyszerekkel együtt szedni, mivel csökkenhet az orális fogamzásgátlók, digoxin, teofillin, karbamazepin, fenobarbitál, fenitoin ( lásd 4.5 pont.
04.5 Kölcsönhatások más gyógyszerekkel és más interakciók
Kölcsönhatások
Más gyógyszerekkel való kölcsönhatás, amely a nemi hormonok megnövekedett clearance -ét eredményezi, intermenstruációs vérzéshez vezethet, vagy csökkentheti az orális fogamzásgátló hatékonyságát.
Anyagok, amelyek csökkenthetik az etinilösztradiol szérumkoncentrációját:
Ellenjavallt egyesületek
Ritonavir: a csökkent fogamzásgátló hatás kockázata az ösztrogén plazmaszintjének csökkenése miatt.
Egyesületek nem ajánlottak
Enziminduktorok: görcsoldók (fenobarbitál, fenitoin, primidon, karbamazepin), rifabutin, rifampicin, griseofulvin, dexametazon, topiramát, fenilbutazon: a kezelés során és a kezelés felfüggesztését követő ciklusban a fogamzásgátló hatás csökkenésének kockázata.
Modafinil: a fogamzásgátló hatás csökkenésének kockázata a kezelés alatt és a kezelés abbahagyását követő ciklusban.
Néhány proteázgátló és valószínűleg oxikarbamazepin, felbamát és nevirapin is.
Hypericum perforatum (orbáncfű), valószínűleg májmikroszomális enzimek indukciójával.
Értékelni kívánt egyesületek
Néhány antibiotikum (például ampicillin, tetraciklin): a fogamzásgátló hatás csökkenésének kockázata az ösztrogének enterohepatikus keringésének csökkenése miatt.
Anyagok, amelyek növelhetik az etinilösztradiol szérumkoncentrációját:
- atorvasztatin
- a gasztrointesztinális fal szulfatációjának versenyképes gátlói, például aszkorbinsav (C -vitamin) és paracetamol (acetaminofen)
- a citokróm P450 3A4 izoenzimeket gátló anyagok, mint például az indinavir, flukonazol, vorikonazol és troleandomicin.
A troleandomicin növelheti az intrahepatikus cholestasis kockázatát a COC-k egyidejű alkalmazásakor.
Az etinil-ösztradiol befolyásolhatja más gyógyszerek metabolizmusát a máj mikroszómális enzimeinek gátlásával vagy a máj gyógyszerkonjugációjának, különösen a glükuronokonjugáció vagy más mechanizmusok kiváltásával.
Következésképpen a plazma- és szövetkoncentrációk növekedhetnek (pl. Ciklosporin, teofillin, kortikoszteroidok) vagy csökkenhetnek (pl. Lamotrigin, levotiroxin és valproát).
Azok a nők, akiket rövid ideig kezelnek egy vagy több, az említett osztályokba tartozó gyógyszerrel, a kombinált orális fogamzásgátló mellett ideiglenesen gátló módszert kell alkalmazniuk a gyógyszer egyidejű szedésének teljes időtartama alatt és az azt követő 7 napon a kezelés abbahagyása. A rifampicin -kezelés és a kombinált orális fogamzásgátló együttes alkalmazása esetén a rifampicin szedésének ideje alatt és a kezelés abbahagyása után 28 napig gátló módszert kell alkalmazni. Ha az egyidejű gyógyszer beadása a COC-csomag befejezése után is folytatódik, akkor a következő COC-csomagot a szokásos tablettamentes időköz betartása nélkül kell elkezdeni.
Májenzim-induktorokkal történő hosszú távú kezelés esetén ajánlott a fogamzásgátló szteroidok adagjának növelése. Ha az orális fogamzásgátló nagy adagja nem javallott, vagy nem kielégítőnek vagy megbízhatatlannak tűnik, például szabálytalan menstruáció esetén, akkor javasolni kell egy másik fogamzásgátló módszer alkalmazását.
Flunarizin: a galactorrhea kockázata a mellszövet prolaktin iránti fokozott érzékenysége miatt, a flunarizin hatása miatt.
A Hypericum perforatum készítményeket nem szabad orális fogamzásgátlókkal egyidejűleg alkalmazni, mivel ez a fogamzásgátlás hatékonyságának elvesztéséhez vezethet. Nemkívánatos terhességről és a menstruációs ciklus újbóli megjelenéséről számoltak be. Ennek oka a gyógyszerek metabolizmusáért felelős enzimek indukciója. Hypericum perforatum alapú készítmények. Az indukciós hatás a Hypericum perforatum termékekkel történő kezelés abbahagyása után legalább 2 hétig fennmaradhat.
LABORATÓRIUMI VIZSGÁLATOK
A fogamzásgátló szteroidok alkalmazása befolyásolhatja egyes laboratóriumi vizsgálatok eredményeit, beleértve a májfunkciós vizsgálatokat (a bilirubin és az alkalikus foszfatáz csökkenése), a pajzsmirigyet (a teljes T3 és T4 növekedés a TBG növekedése miatt, a szabad T3 gyanta felszívódásának csökkenése), a mellékvesét ( megnövekedett plazma kortizol, megnövekedett kortizol-kötő globulin, csökkent dehidroepiandroszteron-szulfát) és vese (fokozott plazma kreatinin- és kreatinin-clearance), plazmafehérje-transzportszintek, például kortikoszteroid-kötő globulin és lipid / lipoprotein frakciók, glükóz anyagcsere, koaguláció és fibrinolízis , a szérum folsavszint csökkenése. A változások általában a normál laboratóriumi értékek tartományán belül vannak.
04.6 Terhesség és szoptatás
Terhesség
A termék nem javallt terhesség alatt.
A dietil -sztilbestroltól eltérően a jelenlegi klinikai adatok és számos epidemiológiai vizsgálat eredményei lehetővé teszik számunkra, hogy a terhesség kezdetén, önmagában vagy kombinációban alkalmazott ösztrogén adagolásával összefüggő malformációk kockázatát csökkentsük.
Ezenkívül a magzat (különösen a nőstény) nemi differenciálódásával kapcsolatos kockázatokat, amelyeket az első erősen androgénomimetikus progesztogénekkel leírtak, nem lehet extrapolálni az újabb progesztogénekre (például a gyógyszerkészítményben használtra). jelentősen kevesebb, vagy egyáltalán nem, androgénomimetikumok.
Következésképpen az "ösztrogén-progesztogén kombinációt" szedő betegnél a terhesség felfedezése nem indokolja az abortuszt.
Ha terhesség következik be a COC alkalmazása során, a kezelést abba kell hagyni. Nincs meggyőző bizonyíték arra vonatkozóan, hogy a COC -ben lévő ösztrogének és progesztogének károsíthatják a magzatot, ha a fogamzásgátlás véletlenül következik be a COC kombinált alkalmazása során (lásd 4.3 pont „Ellenjavallatok”).
Etetési idő
A szoptatást befolyásolhatják a COC -k, mivel csökkenthetik az anyatej mennyiségét és megváltoztathatják az anyatej összetételét. Ezért a szoptatás végéig nem szabad használni a COC -ket. Kis mennyiségű szteroid, fogamzásgátló és / vagy metabolitjai kiválasztódhatnak tej, de nincs bizonyíték arra, hogy ez káros hatással lenne a baba egészségére.
04.7 Hatások a gépjárművezetéshez és gépek kezeléséhez szükséges képességekre
A MINULET -et nem vizsgálták a gépjárművezetéshez és gépek kezeléséhez szükséges képességekre gyakorolt hatása miatt.
04.8 Nemkívánatos hatások
A kombinált orális fogamzásgátlót alkalmazó nők esetében fokozott a vénás thromboembolia (VTE) kockázata. A COC -k trombotikus kockázatának különbségeivel kapcsolatos információkért lásd a 4.4 pontot.
A következő mellékhatásokat jelentették COC -t szedő nőknél:
Viszonylag ritka szövődmények, amelyek azonban a kezelés abbahagyását teszik szükségessé:
- artériás thromboemboliás balesetek (különösen miokardiális infarktus, cerebrovascularis baleset, átmeneti ischaemiás roham);
- vénás thromboemboliás balesetek (phlebitis, tüdőembólia);
- magas vérnyomás, koszorúér -betegség;
- hiperlipidémia (hipertrigliceridémia és / vagy hiperkoleszterinémia)
- súlyos mastodynia, jóindulatú mastopathia;
- intenzív és szokatlan fejfájás, migrén, szédülés, látásváltozások;
- az epilepszia súlyosbodása;
- májsejtes karcinóma, kolesztatikus sárgaság;
- chloasma;
- látóideggyulladás, a retina vaszkuláris trombózisa.
Gyakrabban előforduló szövődmények, amelyek általában nem igénylik a kezelés abbahagyását, de amelyek esetében alternatív orális fogamzásgátló kombináció alkalmazása jöhet szóba:
- hányinger, enyhe fejfájás, súlyváltozások (növekedés vagy csökkenés), ingerlékenység, idegesség, nehézség a lábakban;
- mellérzékenység, tapintási érzékenység, térfogatnövekedés, váladék;
- intermenstruációs vérzés, a hüvelyváladék megváltozása, oligomenorrhea, amenorrhoea, dysmenorrhoea, a libidó megváltozása;
- szemirritáció kontaktlencsék használatával.
Ritkán:
- bőrbetegségek (alopecia, akne, seborrhea, hypertrichosis, kiütés, nodosus erythema, erythema multiforme)
- depressziós hangulat
- hányás és hasi görcsök
- túlérzékenységi reakciók, beleértve nagyon ritka csalánkiütéses eseteket, angioödémát és súlyos légzési és keringési tünetekkel járó reakciókat. A szisztémás lupus erythematosus súlyosbodása.
- a visszerek súlyosbodása.
- puffadás érzése.
- glükózintolerancia és a porfíria súlyosbodása
- hasnyálmirigy -gyulladás
- ischaemiás colitis
- epeúti lithiasis
- gyulladásos bélbetegség (Crohn -betegség, fekélyes vastagbélgyulladás)
- a szérum folsavszint csökkenése.
Egyéb gyakran előforduló mellékhatások:
- folyadékretenció / ödéma, étvágyváltozások (növekedés vagy csökkenés), hüvelygyulladás, candidiasis
A COC -k használatát a következők fokozott kockázatával hozták összefüggésbe:
- artériás és vénás trombotikus események és thromboemboliás események, beleértve a miokardiális infarktust, a stroke -ot, az átmeneti ischaemiás rohamot, a vénás trombózist és a tüdőembóliát
- méhnyak intraepithelialis neoplasia és méhnyakrák
- mellrák diagnosztizálása.
- jóindulatú májdaganatok (pl. fokális nodularis hyperplasia, máj adenoma).
A COC-k súlyosbíthatják a már meglévő epehólyag-betegséget, és felgyorsíthatják e betegség kialakulását korábban tünetmentes nőknél.
Hatások a kezelés abbahagyására: kezelés utáni amenorrhoea.
A kezelés abbahagyásakor ovuláció nélküli amenorrhoea figyelhető meg (gyakrabban fordul elő olyan nőknél, akiknél korábbi cikluszavarok fordultak elő). Ez általában spontán megoldódik. Ha ez továbbra is fennáll, minden további felírást megelőzően tanácsos megvizsgálni az agyalapi mirigy -rendellenességek lehetőségét.
04.9 Túladagolás
A COC túladagolás tünetei felnőtteknél és gyermekeknél: hányinger, mellérzékenység, zavartság, hasi fájdalom, álmosság / fáradtság, elvonási vérzés.
Nincsenek specifikus ellenszerek, és minden további kezelésnek tüneti jellegűnek kell lennie.
05.0 FARMAKOLÓGIAI TULAJDONSÁGOK
05.1 Farmakodinámiás tulajdonságok
Farmakoterápiás csoport: szisztémás hormonális fogamzásgátlók; fix ösztrogén-progesztogén társulások.
ATC kód: G03AA10
A COC -k a gonadotropinok elnyomásával működnek. Bár ennek a hatásnak az elsődleges mechanizmusa az ovuláció gátlása, egyéb változások közé tartozik a méhnyak nyálkahártyájának megváltozása (ami növeli a spermiumok méhbe jutásának nehézségét) és az endometrium változása (ami csökkenti a "növény" valószínűségét).
Ha a COC -ket következetesen és helyesen veszik, a valószínű meghibásodási arány 0,1%; a szokásos gyakorlatban azonban minden orális fogamzásgátló sikertelensége 5%. A legtöbb fogamzásgátló módszer hatékonysága a helyes használattól függ.A módszer kudarca nagyobb valószínűséggel fordul elő, ha elfelejtik a kombinált orális fogamzásgátló tablettákat.
A COC-k alkalmazásával kapcsolatos, nem fogamzásgátló előnyöket epidemiológiai vizsgálatok támasztják alá, amelyek széles körben alkalmaztak olyan készítményeket, amelyek 35 μg-nál nagyobb dózisú etinilösztradiolt vagy 50 μg mestranolt tartalmaznak.
HATÁSOK A MENSTRUÁLIS CIKLUSRA
A menstruációs ciklus rendszerességének javítása.
A vérveszteség csökkentése és a vashiányos vérszegénység előfordulásának csökkentése.
A dysmenorrhoea előfordulásának csökkenése.
Az ovuláció "gátlásával" kapcsolatos hatások
A funkcionális petefészekciszták előfordulásának csökkenése.
A méhen kívüli terhességek előfordulásának csökkenése.
EGYÉB HATÁSOK
A fibroadenomák és a fibrocisztás emlőbetegségek előfordulásának csökkenése.
Az akut kismedencei gyulladásos megbetegedések előfordulásának csökkenése.
Az endometrium rák előfordulásának csökkenése.
A petefészekrák előfordulásának csökkenése.
Az akne súlyossága csökkent.
05.2 Farmakokinetikai tulajdonságok
A gesztodén teljesen és gyorsan felszívódik az emésztőrendszerben. A maximális vérszintet körülbelül egy óra elteltével éri el. Nincs kitéve erős "first pass" hatásnak; felezési ideje a terminális fázisban meglehetősen rövid és alacsonyabb, mint a levonorgesztrelé. Az elimináció főként a vesén keresztül történik felezési ideje körülbelül 24 óra. Az egyszeri beadást követő 7 napon belül a vizelet vagy a széklet eliminációja gyakorlatilag befejeződött.
"Az etinil-ösztradiol gyorsan és teljesen felszívódik az emésztőrendszerben; a vércsúcs körülbelül 1 óra múlva érhető el. A vérszint viszonylag gyorsan csökken az első fázisban, és lassabban a második fázisban (felezési idő 26 óra). L" 40% az elimináció a vizeletben, 60% -a a székletben történik.
05.3 A preklinikai biztonságossági adatok
Toxicitás
A két komponens akut toxicitása alacsony:
Hasonlóképpen, a két szteroid kombinációjának toxicitása alacsony: 1: 0,60, 1: 0,57 és 1: 0,30 arányban az akut toxicitás egereknél és patkányoknál mindig> 4 g / kg volt, os.
A két hatóanyag kapcsolatának krónikus toxicitási vizsgálata patkányokon (26-27 hét) és kutyákon (27-28 hét) nem mutatott szervtoxikus hatást még nagyobb dózisok esetén sem. és az emlőben és az endometriumban bekövetkező változások) a legmagasabb dózisok (4,75 mg / kg progesztin és 47,5 mg / kg ösztrogén) esetén az összetevők farmakodinamikai hatásával kapcsolatosak.
A patkányokon végzett vizsgálatok egyértelműen befolyásolták a termékenységet a szuppresszióig, az alkalmazott ösztrogén-progesztin dózisokhoz képest.
Megfelelő vizsgálatok kimutatták, hogy nincs teratogén, embriotoxikus hatás és peri- vagy postnatális toxicitás.
A mutagenitási tesztek negatívak voltak, és 24 hónapig egereken és patkányokon végzett karcinogenitási tesztek hasonló eredményeket adtak, mint a hasonló vegyületeknél.
06.0 GYÓGYSZERÉSZETI INFORMÁCIÓK
06.1 Segédanyagok
Laktóz; kukoricakeményítő; povidon 25.000; nátrium -kalcium -edetát; magnézium -sztearát, szacharóz; povidon 700 000; makrogol 6000; Kálcium-karbonát; talkum; a montánsav etilénglikol -észtere (E viasz).
06.2 Inkompatibilitás
Nincs ismert összeférhetetlenség
06.3 Érvényességi idő
3 év.
06.4 Különleges tárolási előírások
Legfeljebb 25 ° C -on tárolandó.
06.5 A közvetlen csomagolás jellege és a csomag tartalma
PVC buborékcsomagolás 21 bevont tablettával.
06.6 Használati utasítás
Lásd szekta. 4.2.
07.0 FORGALOMBA HOZATALI ENGEDÉLY
Pfizer Italia S.r.l., Via Isonzo, 71 - 04100 Latina
08.0 A FORGALOMBA HOZATALI ENGEDÉLY SZÁMA
A.I.C. n. 026286029
09.0 Az első forgalomba hozatali engedély engedélyezésének vagy megújításának dátuma
1988. október 24. és 2010. május 31.
10.0 A SZÖVEG FELÜLVIZSGÁLÁSÁNAK DÁTUMA
26/02/2013
11.0 RÁDIÓGYÓGYÁK, TELJES ADATOK A BELSŐ RADIÁCIÓS DOSIMETRIARÓL
12.0 RÁDIÓGYÓGYÁSZATOKHOZ, KIEGÉSZÍTŐ RÉSZLETES UTASÍTÁSOK A KIVÉTELES ELŐKÉSZÍTÉSRE ÉS A MINŐSÉG -ELLENŐRZÉSRE
ELLENŐRZŐK ELLENŐRZÉSI LISTA - KOMBINÁLT HORMONÁLIS SZERZŐDÉSEK
Kérjük, használja ezt az ellenőrzőlistát a készítmény alkalmazási előírásával együtt a kombinált hormonális fogamzásgátlókkal (COC) kapcsolatos konzultációk során.
• Az thromboembolia (pl. mélyvénás trombózis, tüdőembólia, szívroham és stroke) fontos kockázatot jelent a COC -k alkalmazásával kapcsolatban.
• A thromboembolia kockázata magasabb CHC -vel:
- közben első év d "foglalkoztatás;
- amikor elmegy használat folytatása 4 vagy több hetes bevétel szünet után.
• Etinilösztradiolt tartalmazó COC -k levonorgesztrel, norgesztimát vagy noretiszteron megvan a alacsonyabb kockázat vénás tromboembóliát (VTE) okozhat.
• A nők kockázata a tromboembólia kiindulási kockázatától is függ. A COC használatára vonatkozó döntésnél ezért figyelembe kell venni a ellenjavallatok és egyéni kockázati tényezők, különösen a thromboemboliával kapcsolatosakat - lásd az alábbi mezőket és a vonatkozó alkalmazási előírást.
• Bármilyen kombinált kombinált gyógyszer alkalmazásáról, és nem a legalacsonyabb vénás thromboembolia (VTE) kockázatú gyógyszerről, csak a nővel folytatott interjú után szabad dönteni, hogy megértse:
- az kockázat a COC -hez kapcsolódó thromboembolia;
- a hatása bármilyen kockázati tényező a trombózis kockázatának velejárója;
- amire különös figyelmet kell fordítani jelek és tünetek trombózis esetén.
Ne feledje, hogy egy nő kockázati tényezői idővel változhatnak. Ezért fontos, hogy ezt az ellenőrző listát minden konzultáció alkalmával használja.
• műtétre van szüksége;
• Szükséges, hogy hosszabb ideig tartó immobilizáción menjen keresztül (például baleset vagy betegség esetén, vagy „alsó végtagba öntés esetén”).
→ Ezekben az esetekben jobb lenne átgondolni, hogy használjon-e nem hormonális fogamzásgátlót, amíg a kockázat normalizálódik..
• Utazás hosszabb ideig (> 4 óra);
• A kombinált fogamzásgátlók bármely ellenjavallatának vagy kockázati tényezőjének kidolgozása;
• Az elmúlt hetekben szült.
→ Ilyen esetekben a betegnek különös figyelmet kell fordítania a thromboembolia jeleinek és tüneteinek észlelésére.
Kérjük, bátorítsa a nőket, hogy olvassák el az egyes COC -csomagokat kísérő betegtájékoztatót, beleértve a trombózis tüneteit, amelyekre gondosan figyelniük kell.
Kérjük, jelentse a COC -től származó feltételezett mellékhatásokat a területileg illetékes farmakovigilanciai hivataloknak vagy az AIFA -nak, a hatályos jogszabályok előírásainak megfelelően
FONTOS INFORMÁCIÓK A KOMBINÁLT SZÓBELI SZERZŐDÉSEKRŐL (COCS) ÉS A VÉRRÖGZÉSEK KOCKÁZATÁRÓL
Minden kombinált fogamzásgátló növeli a vérrögképződés kockázatát. A kombinált hormonális fogamzásgátló (COC) szedése miatt a vérrögök általános kockázata kicsi., de a vérrögök súlyos állapotot jelenthetnek, és nagyon ritka esetekben akár halálos is lehet.
Nagyon fontos, hogy felismerje, mikor lehet nagyobb a vérrögképződés kockázata, milyen jelekre és tünetekre kell figyelni, és milyen intézkedéseket kell tennie.
Milyen esetekben nagyobb a vérrögképződés kockázata?
- a COC használatának első évében (beleértve a 4 vagy több hetes időközönként történő használat folytatását is)
- ha túlsúlyos
- ha Ön 35 évesnél idősebb
- ha olyan családtagja van, akinek viszonylag fiatalon (azaz 50 év alatt) vérrögöt észleltek
- ha az elmúlt hetekben szült
Maga dohányzik 35 év felett pedig erősen ajánlott a dohányzás abbahagyása vagy nem hormonális fogamzásgátló módszer alkalmazása.
Azonnal forduljon orvoshoz, ha az alábbi tünetek bármelyikét észleli:
• Erős fájdalom vagy duzzanat az egyik lábban amely pelyhesedéssel, melegséggel vagy a bőr színének megváltozásával járhat, például sápadtság, vörösség vagy kékes szín megjelenése. Mélyvénás trombózisa lehet.
• A hirtelen és megmagyarázhatatlan légszomj vagy gyors légzés; súlyos mellkasi fájdalom, amely mély légzéssel fokozódhat; hirtelen köhögés nyilvánvaló ok nélkül (ami vért termelhet). Ez a tüdőembólia nevű mélyvénás trombózis súlyos szövődménye lehet. Ez akkor fordul elő, ha a vérrög a lábból a tüdőbe vándorol.
• Fájdalom a mellkasban, gyakran éles, de néha előfordul mint a rossz közérzet, a nyomásérzet, a súly, a felsőtest kényelmetlensége, amely a hátba, az állkapocsba, a torokba, a karba sugároz, emésztési zavarokkal vagy fulladással, izzadással, hányingerrel, hányással vagy szédüléssel járó teltségérzettel. Szívroham lehet.
• Zsibbadás vagy gyengeségérzet az arcon, a karon vagy a lábon, különösen a test egyik oldalán; a beszéd vagy a megértés nehézsége; "hirtelen zavartság, hirtelen látásvesztés vagy homályos látás; fejfájás / migrén intenzív és a szokásosnál rosszabb. Ez lehet stroke."
Vigyázzon a vérrög tüneteire, különösen, ha:
• most műtötték
• hosszú ideig mozgásképtelen volt (például baleset vagy betegség miatt, vagy mert gipszben volt a lába)
• hosszú utat tett meg (több mint 4 órán keresztül)
Ne felejtse el elmondani orvosának, ápolójának vagy sebészének, hogy kombinált hormonális fogamzásgátlót szed, ha:
• Ön műtéten esett át vagy esedékes
• Van olyan helyzet, amikor egy egészségügyi szakember megkérdezi Önt, hogy milyen gyógyszereket szed
További információkért kérjük, olvassa el figyelmesen a gyógyszerhez mellékelt betegtájékoztatót, és haladéktalanul tájékoztassa kezelőorvosát vagy gyógyszerészét a kombinált hormonális fogamzásgátló alkalmazásával kapcsolatos nemkívánatos hatásokról.