Általánosság
A krónikus myeloid leukémia (CML) kezelése számos terápiás lehetőséget tartalmaz, amelyek hosszú ideig képesek kordában tartani a betegséget. A rutin vér- és csontvelővizsgálatok, valamint a hematológus vagy onkológus gyakori értékelése nyomon követheti a rák előrehaladását.

Az orvosi vizsgálatok (vérkép, citogenetikai és molekuláris vizsgálatok) eredményei alapján megérthető:
- A kezelés hatékonyságának időbeli foka és a terápiára adott válasz alakulása;
- Ha a betegség már nem reagál a gyógyszerekre (terápiával szembeni rezisztencia).
A terápia monitorozása és reagálása
A betegség lefolyásának helyes monitorozása elengedhetetlen a terápia hatékonyságának ellenőrzéséhez, következésképpen ahhoz, hogy a kezelés sikertelensége esetén azonnal beavatkozhassunk.
Citogenetikai elemzést és molekuláris biológiai vizsgálatokat használnak, valamint diagnosztikai célokra is, hogy felmérjék a terápiás protokollra adott válasz mértékét, és kiemeljék a kezelés utáni betegség fennmaradását (a minimális maradványbetegség vizsgálata):
- Teljes hematológiai válasz: Amikor a terápia hatni kezd, a leukémiás sejtek száma csökken. A hematológiai tesztek már nem képesek aberráns klónok kimutatására, de ez citogenetikai elemzéssel lehetséges.
- Teljes citogenetikai válasz: akkor kapható, amikor a Philadelphia kromoszóma (Ph) jelenlétét már nem emeli ki hagyományos citogenetikai elemzés (standard módszer a kezelésre adott válasz nyomon követésére) vagy fluoreszcens in situ hibridizáció (FISH), amely a százalékos arányt értékeli. Ph + csontvelő sejtek. A finom tűvel elszívott csontvelőmintán végzett citogenetikai elemzés az egyetlen módszer annak meghatározására, hogy a Philadelphia kromoszómán kívül milyen prognosztikai szereppel bíró kromoszóma-elváltozások vannak jelen.
- Teljes molekuláris válasz: akkor érhető el, ha a molekuláris elemzés nem képes kimutatni a BCR / ABL hibrid gén expresszióját. A terápia hatékonynak bizonyult, és a bcr-abl fehérjék termelődését elősegítő molekuláris jelek olyan alacsonyak, hogy még nagyon érzékeny tesztekkel, például molekulárisakkal sem észlelhetők. A megfigyelt megnövekedett átirat -szintek jelezhetik a kezelésre adott válasz elvesztését.
Ezen eredmények elérése nagyon fontos eredmény: sok tanulmány azt mutatja, hogy a teljes citogenetikai és molekuláris válaszreakcióval rendelkező betegek nagyon nagy valószínűséggel képesek túlélni hosszú ideig, anélkül, hogy a betegség előrehaladna a gyorsított és / vagy robbanási fázisba. .
Számos tényező befolyásolhatja a terápia hatékonyságát, és ezért a kezdeti szakaszokban ajánlott a vizsgálatokat 3, 6, 12 és 18 hónap elteltével folytatni.
A klinikai vizsgálatokból eddig megszerzett információk, amelyek meghatározzák az optimális választ és a kudarcot a terápia különböző időszakaiban, nyomon követési rendszer kidolgozásához vezettek, amelyet követni kell a beteg megfelelő kezelése érdekében (indikációk Európai leukémia-hálózat):
A hematológus (vagy onkológus) képes lesz kitűzni néhány célkitűzést és ellenőrizni a terápia hatékonyságát az adott klinikai esetben, mivel a betegek eltérő módon reagálnak a terápiára, és nem mindenki tudja elérni az optimális terápiás mérföldköveket a tervezett időn belül ...
Terápiás lehetőségek
A CML kezelésének fő célja "a teljes molekuláris remisszió elérése: a betegséget a kezelés kontrollálja (még ha nem is tűnik el teljesen), és a termelt kóros klónok száma kellően korlátozott ahhoz, hogy ne okozzon tüneteket. A legtöbb ember nem tudja teljesen megszabadulni a leukémiás sejtektől, a kezelés segíthet a betegség hosszú távú remissziójának elérésében.
A terápiás célok a következők lehetnek:
- Korlátozza a krónikus myeloid leukémia tüneteinek megnyilvánulását;
- A vérsejtszámhoz kapcsolódó normál paraméterek visszaállítása;
- Csökkentse a Philadelphia kromoszóma pozitív leukémia sejtek (Ph +) és a molekuláris jelek (BCR / ABL átiratok) számát;
- Cél a Philadelphia + kromoszómák eltűnése (teljes citogenetikai válasz).
Hagyományos antilasztikus gyógyszerek
Egyes antilasztikus gyógyszerek, mint pl buszulfán (alkilálás) és l "hidroxi -karbamid (a DNS -szintézis specifikus inhibitora), különösen a múltban, a citológiai redukció és a betegség krónikus fázisban történő kontrolljának elérésére. A hagyományos kezelés az életminőség javulását eredményezte, de nem tudta jelentősen megváltoztatni a betegség természetes előzményeit, vagy nem tudta megakadályozni a gyorsított / robbanási fázisba való előrehaladást.
Rekombináns interferon-alfa
A nyolcvanas évek elejétől a bevezetése interferonok megengedte, hogy a granulocita -arány csökkentésén és normalizálásán kívül megfigyeljék a citogenetikai és molekuláris tesztek negativizálását, ami a krónikus fázis hosszabb időtartamát idézi elő, és ennek következtében csökken a fejlődés a gyorsított és / vagy robbanási fázisban. Az alfa -interferon csökkentette a hagyományos CML -terápia szerepét: ez a gyógyszer a betegek 20-30% -ában képes teljes citogenetikai választ kiváltani, kifejezetten zavarja a proliferációs jelek transzlációját a Ph + sejtekben, és gátolja a sejtek szaporodását. Az alfa-interferon közvetett mechanizmussal is befolyásolja a leukémiás sejtek túlélését, csökkentve sejtadhéziójukat és felerősítve az immunrendszer sejtjeinek aktivitását.
A gyógyszer alkalmazásának korlátozását a nem elhanyagolható toxicitása adja. Az interferon mellékhatásai közé tartozik a fáradtság, a láz és a fogyás. Az elért eredmények javítása érdekében az interferont más citotoxikus szerekkel kombinálták.Csak az interferon és a citozin-arabinozid (ARA-C) asszociációja bizonyítottan jobb eredményeket nyújt, mint önmagában az interferon, de nyilvánvaló túlélési előny nélkül.
Allogén csontvelő -transzplantáció
A recipienssel kompatibilis egészséges donor őssejt -transzplantációja (allogén transzplantáció) évek óta a leggyakoribb terápiás javallat, és még ma is az egyetlen olyan kezelés, amely képes véglegesen felszámolni a daganatot.
Ez az eljárás, ha krónikus fázisban hajtják végre, az esetek körülbelül 50% -ában ötéves betegségmentes túlélést eredményezhet.
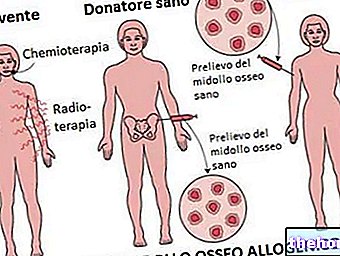
Az allogén csontvelő -transzplantáció magában foglalja az összes (vagy majdnem minden) Ph + -sejt elpusztításának első fázisát kondicionáló terápiával (kemoterápia a teljes test besugárzásával kombinálva), majd a vérképző csontvelő rekonstruálását az infúziós donor őssejtekkel. Ezenkívül a donor csontvelő limfociták hozzájárulnak a Ph + sejtek ellenőrzéséhez és / vagy megszüntetéséhez, immun-közvetített hatással, amelyet "graft versus leukemia" (graft versus leukemia) hatásnak neveznek. A terápiára adott válasz nyomon követhető annak felmérésével, hogy a krónikus myeloid leukémiára jellemző molekuláris elváltozások eltűntek -e vagy sem. Az allogén csontvelő -transzplantáció azt a terápiás kezelést jelenti, amely képes a CML "gyógyítására", de sajnos halálos toxicitás és / vagy visszaesés miatti kudarcot jelent. Ez az eljárás valójában nagyon igényes, és befolyásolható a kor beteg és a transzplantáció koraszülöttsége (a krónikus fázis diagnosztizálásától számított hónapok vagy évek): potenciális veszélye miatt csak 55 év alatti betegeknél kivitelezhető, további egyidejű patológiák nélkül. Ezért az allogén transzplantáció valódi terápiás lehetőséget jelent a CML -ben szenvedő betegek csak egy része számára (figyelembe véve a kompatibilis őssejt -donor megtalálásának nehézségeit is).
Újabban azokban a krónikus myeloid leukémiában szenvedő alanyokban, akik nem jogosultak allograftra (életkor, donorhiány, elutasítás stb.), Autotranszplantációt javasoltak. A páciens csontvelője, amelyet a Ph + sejtek szándékosan megfelelő citocid terápiája után (antilasztikus + interferonnal) újrafundáltak, a Ph-sejtek elterjedt újbóli expanziójával helyreállna.
Imatinib -mezilát (Glivec ®)
A krónikus myeloid leukémia kezelésének történetét forradalmasította az első tirozin -kináz inhibitor (Imatinib -mezilát) bevezetése, amely nagymértékben hozzájárult a betegek életminőségének javításához.
Az imatinib a BCR / ABL specifikus inhibitora, amelyet a betegség molekuláris biológiájának megértése után terveztek, és a Ph + krónikus myeloid leukémia kezelésében használnak.
A gyógyszer képes teljes molekuláris citogenetikai remissziót kiváltani a betegek 80-90% -ában, és aktív a mieloid neoplazmákban is eozinofíliával és PDGRF (vérlemezke-eredetű növekedési faktor, szérum mitogén, amely számos kóros állapotban részt vesz, ami elősegíti a kemotaxist és a proliferációt) kapacitás).
Az imatinib szelektíven blokkolja a BCR / ABL tirozin -kináz aktivitását az ATP gátló mechanizmusán keresztül: a gyógyszer megköti a BCR / ABL kináz specifikus doménjében rendelkezésre álló nagy energiájú molekulát (ATP), megakadályozva más szubsztrátok foszforilációját és blokkolja a kaszkádot a Ph + leukémiás klónok előállítási folyamatáért felelős reakciók. Ennek a molekulának (imatinib -metiszilát) alkalmazott dózisa a betegség fázisától és a választól függően 400 mg / nap és 800 mg / nap között változik. Jelenleg figyelemre méltó hatékonysága miatt a választott gyógyszer a CML kezelésére. A szuszpenzióval és / vagy az adag csökkentésével visszafordítható mellékhatások eltérőek lehetnek (fokozott transzaminázok, hányinger, bőrkiütések, folyadékvisszatartás stb.).
Megfigyeltek olyan eseteket, amelyek idővel rezisztenciát mutattak a gyógyszerrel szemben (például előrehaladott betegségben szenvedő betegek), és biológiai-klinikai kritériumokat határoztak meg a kezelésre adott válasz típusának meghatározására. Az ellenállásért felelős mechanizmusok többszörösnek tűnnek (a kináz domén mutációi, a BCR / ABL amplifikációja / túlzott expressziója, klonális evolúció ...). Ezekben az esetekben az imatinib -kezelés folytatása már nem megfelelő.
Az ilyen állapotú betegeknél a következő lehetőségek állnak rendelkezésre:
- Az allogén transzplantáció;
- Hagyományos terápia (hidroxi -karbamid, buszulfán stb.);
- L "interferon;
- Kísérleti terápia (2. generációs tirozin -kináz inhibitorokkal).
2. generációs tirozin -kináz inhibitorok
Az imatinib -kezelés sikertelensége a gyorsított és / vagy blasztos fázisú krónikus myeloid leukémia progressziójával jár, és különösen rossz prognózissal jár. Az elmúlt években a farmakológiai kutatások lehetővé tették, hogy a klinikai gyakorlatban olyan második generációs tirozin -kináz inhibitorokat alkalmazzanak, amelyek aktívak azoknál a betegeknél, akiknél rezisztencia alakult ki az imatinibdel szemben: krónikus fázisú betegeknél dazatinibot (Sprycel ®) és nilotinibet (Tasigna ®) alkalmaznak. és / vagy progresszív CML, amely nem reagál a Glivec ® -re, és képesek teljes és tartós hematológiai, citogenetikai és molekuláris válaszokat kiváltani. Számos tanulmány kimutatta azonban, hogy a Ph + klón - genetikai instabilitása miatt - mutációkat fejleszthet ki a BCR / ABL kináz domén, és ellenállónak bizonyulnak különböző gátló gyógyszerekkel szemben. A kísérleti fázisban lévő más molekulák (3. generációs inhibitorok) a krónikus myeloid leukémia specifikus célpontjaira irányulnak; különösen képesek specifikus mutációkkal érzékenyíteni a Ph + leukémiás sejteket (példa: Mk-0457 rezisztens CML és T315I mutáció esetén, amely közvetlenül befolyásolja t az imatinib kötőhelye).
További cikkek a "Krónikus mieloid leukémia terápia" témában
- Krónikus mieloid leukémia: Krónikus mieloid leukémia: diagnózis
- Krónikus mieloid leukémia: definíció, okok, tünetek