Hatóanyagok: Ropivakain (Ropivakain -hidroklorid)
Naropin 2 mg / ml, 7,5 mg / ml, 10 mg / ml oldatos injekció
Naropin 2 mg / ml oldatos infúzió
A Naropin csomagolólapok a következő csomagolási méretekhez kaphatók: - Naropin 2 mg / ml, 7,5 mg / ml, 10 mg / ml oldatos injekció, Naropin 2 mg / ml oldatos infúzió
- Naropin 5 mg / ml oldatos injekció
Indikációk Miért használják a Naropint? Mire való?
A gyógyszer neve "Naropin oldatos injekció" vagy "Naropin oldatos infúzió".
- Ropivakain -hidroklorid nevű gyógyszert tartalmaz.
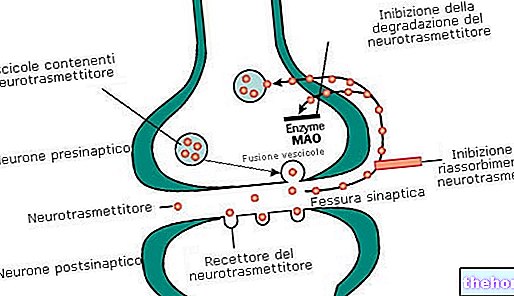
- A helyi érzéstelenítőknek nevezett gyógyszerek csoportjába tartozik.
- Ezt injekcióban vagy infúzióban fogják kapni, attól függően, hogy hogyan fogják használni. A Naropin 7,5 mg / ml -t felnőtteknél és 12 évnél idősebb gyermekeknél alkalmazzák a testrészek zsibbadására. A fájdalom megjelenésének megelőzésére vagy fájdalomcsillapításra szolgál.
Használható:
- A műtét során érzéstelenítse a testrészeket, beleértve a császármetszést is.
- Enyhítse a fájdalmat szülés közben, műtét után vagy sérülés után.
A Naropin 2 mg / ml -t felnőtteknél és minden korú gyermekeknél alkalmazzák akut fájdalom kezelésére.Bénítja (altatja) a testrészeket, pl. műtét után.
Ellenjavallatok Amikor a Naropin nem alkalmazható
Nem kaphat Naropin -t:
- - ha allergiás (túlérzékeny) a ropivakain -hidrokloridra vagy a Naropin egyéb összetevőjére (lásd 6. pont: További információk).
- - ha allergiás bármely más helyi érzéstelenítőre (pl. Lidokain vagy bupivakain).
- Ha azt mondták Önnek, hogy csökkent a vértérfogata (hipovolémia).
- Egy véredényben a test egy adott területének vagy a méhnyaknak a zsibbadásához, hogy enyhítse a szülés alatti fájdalmat.
Ha nem biztos abban, hogy a fentiek bármelyike vonatkozik -e Önre, konzultáljon orvosával, mielőtt elkezdi szedni a Naropin -t.
Az alkalmazással kapcsolatos óvintézkedések Mit kell tudnia a Naropin szedése előtt
mielőtt Naropina -t kapna. A Naropin fokozott elővigyázatossággal alkalmazható:
- Tájékoztassa kezelőorvosát, ha szív-, máj- vagy veseproblémái vannak, mivel orvosának módosítania kell a Naropin adagját.
- Tájékoztassa kezelőorvosát, ha azt mondták, hogy Önnek vagy családtagjainak ritka, porfíriának nevezett vérbetegsége van, és ebben az esetben az orvos más érzéstelenítőt is adhat Önnek.
- A kezelés előtt tájékoztassa kezelőorvosát minden korábbi betegségéről vagy egészségi állapotáról.
- Újszülötteknél, mivel érzékenyebbek a Naropinra.
- Gyermekeknél 12 éves korig bezárólag, mivel a test zsibbadt részeire adott injekciókat nem vizsgáltak fiatalabb gyermekeknél.
- Gyermekeknél 12 éves korig bezárólag, mivel a Naropin 7,5 mg / ml és 10 mg / ml injekciót a test zsibbadt területeire nem vizsgálták. A Naropin 2 mg / ml és 5 mg / ml adagjai alkalmasabb legyen.
Kölcsönhatások Mely gyógyszerek vagy élelmiszerek módosíthatják a Naropin hatását
Tájékoztassa kezelőorvosát, ha jelenleg vagy nemrégiben szedett más gyógyszereket, beleértve a vény nélkül kapható gyógynövényeket is. A Naropin befolyásolhatja más gyógyszerek hatásmechanizmusát, és egyes gyógyszerek hatással lehetnek a Naropinra.
Különösen tájékoztassa kezelőorvosát, ha az alábbi gyógyszerek bármelyikét szedi:
- Más helyi érzéstelenítők
- Erős fájdalomcsillapítók, például morfin vagy kodein.
- Szabálytalan szívverés (aritmia) kezelésére használt gyógyszerek, például lidokain és mexiletin. Tájékoztassa kezelőorvosát, hogy ezeket a gyógyszereket szedi a Naropin megfelelő adagjának meghatározásához.
Tájékoztassa kezelőorvosát is, ha az alábbi gyógyszerek bármelyikét szedi:
- Depresszió elleni gyógyszerek (például fluvoxamin).
- Antibiotikumok a baktériumok által okozott fertőzések kezelésére (például enoxacin). Ha ezeket a gyógyszereket szedi, a szervezetnek hosszabb ideig tart a Naropin eltávolítása.
Figyelmeztetések Fontos tudni, hogy:
Terhesség és szoptatás
A Naropin beadása előtt tájékoztassa kezelőorvosát, ha terhes, terhességet tervez vagy szoptat. Nem ismert, hogy a ropivakain -hidroklorid befolyásolja -e a terhességet, vagy átjut -e az anyatejbe.
Kérjen tanácsot orvosától vagy gyógyszerészétől, mielőtt bármilyen gyógyszert elkezdene szedni, ha terhes vagy szoptat.
A készítmény hatásai a gépjárművezetéshez és gépek kezeléséhez szükséges képességekre
A Naropin álmosságot okozhat, és befolyásolhatja a reakciósebességet. A Naropin beadása után másnapig ne vezessen gépjárművet, és ne használjon semmilyen eszközt vagy gépet.
Fontos információk a Naropin egyes összetevőiről
A Naropin legfeljebb 3,7 milligramm (mg) nátriumot tartalmaz milliliterenként (ml). Ha szabályozott nátrium -diétát folytat, ezt figyelembe kell vennie.
Adagolás, az alkalmazás módja és ideje A Naropin alkalmazása: Adagolás
A Naropint orvos fogja beadni Önnek. Az orvos által adott adag a fájdalomcsillapítás típusától függ. Ez a méretétől, életkorától és fizikai állapotától is függ.
A Naropint injekcióban vagy infúzióban fogják kapni. Az a testrész, ahol beadják, attól függ, hogy miért adják be a Naropint. Orvosa az alábbi helyek egyikén fogja beadni a Naropint:
- Az a testrész, amelyet érzésteleníteni kell.
- A test azon része közelében lévő terület, amelyet altatni kell.
- A testrésztől távol eső terület, amelyet el kell altatni. Ilyenkor "epidurális vagy infúziós injekciót (a gerincvelő körüli" területen) adnak be.
Ha a Naropint a fenti módszerek bármelyikén alkalmazzák, megakadályozza, hogy az idegek fájdalmas üzeneteket továbbítsanak az agyba. Nem fogja érezni a fájdalom, a meleg vagy a hideg érzését, de más érzése is lehet, például nyomás vagy tapintás.
Kezelőorvosa tudni fogja a gyógyszer helyes beadásának módját.
Túladagolás Mi a teendő, ha túladagolta a Naropin -t
A túl sok Naropin szedésének súlyos mellékhatásai különleges kezelést igényelnek, és orvosa kezelni tudja ezeket a helyzeteket. A Naropin túladagolásának első jelei általában a következők:
- Szédülés vagy szédülés.
- Az ajkak és a száj környékének zsibbadása.
- A nyelv zsibbadása.
- Hallási problémák.
- Látási (látási) problémák.
A súlyos mellékhatások kockázatának csökkentése érdekében orvosa abbahagyja a Naropin szedését, amint ezek a jelek megjelennek.
Ez azt jelenti, hogy ha a fentiek bármelyike előfordul, vagy ha úgy gondolja, hogy túl sok Naropin -t kapott, azonnal értesítse orvosát.
A Naropin túladagolásából eredő súlyosabb mellékhatások közé tartoznak a beszédproblémák, izomgörcsök, remegés, remegés, görcsök és eszméletvesztés.
Mellékhatások Melyek a Naropin mellékhatásai?
Mint minden gyógyszer, így a Naropin is okozhat mellékhatásokat, amelyek azonban nem mindenkinél jelentkeznek.
Fontos mellékhatások, amelyekre figyelni kell:
Hirtelen és életveszélyes allergiás reakciók (például anafilaxia) ritkák, 10 000-ből 1-10 beteget érint. Lehetséges tünetek közé tartozik a hirtelen kiütés, viszketés vagy csomós kiütés (csalánkiütés); az arc, az ajkak, a nyelv vagy más részek duzzanata zihálás, zihálás vagy légzési nehézség.
Ha úgy gondolja, hogy a Naropin allergiás reakciót okoz, azonnal értesítse orvosát.
Egyéb lehetséges mellékhatások:
Nagyon gyakori (10 beteg közül több mint 1 beteget érint)
- Alacsony vérnyomás (hipotenzió). Szédülést vagy szellemi zavart okozhat.
- Rosszullét (hányinger).
Gyakori (100 -ból 1-10 beteget érint)
- Paresztézia.
- Szédülés
- Fejfájás.
- Lassú vagy gyors szívverés (bradycardia, tachycardia).
- Magas vérnyomás (hipertónia).
- Visszahúzódott.
- Vizelési nehézség.
- Magas hőmérséklet (láz) vagy remegés (hidegrázás).
- Hátfájás.
Nem gyakori (1000 -ből 1-10 beteget érint)
- Szorongás.
- Csökkent bőrérzékenység.
- Ájulás.
- Nehéz légzés.
- Alacsony testhőmérséklet (hipotermia).
- Bizonyos tünetek akkor jelentkezhetnek, ha tévedésből adták be az erekbe, vagy ha túladagolták a Naropin -t (lásd még "Ha az előírtnál több Naropint kapott"). Ezek közé tartoznak a görcsrohamok, szédülés vagy mentális zavartság, az ajkak és a száj környékének zsibbadása, a nyelv zsibbadása, hallási problémák, látási (látási) problémák, beszédzavarok, izommerevség és remegés.
Ritka (10 000 -ből 1-10 beteget érint)
- Szívroham (szívmegállás).
- Szabálytalan szívverés (aritmia).
Egyéb lehetséges mellékhatások:
- Zsibbadás, a tű vagy az injekció okozta idegi irritáció miatt. Általában nem tart sokáig.
- Akaratlan izommozgások (diszkinézia).
Más helyi érzéstelenítőknél észlelt lehetséges mellékhatások, amelyeket szintén a Naropin okozhat:
- Bántják az idegeket. Ritkán (10 000 -ből 1-10 beteget érint) ez tartós problémákat okozhat.
- Ha a Naropin túladagolását a gerincvelői folyadékba adják, az egész test elzsibbadhat (altatásban).
Gyermekek
Gyermekeknél a mellékhatások ugyanazok, mint a felnőtteknél, kivéve a vérnyomáscsökkenést, amely ritkábban érinti a gyermekeket (100 -ból 1-10 gyermeket érint), és a hányást, amely gyakrabban fordul elő gyermekeknél (több mint 1 gyermeket érint). 10 éves gyerek).
Mellékhatások bejelentése
Ha Önnél bármilyen mellékhatás jelentkezik, tájékoztassa erről kezelőorvosát vagy a gondozását végző egészségügyi szakembert. Ez a betegtájékoztatóban fel nem sorolt bármilyen lehetséges mellékhatásra is vonatkozik. A mellékhatásokat közvetlenül a hatóság részére is bejelentheti az www.agenziafarmaco.gov.it/it webhelyen. felelős. A mellékhatások bejelentésével Ön is hozzájárulhat ahhoz, hogy minél több információ álljon rendelkezésre a gyógyszer biztonságosságáról.
Lejárat és megőrzés
- Gyermekektől elzárva tartandó!
- A dobozon feltüntetett lejárati idő (EXP) után ne alkalmazza a Naropin -t. A lejárati idő a hónap utolsó napjára vonatkozik.
- Legfeljebb 30 ° C -on tárolandó. Nem fagyasztható.
- A Naropint általában orvosa vagy kórháza tárolja, akik szintén felelősek a termék minőségéért, ha a felbontás után nem használják fel. A gyógyszert használat előtt szemrevételezéssel meg kell vizsgálni Az oldatot csak akkor szabad használni, ha tiszta, lényegében részecskéktől mentes, és ha a tartály sértetlen.
- Felelősek a fel nem használt Naropin megfelelő megsemmisítéséért is.
Határidő "> Egyéb információ
Mit tartalmaz a Naropin?
A készítmény hatóanyaga a ropivakain -hidroklorid.
A Naropin a következő hatáserősségben kapható: 2 mg, 7,5 mg vagy 10 mg ropivakain -hidroklorid milliliterenként.
Egyéb összetevők: nátrium -klorid, sósav és / vagy nátrium -hidroxid és injekcióhoz való víz.
Milyen a Naropin külleme és mit tartalmaz a csomagolás?
A Naropin tiszta és színtelen oldatos injekció vagy infúzió.
A 2 mg / ml, 7,5 mg / ml és 10 mg / ml Naropin oldatos injekció a következő formában kapható:
- 10 ml -es polipropilén injekciós üveg (Polyamp) 5 vagy 10 darabos csomagolásban.
- 20 ml -es polipropilén injekciós üvegek (Polyamp) 5 vagy 10 darabos csomagolásban.
A Naropin 2 mg / ml oldatos infúzió a következő formában kapható:
- 100 ml -es polipropilén zsákok (Polybag) 5 darabos csomagolásban.
- 200 ml -es polipropilén zsákok (Polybag) 5 darabos csomagolásban.
Nem minden típusú kiszerelés kerülhet forgalomba.
Forrás betegtájékoztató: AIFA (Olasz Gyógyszerügynökség). A tartalom 2016 januárjában jelent meg. A jelenlévő információk nem feltétlenül naprakészek.
A legfrissebb verzióhoz való hozzáféréshez ajánlatos az AIFA (Olasz Gyógyszerügynökség) webhelyét elérni. Jogi nyilatkozat és hasznos információk.
01.0 A GYÓGYSZER MEGNEVEZÉSE -
NAROPINE
02.0 MINŐSÉGI ÉS MENNYISÉGI ÖSSZETÉTEL -
Naropin 2 mg / ml:
1 ml oldatos injekció 2 mg ropivakain -hidrokloridnak megfelelő ropivakain -hidroklorid -monohidrátot tartalmaz.
1 ampulla 10 ml vagy 20 ml oldatos injekció 20 mg ropivakain -hidroklorid -monohidrátot, illetve 40 mg ropivakain -hidrokloridot tartalmaz.
1 tasak 100 ml infúziós oldat 200 mg ropivakain -hidrokloridnak megfelelő ropivakain -hidroklorid -monohidrátot tartalmaz.
Naropin 7,5 mg / ml:
1 ml oldatos injekció 7,5 mg ropivakain -hidrokloridnak megfelelő ropivakain -hidroklorid -monohidrátot tartalmaz.
1 ampulla 10 ml vagy 20 ml oldatos injekció 75 mg ropivakain -hidroklorid -monohidrátot, illetve 150 mg ropivakain -hidrokloridot tartalmaz.
Naropin 10 mg / ml:
1 ml oldatos injekció 10 mg ropivakain -hidrokloridnak megfelelő ropivakain -hidroklorid -monohidrátot tartalmaz.
1 ampulla 10 ml vagy 20 ml oldatos injekció 100 mg ropivakain -hidroklorid -monohidrátot, illetve 200 mg ropivakain -hidrokloridot tartalmaz.
Segédanyagok:
2 mg / ml:
Minden 10 ml -es injekciós üveg 1,48 mmol (34 mg) nátriumot tartalmaz
Minden 20 ml -es injekciós üveg 2,96 mmol (68 mg) nátriumot tartalmaz
Minden 100 ml -es tasak 14,8 mmol (340 mg) nátriumot tartalmaz
7,5 mg / ml:
Minden 10 ml -es injekciós üveg 1,3 mmol (29,9 mg) nátriumot tartalmaz
Minden 20 ml -es injekciós üveg 2,6 mmol (59,8 mg) nátriumot tartalmaz
10 mg / ml:
Minden 10 ml -es injekciós üveg 1,2 mmol (28 mg) nátriumot tartalmaz
Minden 20 ml -es injekciós üveg 2,4 mmol (56 mg) nátriumot tartalmaz
A segédanyagok teljes listáját lásd a 6.1 pontban.
03.0 GYÓGYSZERFORMA -
Injektálható oldat.
Oldatos infúzió.
Tiszta és színtelen oldat.
04.0 KLINIKAI INFORMÁCIÓK -
04.1 Terápiás javallatok -
A Naropin 7,5 mg / ml és 10 mg / ml felnőttek és 12 év feletti serdülők kezelésére javallt:
Sebészeti érzéstelenítés:
- epidurális blokkok a sebészetben, beleértve a császármetszést is
- fő idegblokkok
- a sebészeti terület blokkjai
A Naropin 2 mg / ml akut fájdalom kezelésére javallt:
Felnőtteknél és 12 év feletti serdülőknél:
- Folyamatos epidurális infúzió vagy szakaszos bólus beadás műtét utáni fájdalom és születési fájdalomcsillapítás esetén
- a sebészeti terület blokkjai
- a perifériás idegek folyamatos blokkolása folyamatos infúzióval vagy szakaszos bolus injekciókkal, például a műtét utáni fájdalom kezelésére
1 évesnél idősebb csecsemőknél és 12 év alatti gyermekeknél (periódus utáni és posztoperatív):
- a perifériás idegek egyetlen és folyamatos blokkja
Újszülötteknél, csecsemőknél és 12 év alatti gyermekeknél (periódus és posztoperatív időszak):
- caudalis epidurális blokk
- folyamatos epidurális infúzió
04.2 Adagolás és alkalmazás
A Naropint csak regionális érzéstelenítésben jártas orvosok használhatják, vagy felügyeletük alatt.
Adagolás
Felnőttek és 12 év feletti serdülők
Az alábbi táblázat útmutatást nyújt az ajánlott adagokhoz a leggyakoribb blokktípusokban. Az alkalmazandó dózisnak a legalacsonyabbnak kell lennie a hatékony blokádhoz. Az adagolást az orvos tapasztalatai és a beteg klinikai állapotára vonatkozó ismeretek alapján kell kiválasztani.
1. táblázat Felnőttek és 12 év feletti serdülők
A táblázatban feltüntetett adagok szükségesek a megfelelő blokád kialakításához, és útmutatásként kell tekinteni a felnőtteknél történő alkalmazásra. Azonban előfordulhatnak egyéni eltérések az aktivitás kezdetében és az időtartamban. Az "adag" oszlop az intervallumokat mutatja. szükséges dózis A referenciaszövegeket tanulmányozni kell mind a specifikus blokkolási technikákat érintő szempontokról, mind a páciens egyéni igényeiről.
* A fő idegblokk tekintetében csak brachialis plexus blokkolás esetén ajánlott adag.
Más típusú idegblokkok esetén kisebb adagokra lehet szükség.Azonban jelenleg nincs tapasztalat más típusú blokádokra vonatkozó ajánlott dózisokról.
1) A növekvő adagokat körülbelül 100 mg (97,5 mg = 13 ml; 105 mg = 14 ml) dózistól kezdve kell beadni 3-5 perces időtartam alatt, összesen 50 mg.
2) n / a = nem alkalmazható.
3) A fő idegblokk adagját a beadás helyének és a beteg állapotának megfelelően kell beállítani.
Az interscalenicus és a supraclavicularis brachialis plexusok elzáródása a használt helyi érzéstelenítőktől függetlenül gyakoribb súlyos mellékhatásokkal járhat (lásd 4.4 pont).
Általában a sebészeti érzéstelenítés (pl. Epidurális alkalmazás esetén) magasabb koncentrációk és dózisok alkalmazását igényli. A Naropin 10 mg / ml alkalmazása epidurális érzéstelenítésben ajánlott olyan műtéteknél, ahol teljes motoros blokk szükséges. Alacsonyabb koncentrációk és adagok ajánlottak fájdalomcsillapításra (pl. Epidurális alkalmazáshoz akut fájdalom kezelésére).
Az alkalmazás módja
Az intravaszkuláris injekció elkerülése érdekében óvatos leszívás javasolt az injekció előtt és alatt. Nagy dózisú injekció beadása esetén ajánlott 3-5 ml lidokain és adrenalin (epinefrin) vizsgálati adagot végrehajtani. A "véletlen intravaszkuláris injekciót a szívfrekvencia átmeneti emelkedése, míg a" véletlen intratekális injekciót a gerincblokk jelei alapján ismerhetjük fel.
Az aspirációt a gyógyszer beadása előtt és alatt kell elvégezni, amelyet lassan vagy osztott adagokban kell beadni, 25-50 mg / perc sebességgel, szoros megfigyelés mellett tartva a beteg életfunkcióit és fenntartva a verbális kapcsolatot. toxicitást, a beadást azonnal abba kell hagyni.
Az epidurális blokk műtét során egyszeri, legfeljebb 250 mg ropivakain dózist alkalmaztak és jól tolerálták.
A brachialis plexus blokkjában 300 mg egyszeri adagot adtak be korlátozott számú betegnek, és jól tolerálták.
Ha hosszan tartó blokkolást végeznek, akár folyamatos epidurális infúzióval, akár ismételt bolus -beadással, mérlegelni kell a toxikus plazmakoncentráció elérésének vagy a helyi idegsejtek károsodásának lehetséges kockázatát. A műtét utáni időszakban sebészeti érzéstelenítésre és fájdalomcsillapításra adott, 24 órán keresztül adott, legfeljebb 675 mg ropivakain-dózist felnőttek jól tolerálták, akárcsak a műtét utáni időszakban 72 órán át tartó, akár 28 mg / órás folyamatos epidurális infúziókat. Korlátozott számú betegnél nagyobb, akár 800 mg / nap dózisokat adtak be viszonylag alacsony számú mellékhatással.
A műtét utáni fájdalom kezelésére a következő technika ajánlott: hacsak a műtét előtt már nem indukálták, epidurális blokkolást végeznek a Naropin 7,5 mg / ml epidurális katéteren keresztül történő beadásával. Ezután fájdalomcsillapítást végeznek, amelyet Naropin infúzióval tartanak fenn. 2 mg / ml: a posztoperatív fájdalom legtöbb esetben, közepes vagy súlyos, a 6-14 ml (12-28 mg / h) infúzió megfelelő fájdalomcsillapítást tart fenn, csak enyhe és nem progresszív motoros blokk esetén. Az epidurális blokk maximális időtartama 3 nap. Mindenesetre gondosan ellenőrizni kell a fájdalomcsillapító hatást a katéter eltávolítása érdekében, amint a fájdalom intenzitása lehetővé teszi. Ezzel a technikával jelentősen csökkent az opioidok alkalmazásának szükségessége.
A klinikai vizsgálatok során a Naropin 2 mg / ml epidurális infúzióját önmagában vagy 1-4 mcg / ml fentanillal keverve legfeljebb 72 órán keresztül adták be a műtét utáni fájdalomcsillapításra.
A Naropin és a fentanil kombinációja további fájdalomcsillapítást tett lehetővé, de az opioidok alkalmazása miatt mellékhatásokat okozott.
A Naropin és a fentanil kombinációját csak 2 mg / ml Naropin esetében vizsgálták.
Ha hosszan tartó perifériás idegblokkokat végeznek, akár folyamatos infúzióval, akár ismételt injekciókkal, akkor mérlegelni kell a toxikus plazmakoncentráció elérésének vagy helyi idegsejtek károsodásának kockázatát. A klinikai vizsgálatok során a combcsont -ideg blokkolását 300 mg Naropin 7,5 mg / ml és az interscalenicus blokkot 225 mg Naropin 7,5 mg / ml adaggal érték el a műtét előtt. Az L "fájdalomcsillapítást ezután 2 mg / ml Naropin -nal fenntartottuk. Az infúziós sebesség vagy az időszakos, 10-20 mg -os injekciók óránként 48 órán keresztül megfelelő fájdalomcsillapítást biztosítottak, és jól toleráltak.
A Naropin 7,5 mg / ml -nél magasabb koncentrációban történő alkalmazását nem dokumentálták császármetszéssel.
Gyermekpopuláció
2. táblázat Epidurális blokk: gyermekgyógyászati betegek 0 (teljes idejű csecsemők)-12 év
A táblázatban feltüntetett dózist a gyermekgyógyászatban alkalmazandó útmutatónak kell tekinteni. Egyéni eltérésekre lehet szükség. Magas testtömegű gyermekgyógyászati betegeknél gyakran szükség van az adag fokozatos csökkentésére, és az ideális testsúlyt kell alapul venni. Epidurális caudalis blokk és az epidurális bolus adagok térfogata nem haladhatja meg a 25 ml -t minden egyes beteg esetében. Referenciaszövegeket kell olvasni, mind a specifikus blokkolási technikákat érintő szempontok, mind a páciens egyéni igényei tekintetében.
a) A bejelentett dózistartományban a mellkasi epidurális blokkoknál alacsonyabb, míg az ágyéki vagy farok epidurális blokkoknál nagyobb adagok ajánlottak.
b) Lumbális epidurális blokkokhoz ajánlott. Jó gyakorlat az epidurális mellkasi fájdalomcsillapítás esetén a bolus adagjának csökkentése.
A 7,5 mg / ml és 10 mg / ml ropivakain alkalmazása szisztémás és központi toxikus eseményekkel járhat gyermekeknél. Alacsonyabb koncentrációk (2 mg / ml és 5 mg alkalmasabbak ebben a populációban). / Ml).
A ropivakain koraszülötteknél történő alkalmazását nem dokumentálták.
3. táblázat Perifériás idegblokkok: 1-12 éves csecsemők és gyermekek
A táblázatban feltüntetett dózist a gyermekgyógyászatban alkalmazandó útmutatónak kell tekinteni. Egyéni eltérésekre lehet szükség. Magas testtömegű gyermekgyógyászati betegeknél gyakran szükséges az adag fokozatos csökkentése, és az ideális testsúlyt kell alapul venni. konzultáltak mind a specifikus blokkolási technikákat érintő szempontokról, mind a páciens egyéni igényeiről.
A perifériás idegblokk egyszeri injekciói (pl. Ilioinguinalis idegblokk, brachialis plexus blokk, iliac fascia rekesz blokk) nem haladhatják meg a 2,5 - 3,0 mg / kg értéket.
A csecsemők és gyermekek perifériás blokkjának adagjai útmutatást adnak a súlyos betegségben nem szenvedő gyermekeknél történő alkalmazáshoz.
Az alkalmazás módja
Az injekció beadása előtt és alatt óvatos leszívás javasolt az intravaszkuláris beadás elkerülése érdekében.Az injekció beadása során a beteg életfunkcióit gondosan figyelni kell. Ha toxikus tünetek jelentkeznek, az alkalmazást azonnal abba kell hagyni.
A betegek többségénél a ropivakain 2 mg / ml -es egyszeri farok -epidurális injekciója a T12 -szint alatt "megfelelő posztoperatív fájdalomcsillapítást eredményez, ha 2 mg / kg 1 ml / kg -os dózist alkalmaznak." adaptálni kell az érzékszervi blokk eltérő eloszlásának eléréséhez, ahogyan azt a referenciaszövegek jelzik. A 3 mg / ml -es ropivakain -koncentrációnál 3 mg / kg -ig terjedő adagokat 4 évesnél idősebb gyermekeknél értékelték. Azonban "a motorblokkok magas előfordulása társul ehhez a koncentrációhoz".
Javasolt a helyi érzéstelenítő kiszámított dózisának fokozatos alkalmazása, az alkalmazás módjától függetlenül.
04.3 Ellenjavallatok -
Túlérzékenység a ropivakainra vagy más amid típusú helyi érzéstelenítőkre.
Figyelembe kell venni az epidurális érzéstelenítés tipikus ellenjavallatait, függetlenül az alkalmazott helyi érzéstelenítőtől.
Regionális intravénás érzéstelenítés.
Szülészeti paracervicalis érzéstelenítés.
Hypovolemia.
04.4 Különleges figyelmeztetések és a használattal kapcsolatos óvintézkedések -
A regionális érzéstelenítési eljárásokat mindig megfelelően felszerelt területeken és szakképzett személyzettel kell elvégezni. Ezenkívül a nyomon követéshez és a sürgősségi újraélesztéshez szükséges eszközöknek és gyógyszereknek azonnal rendelkezésre kell állniuk.
A súlyos blokádon átesett betegeknek optimális állapotban kell lenniük, és intravénás katétert kell behelyezniük a blokkolási eljárás előtt.
A felelős aneszteziológusnak megfelelő óvintézkedéseket kell tennie az intravaszkuláris injekció elkerülése érdekében (lásd 4.2 pont), és megfelelő tapasztalattal és ismeretekkel kell rendelkeznie a mellékhatások, a szisztémás toxicitás és egyéb szövődmények diagnosztizálásával és kezelésével kapcsolatban (lásd 4.8 és 4.9 pont). subarachnoid injekció, amely magas gerincblokkhoz vezethet, apnoe és hypotensio esetén. A görcsök gyakrabban fordultak elő a brachialis plexus és az epidurális blokk után. Ez valószínűleg a véletlen intravaszkuláris injekció vagy az injekció beadásának helyéről történő gyors felszívódás eredménye.
Legyen óvatos, nehogy injekciót adjon a gyulladt területekre.
Szív- és érrendszer
A III. Osztályú antiaritmiás gyógyszerekkel (pl. Amiodaron) kezelt betegeket gondosan ellenőrizni kell, és mérlegelni kell az EKG monitorozását, mivel a szívhatások additívak lehetnek.
Ritka szívelégtelenségről számoltak be a Naropin epidurális érzéstelenítésben vagy perifériás idegblokkban történő alkalmazása során, különösen idős betegeknél és egyidejű szívbetegségben szenvedő betegeknél történt véletlen intravaszkuláris beadás után. Egyes esetekben újraélesztés történt. tartós újraélesztési erőfeszítésre lehet szükség a siker esélyeinek növeléséhez.
Elzáródás a nyakban és a fejben
Egyes helyi érzéstelenítési eljárások, például a fej és a nyak régiójába történő injekciózás, a használt helyi érzéstelenítőktől függetlenül, gyakrabban járhatnak súlyos mellékhatásokkal.
Elzáródás a fő perifériás idegekben
A perifériás főidegek blokádja nagyobb térfogatú helyi érzéstelenítőt eredményezhet egy erősen vaszkuláris területen, gyakran a nagy erek közelében, ahol fokozott az intravaszkuláris injekció és / vagy a gyors szisztémás felszívódás kockázata. magas plazmakoncentrációhoz vezethet.
Túlérzékenység
Figyelembe kell venni a kereszt-túlérzékenység lehetőségét más amid típusú helyi érzéstelenítőkkel.
Hypovolemia
A hypovolaemiában szenvedő betegek bármilyen ok miatt hirtelen és súlyos hipotenziónak lehetnek kitéve az epidurális érzéstelenítés során, függetlenül az alkalmazott helyi érzéstelenítőtől.
Rossz általános állapotú betegek
A rossz általános állapotú betegeknek, életkoruk vagy egyéb veszélyeztető tényezők, például a szívvezetés részleges vagy teljes blokkolása, előrehaladott májbetegség vagy súlyos vesekárosodás miatt, különös figyelmet kell fordítaniuk, azonban ezeknél a betegeknél gyakran javallott a regionális érzéstelenítés.
Károsodott máj- és vesefunkciójú betegek
A ropivakaint a máj metabolizálja, ezért óvatosan kell alkalmazni súlyos májkárosodásban szenvedő betegeknél; az ismételt dózist csökkenteni kell a késleltetett elimináció miatt. Ha a Naropin-t egyszeri adagként vagy rövid távú kezelésben alkalmazzák károsodott veseműködésű betegeknél, általában nincs szükség az adag módosítására. Acidózis és csökkent plazmafehérje-koncentráció, gyakran megfigyelhető krónikus veseelégtelenségben, növelheti a szisztémás toxicitás kockázatát.
Akut porfíria
A Naropin oldatos injekció és infúzió valószínűleg porfirinogén, és csak akut porfíriában szenvedő betegeknél írható fel, ha nincs biztonságosabb alternatíva. Megfelelő óvintézkedéseket kell tenni a veszélyeztetett betegek esetében, a szabványos referenciaszövegekben leírtaknak megfelelően és / vagy e betegség szakértőivel konzultálva.
Kondrolízis
A forgalomba hozatalt követően beszámoltak chondrolysisről azoknál a betegeknél, akik folyamatos műtét utáni intraartikuláris infúziót kaptak helyi érzéstelenítőkből, beleértve a ropivakaint is. A folyamatos intraartikuláris infúzió nem jóváhagyott indikáció a Naropin számára. Kerülni kell a Naropin-nal történő folyamatos intraartikuláris infúziót, mivel a hatásosság és a biztonságosság nem bizonyított.
Ismert hatású / hatású segédanyagok
A gyógyszerkészítmény legfeljebb 3,7 mg nátriumot tartalmaz milliliterenként, ezt figyelembe kell venni kontrollált nátrium -diétás betegeknél.
Elhúzódó ügyintézés
Kerülni kell a ropivakain hosszan tartó alkalmazását azoknál a betegeknél, akiket egyidejűleg erős CYP1A2 inhibitorokkal, például fluvoxaminnal és enoxacinnal kezelnek (lásd 4.5 pont).
Gyermekpopuláció
Különös figyelmet kell fordítani az újszülöttekre a metabolikus utak éretlensége miatt. Az újszülötteknél végzett klinikai vizsgálatok során megfigyelt ropivakain plazmakoncentrációban tapasztalt nagy eltérések arra utalnak, hogy ebben a korcsoportban fokozott a szisztémás toxicitás kockázata, különösen folytatódik az epidurális infúzió.
Az ajánlott adagok újszülötteknél korlátozott klinikai adatokon alapulnak.
Ha ropivakaint alkalmaznak ebben a betegcsoportban, rendszeresen ellenőrizni kell a szisztémás toxicitást (pl. Központi idegrendszeri toxicitás jelei, EKG, SpO2) és a helyi neurotoxicitást (pl. Elhúzódó gyógyulás). A készítmény újszülöttekben történő lassú eliminációját követően az ellenőrzést az infúzió befejezése után is folytatni kell.
- A 7,5 mg / ml és 10 mg / ml ropivakain biztonságosságát és hatásosságát 12 év alatti gyermekeknél még nem igazolták.
- A 2 mg / ml ropivakain biztonságosságát és hatásosságát sebészeti blokád esetén 12 év alatti gyermekek esetében nem igazolták.
- A 2 mg / ml ropivakain biztonságosságát és hatásosságát perifériás idegblokk esetén 1 évesnél fiatalabb csecsemők esetében nem igazolták.
04.5 Kölcsönhatások más gyógyszerekkel és egyéb interakciók -
A Naropin-t óvatosan kell alkalmazni olyan betegeknél, akiket más helyi érzéstelenítőkkel vagy a helyi amid típusú érzéstelenítőkhöz szerkezetileg kapcsolódó anyagokkal, például bizonyos antiaritmiás szerekkel, például lidokainnal és mexiletinnel kezelnek, mivel a szisztémás toxikus hatások additívak.
A Naropin és általános érzéstelenítők vagy opiátok együttes alkalmazása a megfelelő (káros) hatások kölcsönös fokozását eredményezheti.
A ropivakainnal és a III. Osztályú antiaritmiás gyógyszerekkel (pl. Amiodaron) nem végeztek specifikus interakciós vizsgálatokat, de ezekben az esetekben óvatosság ajánlott (lásd még 4.4 pont).
A citokróm P450 (CYP) 1A2 részt vesz a ropivakain fő metabolitja, a 3-hidroxi-ropivakain képződésében. In vivo a ropivakain plazma clearance-e akár 77% -kal csökken a fluvoxaminnal, amely a CYP1A2 szelektív és erős inhibitora. Következésképpen a CYP1A2 erős inhibitorai, például a fluvoxamin és az enoxacin kölcsönhatásba léphetnek a Naropin -nal, ha egyidejűleg alkalmazzák annak hosszan tartó alkalmazásával. Kerülni kell a ropivakain hosszan tartó alkalmazását azoknál a betegeknél, akiket egyidejűleg erős CYP1A2 inhibitorokkal kezelnek, lásd még 4.4 pont.
In vivo a ropivakain plazma clearance-e 15% -kal csökken, amikor ketokonazollal, a CYP3A4 szelektív és erős inhibitorával együtt alkalmazzák. Ennek az izoenzimnek a gátlásának azonban nincs klinikai jelentősége.
Az in vitro ropivakain a CYP2D6 versenyképes inhibitora, de úgy tűnik, hogy klinikai plazmakoncentrációban nem gátolja ezt az izoenzimet.
04.6 Terhesség és szoptatás -
Terhesség
A szülészet epidurális beadását leszámítva nincs elegendő adat a ropivakain terhes nőkön történő alkalmazásáról.Az állatokon végzett kísérleti vizsgálatok nem utalnak közvetlen vagy közvetett káros hatásokra a terhesség, az embrionális / magzati fejlődés, a szülés vagy a születés utáni fejlődés tekintetében (lásd 5.3 pont).
Etetési idő
Nincs adat a ropivakain kiválasztódásáról az anyatejbe.
04.7 Hatások a gépjárművezetéshez és gépek kezeléséhez szükséges képességekre -
Erről nem állnak rendelkezésre adatok. A dózishoz képest a helyi érzéstelenítők kevésbé nyilvánvalóan befolyásolhatják a mentális funkciókat és a koordinációt, még akkor is, ha nincs nyilvánvaló központi idegrendszeri toxicitás, és átmenetileg hátrányosan befolyásolhatják a mozgást és az éberséget.
04.8 Nemkívánatos hatások -
Tábornok
A Naropin mellékhatásprofilja hasonló a többi hosszú hatású amid típusú helyi érzéstelenítőhöz. A mellékhatásokat meg kell különböztetni az idegblokkot követő fiziológiai hatásoktól, mint például a csökkent vérnyomás és a bradycardia.
4. táblázat: A mellékhatások táblázata
A 4.8 pontban található táblázatban használt gyakoriságok: nagyon gyakori (≥1 / 10), gyakori (≥1 / 100,
nak nek) Gyermekeknél a hipotenzió kevésbé gyakori (> 1/100).
b) A hányás gyakoribb gyermekeknél (> 1/10).
* ezek a tünetek rendszerint véletlen intravaszkuláris beadás, túladagolás vagy gyorsan felszívódás után jelentkeznek, lásd 4.9 pont.
Osztályhoz kapcsolódó mellékhatások
Neurológiai szövődmények
Az alkalmazott helyi érzéstelenítőtől függetlenül a neuropátiákat és a gerincvelő elváltozásait (pl. Elülső spinalis artéria szindróma, arachnoiditis, cauda equina szindróma) összefüggésbe hozták a regionális érzéstelenítéssel, amely ritka esetekben tartós következményeket okozhat.
Teljes gerincblokk
Teljes gerincblokk alakulhat ki, ha epidurális adagot véletlenül intratekálisan adnak be.
Akut szisztémás toxicitás
A szisztémás toxikus reakciók elsősorban a központi idegrendszert (CNS) és a kardiovaszkuláris rendszert (CVS) érintik. Ezeket a reakciókat a "helyi érzéstelenítők magas vérkoncentrációja okozza, amelyet kiválthat" véletlen intravaszkuláris injekció, túladagolás vagy kivételesen gyors felszívódás egy erősen vaszkuláris területről, lásd 4.4 pont. A központi idegrendszeri reakciók hasonlóak az összes helyi érzéstelenítővel amid típusú, míg a szívreakciók mennyiségi és minőségi szempontból is jobban függenek a gyógyszertől.
Központi idegrendszeri toxicitás
A központi idegrendszeri toxicitás fokozatosan jelentkezik, egyre súlyosabb tünetekkel és jelekkel. Kezdetben olyan tüneteket észlelnek, mint: látási vagy hallási zavarok, perioralis hypoesthesia, szédülés, mentális zavartság, vellichio és paresztézia. A legsúlyosabb hatások a diszartria, az izommerevség és az izomgörcs, és megelőzhetik az általános görcsöket. Ezeket a tüneteket nem szabad összetéveszteni a neurotikus viselkedéssel. Eszméletvesztés és görcsök (grand mal) következhetnek, amelyek néhány másodperctől néhány percig tarthatnak A görcsrohamok során a fokozott izomtevékenység és a légzés zavarása miatt gyorsan kialakulhat hipoxia és hiperkapnia. Súlyos esetekben apnoe is előfordulhat. A légzőrendszeri és metabolikus acidózis fokozza és meghosszabbítja a helyi érzéstelenítők toxikus hatását.
A páciens visszatérése a kezdeti klinikai állapotokhoz a helyi érzéstelenítők központi idegrendszerben történő újraelosztása, valamint az ezt követő anyagcsere és kiválasztás eredménye. A gyógyulás gyors lehet, ha nem adtak be nagy mennyiségű gyógyszert.
Szív- és érrendszeri toxicitás
A kardiovaszkuláris toxicitás súlyosabb helyzetet jelez. A helyi érzéstelenítők magas szisztémás koncentrációjának eredményeként hipotenzió, bradycardia, aritmia és akár szívmegállás is kialakulhat. Önkénteseknél a ropivakain intravénás infúziója csökkentette a vezetőképességet és a kontraktilitást.
A szív- és érrendszeri toxikus hatásokat általában a központi idegrendszeri toxicitás jelei előzik meg, kivéve, ha a beteg általános érzéstelenítést kapott, vagy erősen nyugtatta benzodiazepinekkel vagy barbiturátokkal.
Gyermekeknél a helyi érzéstelenítő toxicitás korai jeleit nehéz lehet észlelni, mivel előfordulhat, hogy nem tudják verbálisan kifejezni magukat. Lásd 4.4 pont.
Gyermekpopuláció
A mellékhatások gyakorisága, típusa és súlyossága gyermekeknél feltételezhetően megegyezik a felnőttekével, kivéve a gyermekeknél ritkábban előforduló hipotenziót (10 betegből 1).
Gyermekeknél a helyi érzéstelenítő toxicitás korai jelei nehezen észlelhetők, mivel lehet, hogy nem tudják verbálisan kifejezni (lásd még 4.4 pont).
Akut szisztémás toxicitás kezelése
Lásd 4.9.
A feltételezett mellékhatások bejelentése
A gyógyszer engedélyezése után jelentkező feltételezett mellékhatások bejelentése fontos, mivel lehetővé teszi a gyógyszer előny / kockázat arányának folyamatos nyomon követését. Az egészségügyi szakembereket kérjük, hogy jelentsék be a feltételezett mellékhatásokat a nemzeti bejelentési rendszeren keresztül. "Cím www. agenziafarmaco.gov.it/it/responsabili.
04.9 Túladagolás -
Tünetek
A helyi érzéstelenítők véletlen intravaszkuláris injekciója azonnali szisztémás toxikus hatásokat okozhat (másodpercek -percek alatt). Túladagolás esetén a maximális plazmakoncentráció az injekció helyétől függően nem érhető el az első és a második óra között, ezért a toxicitás jelei késleltethetők (lásd 4.8 pont).
Kezelés
A helyi érzéstelenítők alkalmazását azonnal abba kell hagyni, ha akut szisztémás toxicitás tünetei jelentkeznek, és a központi idegrendszeri tüneteket (központi idegrendszeri görcsök és depresszió) gyorsan kezelni kell megfelelő légúti / légzőszervi támogatással és görcsoldó gyógyszerekkel.
Keringési leállás esetén a kardiopulmonális újraélesztést azonnal el kell végezni. Létfontosságú az optimális oxigénellátás biztosítása, a szellőzés és a keringés támogatása, valamint az acidózis kezelése.
Szív- és érrendszeri depresszió (hipotenzió, bradycardia) esetén mérlegelni kell a megfelelő kezelést intravénás folyadékokkal, érszűkítőkkel és vagy inotróp gyógyszerekkel. A gyermekeknek az életkornak és a testsúlynak megfelelő adagot kell adni.
Szívmegállás esetén elhúzódó újraélesztésre lehet szükség a siker esélyeinek növelése érdekében.
05.0 FARMAKOLÓGIAI TULAJDONSÁGOK -
05,1 "Farmakodinamikai tulajdonságok -
Farmakoterápiás csoport: helyi érzéstelenítők, keményítők.
ATC kód: N01B B09.
A ropivakain egy hosszú hatású, amid típusú helyi érzéstelenítő, amely érzéstelenítő és fájdalomcsillapító hatással is rendelkezik. Nagy dózisokban a Naropin sebészeti érzéstelenítést okoz, míg az alacsonyabb dózisok érzékszervi blokkot okoznak, korlátozott és nem progresszív motoros blokkolással.
A hatásmechanizmus az idegrostok membránjának nátrium -ionokra való áteresztőképességének reverzibilis csökkenésével magyarázható. Ennek eredményeként csökken a depolarizációs ráta és növekszik az ingerlékenységi küszöb, ami az idegimpulzusok blokkolásához vezet. helyi szinten.
A ropivakain legjellemzőbb tulajdonsága a hosszú hatástartam. Az aktivitás kezdete és a helyi érzéstelenítés hatékonysága az alkalmazás helyétől és az adagolástól függ, és nem befolyásolja őket az érszűkítő (pl. Adrenalin (epinefrin)) jelenléte. . A tevékenység megkezdésével és a hatás időtartamával kapcsolatos részleteket az "Adagolás és az alkalmazás módja" című 1. táblázat tartalmazza.
Egészséges önkénteseknél az intravénás infúzióban beadott ropivakaint alacsony dózisokban jól tolerálták. Nagy dózisok (maximális tolerált dózis) esetén a központi idegrendszer várható tünetei jelentkeztek. Az ezzel a gyógyszerrel végzett klinikai vizsgálatok azt mutatják, hogy a tolerancia jó, ha az ajánlott adagokban megfelelően alkalmazzák.
05,2 "Farmakokinetikai tulajdonságok -
A ropivakain királis centrummal rendelkezik, és tiszta balkezes enantiomer formában kapható. Nagyon zsírban oldódó. Minden metabolitja helyi érzéstelenítő hatással rendelkezik, de lényegesen kisebb hatékonysággal és rövidebb ideig tart, mint a ropivakain.
A ropivakain plazmakoncentrációja függ az adagolástól, az alkalmazás módjától és az injekció beadásának helyének vaszkuláris jellegétől.
A ropivakain lineáris kinetikát követ, a Cmax pedig dózisarányos.
A ropivakain felnőtteknél teljes és kétfázisú felszívódást mutat az epidurális térből, a két fázis felezési ideje 14 perc, illetve 4 óra. A lassú felszívódás korlátozza a ropivakain eliminációját; ez megmagyarázza, hogy az epidurális alkalmazás után a látszólagos eliminációs felezési idő hosszabb, mint az intravénás beadás után.
A ropivakain kétfázisú felszívódást mutat a farok epidurális teréből még gyermekeknél is.
A ropivakain átlagos plazma clearance-e nagyságrendileg 440 ml / perc, vese clearance-e 1 ml / perc, az egyensúlyi állapotú eloszlási térfogat 47 liter, a végső felezési idő pedig 1,8 óra iv. A ropivakain közepes májkivonási aránya 0,4, és a plazmában főként az 1-es savas glikoproteinhez kötődik, a kötetlen frakció körülbelül 6%.
A folyamatos és interskalénikus epidurális infúzió során a teljes plazmakoncentráció növekedését észlelték, ami korrelálhat az a1-es glikoprotein műtét utáni növekedésével. A kötetlen, farmakológiailag aktív frakció koncentrációjának változása kisebb volt, mint a plazma koncentráció.összesen.
Mivel a ropivakain közepes és alacsony májkivonási aránya van, eliminációs sebessége függ a kötetlen plazmakoncentrációtól.
Gyermekekkel és felnőttekkel végzett klinikai vizsgálatokban az AAG műtét utáni növekedését figyelték meg, ami a kötetlen frakció csökkenéséhez vezetett, a fokozott fehérjekötődés miatt, ami a teljes clearance csökkenését és a plazmakoncentráció növekedését eredményezte.
A kötetlen ropivakain clearance változatlan marad, amint azt a posztoperatív infúzió során megfigyelt stabil koncentrációk is bizonyítják.
A kötetlen plazmakoncentráció korrelál a toxicitással és a szisztémás farmakodinámiás hatásokkal.
A ropivakain gyorsan átjut a méhlepényen, és könnyen megteremti az egyensúlyt a megkötött és a szabad frakciók között.
A ropivakain nagymértékben metabolizálódik, főleg aromás hidroxilezéssel. Intravénás beadás után az adag 86% -a ürül a vizelettel, és ennek csak 1% -a vonatkozik a változatlan gyógyszerre. A fő metabolit a 3 -hidroxi -ropivakain, amelynek körülbelül 37% -a kiválasztódik a vizelettel, főleg konjugátum formájában. A 4-hidroxi-ropivakain, az N-dealkilált metabolit (PPX) és a 4-hidroxi-dealkilált vizelettel történő kiválasztása 1-3%. A konjugált és nem konjugált 3-hidroxi-ropivakain koncentrációja csak a plazmában mutatható ki.
Az anyagcsere kép hasonló volt az 1 év feletti gyermekeknél.
A vesefunkció károsodása alig vagy egyáltalán nem befolyásolja a ropivakain farmakokinetikáját. A PPX vese clearance -e szignifikáns korrelációt mutat a kreatinin clearance -szel. A korreláció hiánya az AUC-ban kifejezett teljes expozíció és a kreatinin-clearance között azt jelzi, hogy a teljes PPX-clearance a vesén keresztül történő kiválasztás mellett a nem-vesén keresztül történő eliminációt is magában foglalja. A PPX ropivakainhoz képest csökkent központi idegrendszeri toxicitása miatt a klinikai következmények elhanyagolhatóak rövid távú kezelés esetén. A végstádiumú vesebetegségben szenvedő, dialízisben részesülő betegeket nem vizsgálták.
Nincs bizonyíték a ropivakain in vivo racemizációjára.
Gyermekgyógyászat
A ropivakain farmakokinetikáját egy 192 és 0-12 év közötti gyermekből álló populáció farmakokinetikai adatainak elemzésével jellemeztük.
A kötetlen ropivakain frakció, a PPX metabolit és a kötetlen ropivakain eloszlási térfogata a testtömeg és az életkor függvénye, amíg a májfunkció el nem éri az érettséget, ezután elsősorban a ropivakain nem kötött frakciójának teljes funkcionális clearance -e úgy tűnik, hogy 3 éves korig teljes, a PPX metabolité 1 évvel, a kötetlen ropivakain eloszlási térfogata pedig 2 életévvel.
A nem kötött PPX metabolit eloszlási térfogata kizárólag a testsúlytól függ. Mivel a PPX-nek hosszabb felezési ideje és alacsonyabb clearance-e van, felhalmozódhat az epidurális infúzió során.
A kötetlen ropivakain (Clu) clearance-e 6 hónapos kor felett elérte a felnőttek tartományát. Az 5. táblázatban közölt összes ropivakain (CL) clearance értékét azok nem befolyásolják, az AAG operatív növekedése.
5. táblázat: A gyermekpopuláció elemzéséből származó farmakokinetikai paraméterek becslése
korcsoport szerinti medián testtömeg -WHO adatbázis.
b a kötetlen ropivakain clearance -e
c a kötetlen ropivakain eloszlási térfogata
d a ropivakain teljes clearance -e
és a ropivakain terminális felezési ideje
f a PPX terminális felezési ideje
Az átlagos szimulált maximális, nem kötött plazmakoncentráció (Cumax) egyetlen caudalis blokk után általában magasabb az újszülötteknél, és a maximális kötés nélküli plazmakoncentrációig eltelt idő (tmax) csökken az életkor előrehaladtával (6. táblázat). Az átlagos szimulált, nem kötött plazmakoncentráció az ajánlott dózisú 72 órás folyamatos epidurális infúzió végén magasabb szintet mutatott újszülötteknél, mint csecsemőknél és gyermekeknél. Lásd 4.4 pont.
6. táblázat A nem kötött cumax szimulált átlaga és tartománya egyetlen caudalis blokk után
a Maximális, nem kötött plazmakoncentráció
b A maximális kötés nélküli plazmakoncentráció eléréséhez szükséges idő
c A maximális megfigyelt kötetlen plazmakoncentráció és normalizált dózis
6 hónapos életkorban a folyamatos epidurális infúzió ajánlott adagjának megváltoztatásának töréspontja, a kötetlen ropivakain és a nem kötődő PPX metabolit clearance -e eléri az érett értékek 34% -át, illetve 71% -át. Szisztémás expozíció magasabb csecsemőknél és az 1-6 hónapos csecsemőknél több, mint az idősebb gyermekeknél, ez összefügg a májfunkciók éretlenségével. Ezt azonban részben ellensúlyozza az ajánlott infúziós adag 50% -os csökkentése 6 hónapos kor alatti gyermekeknél. .
A nem kötődő ropivakain és a PPX metabolit plazmakoncentrációinak összegét szimulálva, a farmakokinetikai paraméterek és a populációanalízis változékonysága alapján azt jelzik, hogy egyetlen caudalis blokk esetén az ajánlott adagot 2,7 -szeresére kell növelni fiatalabb csoport és 7,4 -es faktor az 1–10 évesek csoportjában, így a 90% -os megbízhatósági intervallum felső határának előrejelzése eléri a szisztémás toxicitás küszöbét.
A folyamatos epidurális infúzió megfelelő tényezői 1,8 és 3,8.
A kötetlen ropivakain és a PPX metabolit plazmakoncentrációinak összegének szimulációi, a farmakokinetikai paraméterek és a populációanalízisekben való változékonyságuk alapján, azt mutatják, hogy 1 éves és 12 év közötti gyermekeknél egyetlen perifériás idegblokk (dózis) 3 mg / kg, a szabad plazma csúcskoncentráció medián értéke 0,8 óra elteltével 0,0347 mg / l, a toxicitási küszöb tizede (0,34 mg / l). A maximális szabad plazmakoncentráció esetén a 90% -nál nagyobb megbízhatósági intervallum 0,074 mg / l, a toxicitási küszöb egyötöde. Hasonlóképpen a folyamatos perifériás idegblokk esetében (0,6 mg ropivakain / kg 72 órán keresztül), amelyet egyetlen 3 mg / kg előz meg perifériás idegblokk esetén a szabad plazma csúcskoncentráció medián értéke 0,053 mg / l. A maximális szabad plazmakoncentráció 90% -nál nagyobb megbízhatósági intervalluma 0,088 mg / l, a toxicitási küszöb negyede.
05.3 A preklinikai biztonságossági adatok -
A tolerancia, az egyszeri és ismételt dózisú toxicitás, a reproduktív toxicitás, a mutagén potenciál és a helyi toxicitás hagyományos farmakológiai vizsgálatai alapján az emberekre gyakorolt kockázatok nem kerültek kiemelésre, kivéve azokat, amelyek a ropivakain nagy dózisának (például a központi idegrendszeri jelek, beleértve a görcsöket és a kardiotoxicitást).
06.0 GYÓGYSZERÉSZETI INFORMÁCIÓK
06.1 Segédanyagok -
Nátrium-klorid
Sósav
Nátrium-hidroxid
Injekcióhoz való víz.
06.2 Inkompatibilitás "-
A 6.6 pontban felsoroltakon kívül más megoldásokkal való kompatibilitást nem vizsgálták.
Lúgos oldatokban csapadék fordulhat elő, mivel a ropivakain 6,0 feletti pH -értéknél rosszul oldódik.
06.3 Érvényességi idő "-
Fiola (Polyamp):
3 év.
Infúziós zsákok (Polybag):
2 év.
Érvényesség az első felbontás után:
mikrobiológiai szempontból a készítményt azonnal fel kell használni.
Ha ez nem így van, a tárolás körülményei és a használat előtti idő a felhasználó felelőssége, és ezek minden esetben nem haladhatják meg a 24 órát 2–8 ° C közötti hőmérsékleten.
A keverékeket lásd a 6.6 pontban.
06.4 Különleges tárolási előírások -
Legfeljebb 30 ° C -on tárolandó.
A felbontás utáni tárolást lásd a 6.3 pontban.
06.5 A közvetlen csomagolás jellege és a csomagolás tartalma -
Naropin 2 mg / ml
10 ml -es polipropilén injekciós üvegek (Polyamp) 5 és 10 darabos csomagolásban
steril, 10 ml -es polipropilén injekciós üvegek (Polyamp) 5 és 10 db -os steril buborékcsomagolásban
20 ml -es polipropilén injekciós üvegek (Polyamp) 5 és 10 darabos csomagolásban
steril 20 ml -es polipropilén injekciós üvegek (Polyamp) 5 és 10 db steril buborékcsomagolásban
100 ml steril polipropilén tasak (Polybag), 5 db -os steril buborékcsomagolásban
Naropin 7,5 mg / ml
10 ml -es polipropilén injekciós üvegek (Polyamp) 5 és 10 darabos csomagolásban
steril, 10 ml -es polipropilén injekciós üvegek (Polyamp) 5 és 10 db -os steril buborékcsomagolásban
20 ml -es polipropilén injekciós üvegek (Polyamp) 5 és 10 darabos csomagolásban
steril 20 ml -es polipropilén injekciós üvegek (Polyamp) 5 és 10 db steril buborékcsomagolásban.
Naropin 10 mg / ml
10 ml -es polipropilén injekciós üvegek (Polyamp) 5 és 10 darabos csomagolásban
steril, 10 ml -es polipropilén injekciós üvegek (Polyamp) 5 és 10 db -os steril buborékcsomagolásban
20 ml -es polipropilén injekciós üvegek (Polyamp) 5 és 10 darabos csomagolásban
steril 20 ml -es polipropilén injekciós üvegek (Polyamp) 5 és 10 db steril buborékcsomagolásban.
Nem feltétlenül mindegyik kiszerelés kerül kereskedelmi forgalomba.
A polipropilén (Polyamp) injekciós üvegeket kifejezetten a Luer Lock és a Luer fit fecskendőkhöz tervezték.
06.6 Használati és kezelési útmutató -
A Naropin tartósítószer-mentes, és csak egyszer használható. A maradék oldatot meg kell szüntetni.
A bontatlan elsődleges tartályt nem szabad újra sterilizálni. Steril buborékcsomagolást kell választani azokban az esetekben, amikor az injekciós üveg külső felületének sterilitása is szükséges.
A polipropilén zsákokban (Polybag) található Naropin infúziós oldat kémiailag és fizikailag kompatibilis a következő gyógyszerekkel:
* A táblázatban bemutatott koncentrációértékek tartománya szélesebb, mint a klinikai gyakorlatban használt.
A gyógyszert használat előtt szemrevételezéssel meg kell vizsgálni Az oldatot csak akkor szabad használni, ha tiszta, lényegében részecskéktől mentes, és ha a tartály sértetlen.
A keverékek kémiailag és fizikailag 30 napig stabilak, ha 20 és 30 ° C között tárolják, de mikrobiológiai szempontból a keverékeket azonnal fel kell használni. Ha nem ez a helyzet, akkor a használatban lévő tárolási feltételek és a használat előtti idők a felhasználó felelőssége, és ezek minden esetben nem haladhatják meg a 24 órát 2–8 ° C közötti hőmérsékleten.
07.0 A „FORGALOMBA HOZATALI ENGEDÉLY” TULAJDONOSA -
AstraZeneca S.p.A. - Palazzo Ferraris - Via Ludovico il Moro 6 / C - Basiglio (MI) 20080
08.0 A FORGALOMBA HOZATALI ENGEDÉLY SZÁMA -
AIC n. 032248015 "2 mg / ml oldatos injekció / infúzió" 5 db 10 ml -es polipropilén ampulla (Polyamp)
AIC n. 032248027 "2 mg / ml oldatos injekció / infúzió" 5 steril 10 ml -es polipropilén injekciós üveg (Polyamp) steril buborékcsomagolásban
AIC n. 032248041 "2 mg / ml oldatos injekció / infúzió" 5 db 20 ml -es polipropilén ampulla (Polyamp)
AIC n. 032248054 "2 mg / ml oldatos injekció / infúzió" 5 steril, 20 ml -es polipropilén injekciós üveg (Polyamp) steril buborékcsomagolásban
AIC n.032248078 "2 mg / ml oldatos injekció / infúzió" 5 steril 100 ml -es polipropilén zsák (Polybag) steril buborékcsomagolásban
AIC n. 032248092 "7,5 mg / ml oldatos injekció" 5 db 10 ml -es polipropilén ampulla (Polyamp)
AIC n. 032248104 "7,5 mg / ml oldatos injekció" 5 steril, 10 ml -es polipropilén injekciós üveg (Polyamp) steril buborékcsomagolásban
AIC n. 032248128 "7,5 mg / ml oldatos injekció" 5 db 20 ml -es polipropilén ampulla (Polyamp)
AIC n. 032248130 "7,5 mg / ml oldatos injekció" 5 steril, 20 ml -es polipropilén injekciós üveg (Polyamp) steril buborékcsomagolásban
AIC n. 032248155 "10 mg / ml oldatos injekció" 5 db 10 ml -es polipropilén ampulla (Polyamp)
AIC n. 032248167 "10 mg / ml oldatos injekció" 5 steril 10 ml -es polipropilén injekciós üveg (Polyamp) steril buborékcsomagolásban
AIC n. 032248181 "10 mg / ml oldatos injekció" 5 db 20 ml -es polipropilén ampulla (Polyamp)
AIC n. 032248193 "10 mg / ml oldatos injekció" 5 steril, 20 ml -es polipropilén injekciós üveg (Polyamp) steril buborékcsomagolásban
09.0 AZ ELSŐ ENGEDÉLYZÉS ÉS A JÓVÁHAGYÁS MEGÚJÍTÁSÁNAK DÁTUMA -
Az első engedély kiadásának dátuma: 1996.10.30
Az utolsó megújítás dátuma: 2009.11.13
10.0 A SZÖVEG FELÜLVIZSGÁLÁSÁNAK DÁTUMA -
2016. szeptember 08