Hatóanyagok: Ondansetron
Ondansetron Mylan Generics 4 mg filmtabletta
Ondansetron Mylan Generics 8 mg filmtabletta
Miért használják az Ondansetron - általános gyógyszert? Mire való?
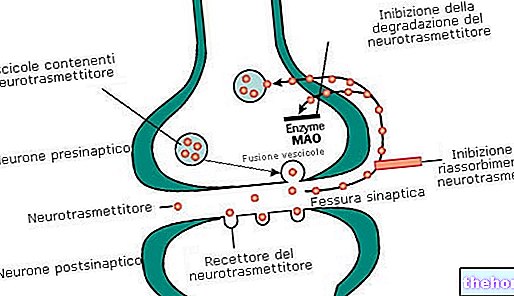
Az Ondansetron Mylan Generics az antiemetikus vagy hányásgátló gyógyszerek csoportjába tartozik. Az ondanszetron gátolja az agyban a szerotonin neurotranszmitter hatását, a szerotonin hányingert és hányást okoz.
Az Ondansetron Mylan Generics felnőtteknél a következőkre alkalmazható:
- a kemoterápia vagy a sugárkezelés okozta hányinger és hányás szabályozása
- a műtétet követő hányinger és hányás megelőzése
Az Ondansetron Mylan Generics gyermekeknél a következőkre alkalmazható:
- a kemoterápia által okozott hányinger és hányás ellenőrzése 6 hónapos és idősebb gyermekeknél
- a műtétet követő hányinger és hányás megelőzése 1 hónapos és idősebb gyermekeknél.
Kérdezze meg kezelőorvosát, nővérét vagy gyógyszerészét, ha további magyarázatokat szeretne kapni ezekről a felhasználásokról.
Ellenjavallatok, amikor az Ondansetron - Generic Drug nem alkalmazható
Ne szedje az Ondansetron Mylan Generics -et:
- ha allergiás az ondanszetronra vagy a gyógyszer (6. pontban felsorolt) egyéb összetevőjére.
- ha allergiás a szelektív szerotonin (5-HT3) receptor antagonisták csoportjába tartozó más hányás elleni gyógyszerekre (pl. granisetron vagy dolasetron), mivel ezekben az esetekben allergiás lehet az ondanszetronra is
- ha apomorfint szed (Parkinson -kór kezelésére használják)
Ha nem biztos benne, beszéljen kezelőorvosával, ápolójával vagy gyógyszerészével az Ondansetron Mylan Generics szedése előtt.
Az alkalmazással kapcsolatos óvintézkedések Mit kell tudnia a Generic Ondansetron szedése előtt?
Az Ondansetron Mylan Generics szedése előtt beszéljen kezelőorvosával, gyógyszerészével vagy a nővérrel:
- - ha valaha szívproblémái vagy szívritmus -változásai voltak (aritmiák vagy szívvezetési zavarok)
- - ha problémái vannak a vérében lévő sók, például a kálium, a nátrium és a magnézium szintjével
- ha bélproblémái vannak, például bélelzáródás vagy súlyos székrekedésben szenved
- - ha Ön adenoidjait vagy manduláit eltávolítja vagy nemrégiben eltávolította, mivel ezzel a gyógyszerrel elfedheti a belső vérzés tüneteit
- ha Ön gyermek, akinek testfelülete kisebb, mint 0,6 m2
- ha májproblémái vannak.
Gyermekek és serdülők
Ezt a gyógyszert nem szabad gyermekeknek adni gyomorműtét utáni hányinger és hányás megelőzésére.
Ha nem biztos abban, hogy a fentiek bármelyike vonatkozik -e Önre, beszéljen kezelőorvosával, ápolójával vagy gyógyszerészével az Ondansetron Mylan Generics szedése előtt.
Kölcsönhatások Mely gyógyszerek vagy élelmiszerek módosíthatják az Ondansetron - Generic Drug hatását
Feltétlenül tájékoztassa kezelőorvosát, nővérét vagy gyógyszerészét a jelenleg vagy nemrégiben szedett, valamint szedni tervezett egyéb gyógyszereiről. Ide tartoznak a vény nélkül kapható gyógyszerek vagy gyógynövénykészítmények is. Ez azért van így, mert az Ondansetron Mylan Generics hatással lehet másokra. Gyógyszerek vagy egyéb gyógyszerek befolyásolja az Ondansetron Mylan Generics -et.
Különösen tájékoztassa kezelőorvosát, nővérét vagy gyógyszerészét, ha az alábbi gyógyszerek bármelyikét szedi:
- apomorfin (a Parkinson -kór kezelésére használt gyógyszer), mivel jelentős vérnyomáscsökkenésről és eszméletvesztésről számoltak be, amikor az apomorfint ondanszetronnal - fenitoinnal vagy karbamazepinnel (epilepszia kezelésére használt gyógyszerek) együtt alkalmazták, ami csökkentheti az ondanszetron hatását
- rifampicin (antibiotikum fertőzés, például tuberkulózis kezelésére), amely csökkentheti az ondanszetron hatását
- antibiotikumok, például eritromicin vagy ketokonazol - antiaritmiás gyógyszerek, például amiodaron (szabálytalan szívverés kezelésére használják)
- béta -blokkolók, például atenolol vagy timolol (bizonyos szív- vagy szemproblémák, szorongás vagy migrén kezelésére szolgálnak) - tramadol (fájdalomcsillapító), amely csökkenthető az ondansetron Mylan Generics segítségével
- rákellenes gyógyszerek (különösen antraciklinek és trasztuzumab)
- a depresszió kezelésére használt gyógyszerek bizonyos típusai, amelyek SSRI-k (szelektív szerotonin-újrafelvétel-gátlók) vagy SNRI-k (szerotonin- és norepinefrin-visszavétel-gátlók) néven ismertek, mivel ezek ondanszetronnal együtt alkalmazva szerotonin-szindrómát, potenciálisan életveszélyes reakciót okozhatnak. A szerotonin -szindróma tünetei a következők kombinációi lehetnek: hányinger (hányinger), hányinger, izgatottság, hasmenés, magas hőmérséklet, emelkedett vérnyomás, túlzott izzadás, gyors szívverés, hallucinációk, koordinációvesztés, hiperaktív reflexek és kóma.
Ha nem biztos abban, hogy a fentiek bármelyike vonatkozik -e Önre, beszéljen kezelőorvosával, ápolójával vagy gyógyszerészével az Ondansetron Mylan Generics szedése előtt.
Figyelmeztetések Fontos tudni, hogy:
Terhesség és szoptatás
Az Ondansetron Mylan Generics alkalmazása terhesség alatt nem ajánlott.Az Ondansetron Mylan Generics szedése előtt kérje ki kezelőorvosa vagy gyógyszerésze tanácsát, ha terhes vagy teherbe eshet.
Az Ondansetron Mylan Generics kezelés alatt ne szoptasson. Ez azért van, mert ez a gyógyszer átjuthat az anyatejbe. Kérjen tanácsot orvosától, gyógyszerészétől vagy szülésznőjétől.
Ha Ön terhes vagy szoptat, illetve ha fennáll Önnél a terhesség lehetősége vagy gyermeket szeretne, a gyógyszer alkalmazása előtt beszéljen kezelőorvosával vagy gyógyszerészével.
A készítmény hatásai a gépjárművezetéshez és gépek kezeléséhez szükséges képességekre
Az Ondansetron Mylan Generics nem befolyásolja a gépjárművezetéshez és gépek kezeléséhez szükséges képességeket.
Az Ondansetron Mylan Generics laktózt tartalmaz
Ha kezelőorvosa korábban már figyelmeztette Önt, hogy bizonyos cukrokra érzékeny, keresse fel orvosát, mielőtt elkezdi szedni ezt a gyógyszert.
Adagolás, az alkalmazás módja és ideje Az Ondansetron - Generic Drug használata: Adagolás
Ezt a gyógyszert mindig az orvos vagy a gyógyszerész által elmondottaknak megfelelően szedje. Kérdezze meg kezelőorvosát, nővérét vagy gyógyszerészét, ha nem biztos benne. Az Ön által előírt adag attól függ, hogy milyen kezelést kap.
Az ajánlott adag:
Kemoterápiával vagy sugárkezeléssel kapcsolatos hányinger és hányás kezelése és megelőzése a rák kezelésére
Felnőttek
A kezelés előtt egy vagy két órával vegyen be 8 mg ondanszetront, majd 12 órával később 8 mg ondanszetront. Naponta kétszer 8 mg -os ondanszetron adag vehető be a kezelés után legfeljebb 5 napig. Kezelőorvosa dönthet úgy, hogy az első adagot injekció formájában adja be közvetlenül a kezelés előtt.
Alkalmazása gyermekeknél (6 hónapos kortól és idősebbeknél) és serdülőknél
Az adag egyéni, és függ a gyermek súlyától, méretétől / testfelületétől, azonban a teljes napi adag nem haladhatja meg a 32 mg -ot. Kezelőorvosa határozza meg a gyermeke adagját. További információért lásd a címkét. Az ajánlott adag gyermek számára 8 mg naponta kétszer, testsúlytól függően. Ez legfeljebb 5 napig adható.
Idős államporgárok
Az ondanszetron jól tolerálható a 65 évesnél idősebb betegeknél, akik kemoterápiát kapnak, nincs szükség az adag módosítására.
A műtét utáni hányinger és hányás megelőzése és kezelése
Felnőttek
A szokásos adag 16 mg ondanszetron egy órával a műtét előtt vagy 8 mg ondanszetron egy órával a műtét előtt, majd 2 8 mg -os adag 8 órás időközönként.
Alkalmazása gyermekeknél (1 hónaposnál idősebb) és serdülőknél
Ajánlott az ondanszetront injekció formájában beadni A gyógyszer egyéb gyógyszerformái alkalmasabbak gyermekek kezelésére; kérdezze meg orvosát vagy gyógyszerészét.
Idős államporgárok
Korlátozott tapasztalat áll rendelkezésre az ondanszetron időskori alkalmazásával kapcsolatban, azonban az ondanszetront jól tolerálják azok a 65 évnél idősebb betegek, akik kemoterápiát kapnak (lásd fent).
Vesebetegségben szenvedő betegek vagy a spartein/ debrisokin alacsony metabolizmusa esetén
Nincs szükség az adag módosítására vesebetegségben szenvedő betegeknél vagy olyan betegeknél, akik nem képesek metabolizálni a sparteint/ debrizokint.
Májbetegségben szenvedő betegek
A teljes napi adag nem haladhatja meg a napi 8 mg -ot, ha közepesen súlyos vagy súlyos májbetegsége van.
Ha továbbra is hányingere van, forduljon orvosához, gyógyszerészéhez vagy a nővérhez.
Az alkalmazás módja:
- A tablettákat egy pohár vízzel kell lenyelni
- Az Ondasetron injekció formájában is kapható.
Ha elfelejtette bevenni az Ondansetron Mylan Generics -et
- Ha elfelejtett bevenni egy adagot, és hányingere vagy hányása van, vegye be, amint eszébe jut. Ezt követően vegye be a következő tablettát a szokásos időben (a címkén látható módon). Ha azonban már itt az ideje a következő adagnak, hagyja ki az elfelejtett adagot, és folytassa a szokásos módon.
Ne vegyen be kétszeres adagot a kihagyott adag pótlására.
- Ha kihagyott egy adagot, de nem émelygett, vegye be a következő adagot a címkén látható módon.
Ne vegyen be kétszeres adagot a kihagyott adag pótlására.
Ha idő előtt abbahagyja az Ondansetron Mylan Generics szedését
Ne hagyja abba a gyógyszer szedését, hacsak kezelőorvosa nem mondja. A tünetek kiújulhatnak.
Túladagolás Mi a teendő, ha túl sok Ondansetron - Generic Drug -t vett be?
Ha Ön vagy gyermeke az előírtnál több Ondansetron Mylan Generics -et szed
Azonnal forduljon orvosához vagy a legközelebbi sürgősségi osztályhoz. Vigye magával a doboz gyógyszert és a megmaradt tablettákat. Az ondansetron túladagolásáról korlátozott információ áll rendelkezésre. A túladagolás jelei a következők: látási problémák, súlyos székrekedés, alacsony vérnyomás, amely szédülést vagy ájulást és szabálytalan szívritmust okozhat.
Mellékhatások Melyek az Ondansetron - Generic Drug mellékhatásai
Mint minden gyógyszer, így ez a gyógyszer is okozhat mellékhatásokat, amelyek azonban nem mindenkinél jelentkeznek.
A gyógyszer szedése során a következő súlyos mellékhatások jelentkezhetnek: Ha ezen mellékhatások bármelyikét észleli, hagyja abba a gyógyszer szedését, és azonnal forduljon orvoshoz, vagy menjen a legközelebbi kórházba.
Ritka (1000 -ből legfeljebb 1 beteget érinthet)
- ha allergiás reakciója van, a következők a következők:
- hirtelen zihálás és mellkasi fájdalom vagy mellkasi szorítás
- a szemhéjak, az arc, az ajkak, a száj vagy a nyelv duzzanata
- kiütés
- vörös foltok vagy csomók a bőr alatt (csalánkiütés) a test bármely pontján
- összeomlás
Nem gyakori (100 beteg közül legfeljebb 1 beteget érinthet)
- akaratlan szemmozgások (szemészeti válság)
Egyéb lehetséges mellékhatások
Nagyon gyakori (10 beteg közül több mint 1 beteget érinthet):
- fejfájás.
Gyakori (10 beteg közül legfeljebb 1 beteget érinthet):
- székrekedés
- melegség vagy bőrpír
Nem gyakori (100 beteg közül legfeljebb 1 beteget érinthet):
- zokogás
- alacsony vérnyomás, ami ájulást vagy szédülést okozhat
- szabálytalan szívverés vagy lassú szívverés
- mellkasi fájdalom EKG változásokkal vagy anélkül
- görcsök, szokatlan testmozgások vagy remegés
- izomgörcsök
- a májműködés megváltozását mutató vérvizsgálatok változásai (gyakrabban ciszplatin kemoterápiában részesülő betegeknél)
Ritka (1000 -ből legfeljebb 1 beteget érinthet):
- átmeneti homályos látás
- szívritmuszavarok, amelyeket QT -intervallum meghosszabbításnak neveznek (az EKG -n látható elektromos jelek késleltetett vezetése, a szív elektromos felvétele). Néhány embernél ez potenciálisan súlyos szívbetegséghez vezethet, amely torsades de pointes néven ismert. nagyon gyors szívverést okoz, ami eszméletvesztést okoz.
Nagyon ritka (10 000 -ből legfeljebb 1 beteget érinthet):
- rossz látás vagy átmeneti látásvesztés, amely általában 20 percen belül elmúlik
- kórosan gyors szívverés
Nemkívánatos hatások gyermekeknél és serdülőknél
A gyermekeknél és serdülőknél jelentett mellékhatások nagyon hasonlóak voltak a felnőtteknél észlelt és a fenti listában jelentett mellékhatásokhoz.
Mellékhatások bejelentése
Ha Önnél bármilyen mellékhatás jelentkezik, tájékoztassa erről kezelőorvosát, gyógyszerészét vagy a gondozását végző egészségügyi szakembert. Ez a betegtájékoztatóban fel nem sorolt bármilyen lehetséges mellékhatásra is vonatkozik. A mellékhatásokat közvetlenül a hatóság részére is bejelentheti a www.agenziafarmaco.gov. It / it webhelyen. / felelős. A mellékhatások bejelentésével Ön is hozzájárulhat ahhoz, hogy minél több információ álljon rendelkezésre a gyógyszer biztonságosságáról.
Lejárat és megőrzés
A gyógyszer gyermekektől elzárva tartandó!
Ez a gyógyszer nem igényel különleges tárolási körülményeket. A buborékcsomagoláson és a dobozon feltüntetett lejárati idő (EXP) után ne alkalmazza ezt a gyógyszert. A lejárati idő az adott hónap utolsó napjára vonatkozik.
Semmilyen gyógyszert ne dobjon a szennyvízbe vagy a háztartási hulladékba. Kérdezze meg gyógyszerészét, hogy mit tegyen a már nem használt gyógyszereivel. Ez elősegíti a környezet védelmét.
Határidő "> Egyéb információ
Mit tartalmaz az Ondansetron Mylan Generics
- A készítmény hatóanyaga az ondanszetron.
Minden tabletta 4 mg vagy 8 mg ondanszetron hatóanyagot tartalmaz (hidroklorid -dihidrát formájában)
- Egyéb összetevők: laktóz -monohidrát (lásd 2. pont "Az Ondansetron Mylan Generics laktóz -monohidrátot tartalmaz"), mikrokristályos cellulóz, előzselatinizált kukoricakeményítő és magnézium -sztearát.
A bevonat hipromellózt, titán -dioxidot (E 171), hidroxi -propil -cellulózt, makrogolt, szorbitán -oleátot, szorbinsavat, vanillint, kinolin -sárgát (E 104) tartalmaz.
Milyen az Ondansetron Mylan Generics külleme és mit tartalmaz a csomagolás?
4 mg tabletta: Halványsárga, kerek és mindkét oldalán domború filmtabletta, egyik oldalán mélynyomású "41" jelzéssel.
8 mg tabletta: Halványsárga, kerek és mindkét oldalán domború filmtabletta, egyik oldalán mélynyomású "42" jelzéssel.
Buborékcsomagolás:
4 mg: 3, 6, 9, 10, 14, 15, 20, 30, 40, 50, 60, 90, 100, 200, 300, 500 filmtabletta.
8 mg: 3, 6, 9, 10, 14, 15, 20, 30, 40, 50, 60, 90, 100, 200, 300, 500 filmtabletta.
Nem feltétlenül mindegyik kiszerelés kerül kereskedelmi forgalomba.
Forrás betegtájékoztató: AIFA (Olasz Gyógyszerügynökség). A tartalom 2016 januárjában jelent meg. A jelenlévő információk nem feltétlenül naprakészek.
A legfrissebb verzióhoz való hozzáféréshez ajánlatos az AIFA (Olasz Gyógyszerügynökség) webhelyét elérni. Jogi nyilatkozat és hasznos információk.
01.0 A GYÓGYSZER MEGNEVEZÉSE -
FILMBE VONATT ONDANSETRONE MYLAN GENERICS TABLETTA
02.0 MINŐSÉGI ÉS MENNYISÉGI ÖSSZETÉTEL -
Ondansetron Mylan Generics 4 mg filmtabletta.
Minden filmtabletta 4 mg ondanszetront tartalmaz (ondanszetron-hidroklorid-dihidrát formájában).
Ismert hatású segédanyagok: minden tabletta 84,50 mg laktóz -monohidrátot tartalmaz.
Ondansetron Mylan Generics 8 mg filmtabletta.
Minden filmtabletta 8 mg ondanszetront tartalmaz (ondanszetron-hidroklorid-dihidrát formájában).
Ismert hatású segédanyagok: minden tabletta 169,00 mg laktóz -monohidrátot tartalmaz.
A segédanyagok teljes listáját lásd a 6.1 pontban.
03.0 GYÓGYSZERFORMA -
Filmtabletta.
Minden 4 mg-os filmtabletta halványsárga, kerek, mindkét oldalán domború felületű, egyik oldalán "41" jelzéssel.
Minden 8 mg-os filmtabletta halványsárga, kerek, mindkét oldalán domború felületű, egyik oldalán "42" jelzéssel.
04.0 KLINIKAI INFORMÁCIÓK -
04.1 Terápiás javallatok -
Felnőttek
Az Ondansetron a citotoxikus kemoterápia és sugárterápia okozta hányinger és hányás kezelésére, valamint a posztoperatív hányinger és hányás (PONV) megelőzésére és kezelésére javallt.
Gyermekpopuláció
Az ondanszetron kemoterápia által kiváltott hányinger és hányás (CINV) kezelésére javallt ≥ 6 hónapos gyermekeknél, valamint a műtét utáni hányinger és hányás (PONV) megelőzésére és kezelésére ≥ 1 hónapos gyermekeknél.
04.2 Adagolás és alkalmazás
Adagolás
A kemoterápia és a sugárkezelés hányingert és hányást váltott ki.
Felnőttek
A rák kezelésének hányásgátló potenciálja az alkalmazott kemoterápia és sugárkezelés dózisaitól és kombinációitól függően változik. Az ondanszetron adagolási módjának és adagjának rugalmasnak kell lennie, és az alábbiak szerint kell kiválasztani.
Emetogén kemoterápia és sugárkezelés
Az emetogén kemoterápiában vagy sugárkezelésben részesülő betegeknél az ondanszetron orálisan vagy intravénásan is beadható.
A legtöbb betegnél, akik emetogén kemoterápiát vagy sugárkezelést kapnak, az ondanszetront kezdetben intravénásan kell beadni közvetlenül a kezelés előtt, majd 8 mg szájon át 12 óránként.
Orális adagolás: 8 mg 1-2 órával a kezelés előtt, majd 8 mg 12 óra múlva.
Az első 24 óra utáni késleltetett vagy elhúzódó hányás elleni védelem érdekében az orális ondanszetron -kezelést a kezelés után legfeljebb 5 napig folytatni kell.
Erősen emetogén kemoterápia
Azoknál a betegeknél, akik erősen hányásgátló kemoterápiát kapnak, pl. nagy dózisú ciszplatin, ondanszetron intravénásan adható be.
Az első 24 óra utáni késleltetett vagy elhúzódó hányás elleni védelem érdekében az orális ondanszetron -kezelést a kezelés után legfeljebb 5 napig folytatni kell.
Az ajánlott adag orális adagolásra naponta kétszer 8 mg.
Gyermekpopuláció
CINV ≥ 6 hónapos gyermekeknél és serdülőknél:
A CINV dózisa a testfelület (BSA) vagy a súly alapján számítható ki - lásd alább. A súlyalapú adagolás nagyobb napi összdózist eredményez, mint a BSA-alapú adag (lásd 4.4 és 5.1 pont).
Az Ondansetron Mylan Generics infúziót 5% -os dextrózban vagy 0,9% -os nátrium -kloridban vagy más hasonló infúziós folyadékban kell hígítani, és legalább 15 percig intravénásan kell beadni.
Nincsenek ellenőrzött klinikai vizsgálatokból származó adatok az Ondasetron Mylan Generics alkalmazásáról a kemoterápia által okozott késleltetett vagy elhúzódó hányinger és hányás megelőzésére. Nincsenek ellenőrzött klinikai vizsgálatokból származó adatok az Ondasetron Mylan Generics hányinger és hányás elleni alkalmazásáról. gyermekek sugárkezelésével.
A BSA által kiszámított dózis
Az Ondasetron Mylan Generics -et közvetlenül a kemoterápia előtt kell beadni, egyetlen intravénás 5 mg / m² dózisban. Az intravénás adag nem haladhatja meg a 8 mg -ot.
Az orális adag 12 órával később kezdődhet, és legfeljebb 5 napig folytatható (lásd az alábbi 1. táblázatot).
A teljes napi adag nem haladhatja meg a felnőttek 32 mg -os adagját.
1. táblázat: BSA -alapú dózis kemoterápiához - ≥ 6 hónapos gyermekek és serdülők
a: az intravénás adag nem haladhatja meg a 8 mg -ot.
b: A teljes napi adag nem haladhatja meg a felnőttek 32 mg -os adagját.
Adag a testtömegre számítva
A súlyalapú dózisok magasabb teljes napi adagot eredményeznek, mint a BSA-alapú dózis-lásd 4.4 és 5.1 pont.
Az Ondasetron Mylan Generics -et közvetlenül a kemoterápia előtt kell beadni, egyetlen intravénás 0,15 mg / kg dózisban. Az intravénás adag nem haladhatja meg a 8 mg -ot.
Két további intravénás adag adható 4 órás időközönként.
A teljes napi adag nem haladhatja meg a felnőttek 32 mg -os adagját.
Az orális adag 12 órával később kezdődhet, és legfeljebb 5 napig folytatható (lásd 2. táblázat).
2. táblázat: Súlyalapú dózis kemoterápiához - ≥ 6 hónapos gyermekek és serdülők
a: az intravénás adag nem haladhatja meg a 8 mg -ot.
b: A teljes napi adag nem haladhatja meg a felnőttek 32 mg -os adagját.
Idős államporgárok
A 65 év feletti betegeknél az ondanszetron jól tolerálható, és nincs szükség az adagolás, gyakoriság vagy beadás módosítására.
Lásd még "Különleges populációk".
Műtét utáni hányinger és hányás (PONV)
Felnőttek
A PONV megelőzése
A PONV megelőzésére az ondanszetron orálisan vagy intravénás injekció formájában adható be.
Orális alkalmazás:
- 16 mg egy órával az érzéstelenítés előtt
- alternatív módon 8 mg egy órával az érzéstelenítés előtt, majd 2 további 8 mg -os adag 8 órás időközönként.
PONV kezelés a helyén
Intravénás adagolás javasolt a meglévő PONV kezelésére.
Gyermekpopuláció
Műtét utáni hányinger és hányás ≥ 1 hónapos gyermekeknél és serdülőknél
Orális készítmények
Nem végeztek vizsgálatokat az orálisan beadott ondanszetron alkalmazásával a műtét utáni hányinger és hányás megelőzésére vagy kezelésére; erre a célra lassú intravénás injekció ajánlott.
Injekció:
A PONV megelőzésére gyermekkorú betegeknél általános érzéstelenítésben végzett műtéttel egyszeri ondanszetron adag beadható lassú intravénás injekcióval (legalább 30 másodperc) 0,1 mg / kg és legfeljebb 4 mg dózisban. , az érzéstelenítés indukciója előtt vagy után.
A PONV műtét utáni kezelésére olyan gyermekeknél, akiknél általános érzéstelenítésben végzett műtétet végeztek, az Ondansetron Mylan Generics egyszeri adagja beadható lassú intravénás injekcióval (legalább 30 másodpercig), legfeljebb 0,1 mg / kg dózisban 4 mg.
Nincsenek adatok az ondansetron Mylan Generics alkalmazásáról a posztoperatív hányás kezelésére 2 év alatti gyermekeknél.
Idős államporgárok
Az ondanszetron idős betegeknél a műtét utáni hányinger és hányás (PONV) megelőzésére és kezelésére vonatkozó tapasztalatai korlátozottak, azonban az ondanszetront jól tolerálják azok a 65 év feletti betegek, akik kemoterápiát kapnak.
Lásd még "Különleges populációk".
Különleges populációk
Vesekárosodásban szenvedő betegek
Nincs szükség napi dózismódosításra, gyakoriságra vagy beadási módra.
Májkárosodásban szenvedő betegek
Közepes vagy súlyos májkárosodásban szenvedő betegeknél az ondanszetron clearance-e jelentősen csökken, és a szérum felezési ideje jelentősen meghosszabbodik. Ilyen betegeknél a napi 8 mg -os teljes dózist nem szabad túllépni, ezért parenterális vagy orális adagolás javasolt.
Spartein/ debrizokin metabolizmus zavara esetén szenvedő betegek
Az ondanszetron eliminációs felezési ideje nem változik azoknál a betegeknél, akik a szpartein és a debriszokin gyenge metabolizálói közé tartoznak. Következésképpen ezeknél a betegeknél az ismételt dózisok a gyógyszer expozíciójának szintjét nem különbözik az általános populációétól. Nincs szükség a napi adag vagy az adagolás gyakoriságának megváltoztatására.
Az alkalmazás módja
Szájon át történő alkalmazás.
04.3 Ellenjavallatok -
A készítmény hatóanyagával vagy a 6.1 pontban felsorolt bármely segédanyagával szembeni túlérzékenység.
Túlérzékenység más szelektív 5-HT3 receptor antagonistákkal (pl. Granisetron, dolasetron) szemben.
Az apomorfin egyidejű alkalmazása (lásd 4.5 pont).
04.4 Különleges figyelmeztetések és a használattal kapcsolatos óvintézkedések -
Túlérzékenységi reakciókat jelentettek olyan betegeknél, akik túlérzékenységet mutattak más szelektív 5HT3 receptor antagonistákkal szemben.
A légzőszervi eseményeket tünetileg kell kezelni, és az orvosoknak különös figyelmet kell fordítaniuk rájuk, mint a túlérzékenységi reakciók előfutáraira.
QT -megnyúlás
Az ondanszetron dózisfüggően meghosszabbítja a QT intervallumot (lásd 5.1 pont). Ezenkívül a forgalomba hozatalt követően beszámoltak torsade de pointesról ondanszetron-kezelésben részesülő betegeknél. Kerülje az ondanszetron alkalmazását veleszületett hosszú QT -szindrómában szenvedő betegeknél. Az ondanszetront óvatosan kell alkalmazni azoknál a betegeknél, akiknél a QTc -intervallum megnyúlása jelentkezik, vagy fennállhat, beleértve azokat a betegeket, akiknél elektrolit -zavarok, pangásos szívelégtelenség, bradiaritmiák, ritmuszavarok vagy vezetési zavarok fordulnak elő, vagy antiaritmiás szerekkel, béta-adrenerg blokkoló szerekkel vagy más gyógyszerekkel kezelt betegek, akik a QT-intervallum megnyúlásához vagy elektrolit-rendellenességekhez vezetnek. Óvatosan kell eljárni, ha az Ondansetron Mylan Generics -et egyidejű érzéstelenítésben szenvedő szívbetegeknek adják.
A hypokalaemiát és a hipomagnesémiát az ondanszetron beadása előtt korrigálni kell.
A forgalomba hozatalt követően beszámoltak szerotonin-szindrómás betegekről (beleértve a megváltozott mentális állapotot, autonóm instabilitást és neuromuszkuláris rendellenességeket) az ondanszetron és más szerotoninerg gyógyszerek (beleértve a szelektív szerotonin-újrafelvétel-gátlókat (SSRI-ket)) és a norepinefrin és szerotonin-újrafelvétel-gátlók egyidejű alkalmazása után SNRI -k).) Ha az ondanszetron és más szerotoninerg gyógyszerek egyidejű kezelése klinikailag indokolt, a betegek megfelelő monitorozása javasolt.
Mivel az ondanszetronról ismert, hogy növeli a vastagbélben az áthaladási időt, a szubakut bélelzáródás jeleit mutató betegeket a beadás után ellenőrizni kell.
Az ondanszetron nem javallott hasi műtétet követő gyermekek posztoperatív hányingerének és hányásának megelőzésére és kezelésére.
Adeno-tonsillar műtéten átesett betegeknél a hányinger és hányás megelőzése ondanszetronnal elfedheti az okkult vérzést, ezért az ilyen betegeket az ondanszetron beadása után gondosan figyelemmel kell kísérni.
Az Ondansetron Mylan Generics -et óvatosan kell alkalmazni májkárosodásban szenvedő betegeknél.
Az Ondansetron Mylan Generics filmtabletta nem alkalmazható 0,6 m²-nél kisebb testfelületű gyermekeknél.
Gyermekpopuláció
Az ondanszetront hepatotoxikus kemoterápiás szerekkel együtt szedő gyermekgyógyászati betegeket gondosan ellenőrizni kell májkárosodás szempontjából.
Kemoterápia okozta hányinger és hányás (CINV)
Ha az adagot tömeg (mg / kg) alapján számítják ki, és ha 3 adagot adnak be 4 órás időközönként, akkor a teljes napi dózis magasabb lesz, mint ha egyetlen 5 mg / m² dózist adnak, amit egy orális adag követ. E két különböző adagolási rend összehasonlító hatékonyságát klinikai vizsgálatok nem igazolták.
A kölcsönös megfeleltetési vizsgálatok azt mutatják, hogy "mindkét terápia esetében hasonló a hatékonyság (lásd 5.1 pont).
Ismert hatású segédanyagok
Az Ondansetron Mylan Generics laktóz -monohidrátot tartalmaz. Ritka örökletes galaktóz intoleranciában, lapp-laktáz elégtelenségben vagy glükóz-galaktóz felszívódási zavarban szenvedő betegek nem szedhetik ezt a gyógyszert.
04.5 Kölcsönhatások más gyógyszerekkel és egyéb interakciók -
Nincs bizonyíték arra, hogy az ondanszetron más, gyakran együtt alkalmazott gyógyszerek metabolizmusát indukálja vagy gátolja. Speciális vizsgálatok kimutatták, hogy nincs kölcsönhatás, ha az ondanszetront alkohollal, temazepámmal, furoszemiddel, alfentanillal, tramadollal, morfinnal, lidokainnal, tiopentállal vagy propofol.
Az ondanszetront több máj citokróm P-450 enzim metabolizálja: CYP3A4, CYP2D6 és CYP1A2. A CYP2D6 genetikai hiánya), általában más enzimek kompenzálják, és kismértékben vagy egyáltalán nem okoz jelentős változásokat az ondanszetron és az előírt dózisok teljes clearance-ében .
Az ondanszetron QT -intervallumot meghosszabbító gyógyszerekkel történő alkalmazása a kiegészítő QT -intervallum meghosszabbodását okozhatja. Az ondanszetron egyidejű alkalmazása kardiotoxikus gyógyszerekkel (pl. Antraciklinekkel, például doxorubicinnel, daunorubicinnel vagy trasztuzumabbal), antibiotikumokkal (például eritromicin vagy ketokonazol), antiaritmiás szerekkel ( amiodaron) és a béta-blokkolók (például atenolol vagy timolol) növelhetik az aritmia kockázatát (lásd 4.4 pont).
A forgalomba hozatalt követően beszámoltak szerotonin-szindrómás betegekről (beleértve a megváltozott mentális állapotot, autonóm instabilitást és neuromuszkuláris rendellenességeket) az ondanszetron és más szerotoninerg gyógyszerek (beleértve az SSRI-ket és SNRI-ket) egyidejű alkalmazása után. (Lásd 4.4 pont)
Apomorfin: Az ondansetron apomorfin -hidrokloriddal történő együttes adásakor jelentkező mély hypotensióról és eszméletvesztésről szóló jelentések alapján az apomorfin egyidejű alkalmazása ellenjavallt.
Fenitoin, karbamazepin és rifampicin: Erős CYP3A4 induktorokkal (pl. Fenitoinnal, karbamazepinnel és rifampicinnel) kezelt betegeknél az ondanszetron orális clearance -e nő, és az ondanszetron vérkoncentrációja csökken.
Tramadol: Kis vizsgálatok adatai azt mutatják, hogy az ondanszetron csökkentheti a tramadol fájdalomcsillapító hatását.
04.6 Terhesség és szoptatás -
Terhesség
Az ondasetron biztonságosságát terhes nőknél nem igazolták.
A kísérleti állatkísérletek értékelése nem mutat közvetlen vagy közvetett káros hatásokat az embrió, a magzat, a terhesség, valamint a peri- és postnatális fejlődés tekintetében, férfiak esetében az ondasetron alkalmazása terhesség alatt nem ajánlott.
Etetési idő
Tanulmányok kimutatták, hogy az ondanszetron kiválasztódik a laktáló állatok anyatejébe (lásd 5.3 pont), ezért ajánlott, hogy az ondanszetronnal kezelt anyák ne szoptassanak.
04.7 Hatások a gépjárművezetéshez és gépek kezeléséhez szükséges képességekre -
A pszichomotoros tesztek során az ondanszetron nincs hatással a teljesítményre és nem okoz szedációt, az ondanszetron farmakológiája alapján ezekre a tevékenységekre nem várható káros hatás.
04.8 Nemkívánatos hatások -
A mellékhatásokat az alábbiakban soroljuk fel szervrendszerek és gyakoriság szerint.
A gyakoriságot a következőképpen határozzák meg:
Nagyon gyakori: (≥1 / 10)
Gyakori: (≥ 1/100 év
Nem gyakori: (≥1 / 1000 y
Ritka: (≥1 / 10 000 éves
Nagyon ritka: (
Nem ismert: (a gyakoriság a rendelkezésre álló adatokból nem becsülhető meg)
Nagyon gyakori, gyakori és nem gyakori események a klinikai vizsgálatok során általában meghatározott események. Ritka és nagyon ritka események azok az események, amelyeket általában spontán jelentések határoznak meg a forgalomba hozatalt követő szakaszban.
A következő gyakoriságokat az ondanszetron szokásos ajánlott dózisaival becsüljük az indikációk és a készítmény alapján.
¹ Megfigyelték a tartós klinikai következmények végleges bizonyítéka nélkül
² A legtöbb bejelentett vakság 20 perc alatt megszűnt. Sok beteget kemoterápiás szerekkel, köztük ciszplatinnal kezeltek. Néhány átmeneti vakság esetét kortikális eredetűnek jelentették.
³ Ezeket az eseteket gyakran figyelték meg ciszplatin kemoterápiában részesülő betegeknél.
Gyermekpopuláció
A nemkívánatos események profilja gyermekeknél és serdülőknél hasonló a felnőtteknél tapasztaltakhoz.
A feltételezett mellékhatások bejelentése
A gyógyszer engedélyezését követően jelentkező feltételezett mellékhatások bejelentése fontos, mivel lehetővé teszi a gyógyszer előny / kockázat arányának folyamatos nyomon követését. agenziafarmaco.gov.it/it/responsabili.
04.9 Túladagolás -
Jelek és tünetek
Korlátozott tapasztalat áll rendelkezésre az ondasetron túladagolásával kapcsolatban.A legtöbb esetben a tünetek hasonlóak voltak az ajánlott adagot kapó betegeknél már jelentettekhez (lásd 4.8 pont).
A bejelentett megnyilvánulások közé tartoznak a látászavarok, a súlyos székrekedés, a hypotensio és a vasovagalis epizódok, átmeneti másodfokú AV -blokáddal.
Az ondanszetron dózisfüggő módon meghosszabbítja a QT intervallumot. Túladagolás esetén ajánlott az EKG monitorozása
Kezelés
Az ondanszetronnak nincs specifikus ellenszere, ezért megfelelő tüneti és támogató terápiát kell biztosítani minden túladagolás gyanúja esetén.
Az ipecac alkalmazása az ondanszetron túladagolásának kezelésére nem ajánlott, mivel a betegek valószínűleg nem reagálnak az ondasetron antiemetikus hatása miatt.
05.0 FARMAKOLÓGIAI TULAJDONSÁGOK -
05,1 "Farmakodinamikai tulajdonságok -
Farmakoterápiás csoport: hányáscsillapítók és hányingercsökkentők, szerotonin (5HT3) antagonisták.
ATC kód: A04AA01.
A cselekvés mechanizmusa
Az ondanszetron erős és nagyon szelektív 5-HT3 receptor antagonista.
Pontos hányáscsillapító és hányingerellenes hatásmechanizmusa nem ismert. A kemoterápiás szerek és a sugárterápia szerotonin (5-HT) felszabadulását okozhatja a vékonybélből, ami az 5-HT3 receptorokon keresztül a szerotoninerg vagális afferensek aktiválásával kiválthatja a gag reflex. Az ondanszetron gátolja ennek a reflexnek a beindulását. Továbbá, a vagális afferens útvonalak aktiválása meghatározhatja a IV kamra fenekén elhelyezkedő posztrema terület szintjén a szerotonin felszabadulását, és ez központi mechanizmuson keresztül stimulálhatja a hányást. Ezért az ondanszetron hatékonysága a citotoxikus kemoterápia és sugárterápia által kiváltott hányinger és hányás kezelésében valószínűleg annak köszönhető, hogy antagonista hatást fejt ki a központi és a perifériás idegrendszerben elhelyezkedő idegsejtek 5HT3 -receptoraira.
A hatásmechanizmus a műtét utáni hányinger és hányás ellenőrzésében ismeretlen, de hasonló lehet a citotoxikus okozta hányinger és hányás kontrollmechanizmusához.
Egy önkénteseken végzett farmakopszichológiai vizsgálatban az ondanszetron nem mutatott nyugtató hatást.
Az ondanszetron nem változtatja meg a plazma prolaktin koncentrációját.
Az ondanszetron szerepe az opioidok által kiváltott hányásban még mindig nem világos.
Gyermekpopuláció
Kemoterápia okozta hányinger és hányás (CINV)
Az ondansetron hatékonyságát a rákos kemoterápia által kiváltott hányás és hányinger leküzdésében egy randomizált kettős-vak klinikai vizsgálatban értékelték 415 1 és 18 év közötti betegen (S3AB3006).
A kemoterápia napján a betegek 5 mg / m² ondanszetront i.v. + 4 mg ondanszetron orálisan 8 vagy 12 óra elteltével, vagy ondansetron 0,45 mg / kg iv. + orális placebo 8 vagy 12 óra múlva.
A kemoterápia után mindkét csoport 4 mg ondanszetron -szirupot kapott naponta kétszer 3 napon keresztül. A hányás teljes kontrollja a kemoterápia legrosszabb napján 49% (5 mg / m² iv. + Ondanszetron 4 mg szájon át) és 41% (0,45 mg / kg iv. + Placebo orálisan).
A kemoterápia után mindkét csoport 4 mg ondanszetron -szirupot kapott naponta kétszer 3 napon keresztül.
Egy kettős vak, randomizált, placebo-kontrollos klinikai vizsgálat (S3AB4003) 438, 1-17 éves korú betegen, a kemoterápia legrosszabb napján a hányinger teljes ellenőrzését igazolta:
• A betegek 73% -a ≥, amikor ondanszetront intravénásan adtak be 5 mg / m² dózisban i.v. orálisan 2-4 mg dexametazonnal együtt
• a betegek 71% -a, amikor az ondanszetront szirupként 8 mg + 2-4 mg dexametazon dózisban, szájon át adták kemoterápiás napokon).
A kemoterápia után mindkét csoport 4 mg ondanszetron -szirupot kapott naponta kétszer 2 napon keresztül.
Az ondanszetron hatékonyságát 75, 6-48 hónapos gyermeknél vizsgálták egy nyílt, nem összehasonlító egykaros vizsgálatban (S3A40320). Minden gyermek 3, 0,15 mg / kg dózisú intravénás ondanszetront kapott, 30 perccel a kezdés előtt. kemoterápia után, és 4 és 8 órával az első adag után.
A hányás teljes kontrollját a betegek 56% -ában sikerült elérni.
Egy másik nyílt, nem összehasonlító egykaros vizsgálat (S3A239) egy 0,15 mg / kg ondanszetron adag, majd ezt követően 2 orális 4 mg ondasetron dózis hatékonyságát vizsgálta az éves korú gyermekeknél
A hányás teljes kontrollját a betegek 42% -ában sikerült elérni.
A műtét utáni hányinger és hányás megelőzése (PONV)
Az ondanszetron egyetlen adagjának hatékonyságát a posztoperatív hányinger és hányás megelőzésében egy randomizált, placebo-kontrollos, kettős-vak vizsgálatban vizsgálták 670 1–24 hónapos (fogamzás utáni életkor ≥ 44 hét, súly ≥ 3) gyermek bevonásával. A bevont alanyok szelektív műtétet akartak végezni általános érzéstelenítésben, és ASA -szintjük ≤ III volt. Egyszer 0,1 mg / kg ondanszetron dózist adtak be az altatást követő 5 percen belül.A 24 órás értékelési időszakban (ITT) legalább egy hányási epizódot tapasztaló alanyok százalékos aránya magasabb volt a placebót kapó betegeknél, mint azoknál, akik ondanszetront kaptak (28% vs 11%, p
Négy kettős-vak, placebo-kontrollos vizsgálatot végeztek 1469 férfi és női (2-12 éves) betegben, akik altatásban részesültek. A betegeket randomizálták az ondanszetron egyszeri intravénás adagjaira (0,1 mg / kg 40 kg -os gyermekgyógyászati betegeknél vagy 4 mg -nál kevesebbnél 40 kg -nál nagyobb testtömegű gyermekeknél, a betegek száma = 735) vagy placebót (betegek száma = 734) . A vizsgálati gyógyszert legalább 30 másodperc alatt adták be, közvetlenül az érzéstelenítés indukálása előtt vagy után Az ondanszetron szignifikánsan hatékonyabb volt a hányinger és hányás megelőzésében, mint a placebo. E vizsgálatok eredményeit a 3. táblázat foglalja össze.
3. táblázat: A PONV megelőzése és kezelése gyermekgyógyászati betegeknél - 24 órás válaszreakció
CR = nincs hányinger, mentés vagy elvonás
05,2 "Farmakokinetikai tulajdonságok -
Orális adagolást követően az ondanszetron passzívan és teljes mértékben felszívódik a gyomor -bél traktuson keresztül, és első metabolizmuson megy keresztül (biohasznosulása körülbelül 60%). A plazma csúcskoncentrációja 8 mg -os adag után körülbelül 30 ng / ml, és körülbelül 1,5 órával az alkalmazás után . 8 mg feletti dózisok esetén az ondanszetron szisztémás expozíciójának növekedése az adag növelésével nagyobb, mint az arányos növekedés; tükrözheti az első lépcső metabolizmusának csökkenését nagyobb orális dózisok esetén. Orális adagolás után a biohasznosulás kissé megnő az étel jelenlétében, de Egészséges idős önkénteseken végzett vizsgálatok kimutatták az ondanszetron orális biohasznosulásának (65%) és felezési idejének (5 óra) enyhe, de klinikailag nem szignifikáns, az életkorral összefüggő növekedését. Nemek közötti különbségeket figyeltek meg az ondanszetron metabolizmusában: a nőknél nagyobb a felszívódás sebessége és foka az orális adag után, és csökken a szisztémás clearance és az eloszlási térfogat (súlyhoz igazítva).
Az ondanszetron rendelkezésre állása orális, intramuszkuláris és intravénás adagok után hasonló, a terminális felezési idő körülbelül 3 óra, és az egyensúlyi állapotú eloszlási térfogat körülbelül 140 liter. Az ondansetron intramuszkuláris és intravénás beadása után ekvivalens szisztémás expozíció érhető el.
Az ondanszetron nem kötődik erősen a fehérjékhez (70-76%). A plazmakoncentráció és a hányáscsillapító hatás között nincs közvetlen összefüggés. Az ondanszetron a metabolikus úton többnyire a máj metabolizmusa révén ürül ki a szisztémás keringésből. A felszívódott adag kevesebb mint 5% -a változatlan formában ürül a vizelettel. A CYP2D6 enzim hiánya ( debrizokin polimorfizmus) nincs hatással az ondanszetron farmakokinetikájára Az ondanszetron farmakokinetikai jellemzői változatlan adagolás után változatlanok.
Különleges populációk
Gyermekek és serdülők (1 hónap és 17 év között)
1–4 hónapos (n = 19) gyermekgyógyászati betegeknél, akiket műteni kellett, súlyuk normalizálódott, a clearance megközelítőleg 30% -kal alacsonyabb volt, mint az 5–24 hónapos betegeknél (n = 22), de összehasonlítható a 3 és 12 év közötti betegekkel évek. Az 1-4 hónapos betegpopulációban a felezési idő 6,7 órát jelentett, szemben az 5-24 hónapos és 3-12 éves betegek 2,9 órájával.
Az 1-4 hónapos betegpopuláció farmakokinetikai paramétereiben mutatkozó különbségek részben azzal magyarázhatók, hogy a csecsemőknél és gyermekeknél nagyobb a vízmennyiség, és nagyobb a vízben oldódó gyógyszerek, például az ondanszetron eloszlási térfogata.
A 3-12 éves gyermekeknél, akik általános érzéstelenítésben szelektív műtéten estek át, a clearance és az eloszlási térfogat abszolút értékei csökkentek a felnőtt betegekhez képest.
Mindkét paraméter lineárisan nőtt a súlyával, és 12 éves korukra az értékek megközelítették a fiatal felnőttekét.
Amikor a clearance -t és az eloszlási térfogatot testtömeg szerint normalizálták, ezeknek a paramétereknek az értékei hasonlóak voltak a populáció korcsoportjai között. A súlyalapú adagolás alkalmazása kompenzálja az életkorral kapcsolatos eltéréseket, és hatékonyan normalizálja a szisztémás expozíciót gyermekgyógyászati betegeknél.
A populáció farmakokinetikai elemzését 428 alanyon (rákos betegek, műtéti betegek és egészséges betegek) végezték 1 hónaptól 44 éves korig az ondanszetron intravénás beadását követően. Ezen elemzés alapján az ondanszetron orális vagy intravénás adagolását követően szisztémás expozíció (AUC) gyermekeknél és serdülők összehasonlíthatóak voltak a felnőttekkel, az 1-4 hónapos gyermekek kivételével A kötet korfüggő volt, és felnőtteknél alacsonyabb volt, mint csecsemőknél és gyermekeknél. A clearance a súlyhoz, de nem az életkorhoz kapcsolódott, az 1-4 hónapos csecsemők kivételével.
Nehéz megállapítani, hogy az 1-4 hónapos csecsemőknél tovább csökkent-e az életkorral összefüggő clearance, vagy egyszerűen veleszületett variabilitás az ebben a korcsoportban vizsgált alanyok alacsony száma miatt. Mivel a betegek 6 hónaposnál fiatalabbak csak egy adag PONV -t kap, a csökkent clearance nem lehet klinikailag releváns.
Veseelégtelenség
Veseelégtelenségben (kreatinin-clearance 15-60 ml / perc) szenvedő betegeknél az ondanszetron intravénás beadását követően mind a szisztémás clearance, mind az eloszlási térfogat csökken, ami az eliminációs felezési idő enyhe, de klinikailag jelentéktelen növekedését eredményezi. (5.4 óra.) A rendszeres hemodialízist igénylő, súlyos veseelégtelenségben szenvedő betegeknél végzett vizsgálat (dialízisek között vizsgálva) kimutatta, hogy az ondanszetron farmakokinetikája lényegében változatlan az intravénás beadás után.
Idős vagy veseelégtelenség
Az idősekkel vagy veseelégtelenségben szenvedő betegeken végzett speciális vizsgálatok az IV -re és az orális adagolásra korlátozódtak. Az ondanszetron felezési ideje a rektális beadás után azonban ezekben a populációkban várhatóan hasonló lesz az egészséges önkéntesekéhez, mivel a rektális beadást követő ondanszetron-eliminációs sebességet nem a szisztémás clearance határozza meg.
Májelégtelenség
Orális, intravénás vagy intramuszkuláris adagolás után súlyos májelégtelenségben szenvedő betegeknél a szisztémás clearance jelentősen csökken, az eliminációs felezési idő meghosszabbodik (15-32 óra), és a szájon át történő biológiai hozzáférhetőség megközelíti a 100% -ot a csökkent metabolizmus miatt. Az ondasentron farmakokinetikáját kúpként történő alkalmazás után nem értékelték májelégtelenségben szenvedő betegeknél.
05.3 A preklinikai biztonságossági adatok -
A hagyományos farmakológiai biztonságossági, ismételt dózistoxicitási, genotoxicitási és karcinogenitási vizsgálatok alapján a nem klinikai adatok nem mutattak ki különleges veszélyt az emberekre.
Az ondanszetron és metabolitjai felhalmozódnak a patkányok tejében, a tej / plazma arány 5,2.
A klónozott emberi ionok szívcsatornáiban végzett vizsgálat kimutatta, hogy az ondanszetron a HERG káliumcsatornák blokkolásával befolyásolhatja a szív repolarizációját. Ennek a megállapításnak a klinikai jelentősége nem világos. A QT-megnyúlás. Dózisfüggő, részletes önkéntesek (lásd 5.1 pont)
06.0 GYÓGYSZERÉSZETI INFORMÁCIÓK
06.1 Segédanyagok -
A tabletta magja:
Laktóz -monohidrát, mikrokristályos cellulóz, előzselatinizált kukoricakeményítő, magnézium -sztearát.
A tabletták bevonata:
Hipromellóz, titán -dioxid (E171), hidroxi -propil -cellulóz, makrogol, szorbitán -oleát, szorbinsav, vanillin, kinolin -sárga (E104).
06.2 Inkompatibilitás "-
Nem releváns.
06.3 Érvényességi idő "-
3 év.
06.4 Különleges tárolási előírások -
Ez a gyógyszer nem igényel különleges tárolási előírásokat.
06.5 A közvetlen csomagolás jellege és a csomagolás tartalma -
Buborékcsomagolás (PVC / AL)
4 mg: 3, 6, 10, 14, 15, 20, 30, 40, 50, 60, 90, 100, 200, 300 és 500 filmtabletta.
8 mg: 3, 6, 9,10, 14, 15, 20, 30, 40, 50, 60, 90, 100, 200, 300 és 500 filmtabletta.
Nem feltétlenül mindegyik kiszerelés kerül kereskedelmi forgalomba.
06.6 Használati és kezelési útmutató -
Nincsenek speciális utasítások.
A fel nem használt gyógyszereket és a keletkező hulladékot a helyi előírásoknak megfelelően kell megsemmisíteni.
07.0 A „FORGALOMBA HOZATALI ENGEDÉLY” TULAJDONOSA -
Mylan S.p.A. - Via Vittor Pisani, 20 - 20124 Milánó, Olaszország
08.0 A FORGALOMBA HOZATALI ENGEDÉLY SZÁMA -
4 mg filmtabletta 3 tabletta PVC / AL buborékcsomagolásban - AIC n. 037548017
4 mg filmtabletta 6 tabletta PVC / AL-AIC buborékcsomagolásban n. 037548029
4 mg filmtabletta 10 tabletta PVC / AL-AIC buborékcsomagolásban n. 037548031
4 mg filmtabletta 14 tabletta PVC / AL-AIC buborékcsomagolásban n. 037548043
4 mg filmtabletta 15 tabletta PVC / AL buborékcsomagolásban - AIC n. 037548056
4 mg filmtabletta 20 tabletta PVC / AL buborékcsomagolásban - AIC n. 037548068
4 mg filmtabletta 30 tabletta PVC / AL buborékcsomagolásban - AIC n. 037548070
4 mg filmtabletta 40 tabletta PVC / AL-AIC buborékcsomagolásban n. 037548082
4 mg filmtabletta 50 tabletta PVC / AL-AIC buborékcsomagolásban n. 037548094
4 mg filmtabletta 60 tabletta PVC / AL-AIC buborékcsomagolásban n. 037548106
4 mg filmtabletta 90 tabletta PVC / AL-AIC buborékcsomagolásban n. 037548118
4 mg filmtabletta 100 tabletta PVC / AL-AIC buborékcsomagolásban n. 037548120
4 mg filmtabletta 200 tabletta PVC / AL-AIC buborékcsomagolásban n. 037548132
4 mg filmtabletta 300 tabletta PVC / AL-AIC buborékcsomagolásban n. 037548144
4 mg filmtabletta 500 tabletta PVC / AL-AIC buborékcsomagolásban n. 037548157
8 mg filmtabletta 3 tabletta PVC / AL-AIC buborékcsomagolásban n. 037548169
8 mg filmtabletta 6 tabletta PVC / AL-AIC buborékcsomagolásban n. 037548171
8 mg filmtabletta 10 tabletta PVC / AL-AIC buborékcsomagolásban n. 037548183
8 mg filmtabletta 14 tabletta PVC / AL-AIC buborékcsomagolásban n. 037548195
8 mg filmtabletta 15 tabletta PVC / AL-AIC buborékcsomagolásban n. 037548207
8 mg filmtabletta 20 tabletta PVC / AL-AIC buborékcsomagolásban n. 037548219
8 mg filmtabletta 30 tabletta PVC / AL-AIC buborékcsomagolásban n. 037548221
8 mg filmtabletta 40 tabletta PVC / AL-AIC buborékcsomagolásban n. 037548233
8 mg filmtabletta 50 tabletta PVC / AL-AIC buborékcsomagolásban n. 037548245
8 mg filmtabletta 60 tabletta PVC / AL-AIC buborékcsomagolásban n. 037548258
8 mg filmtabletta 90 tabletta PVC / AL-AIC buborékcsomagolásban n. 037548260
8 mg filmtabletta 100 tabletta PVC / AL-AIC buborékcsomagolásban n. 037548272
8 mg filmtabletta 200 tabletta PVC / AL-AIC buborékcsomagolásban n. 037548284
8 mg filmtabletta 300 tabletta PVC / AL-AIC buborékcsomagolásban n. 037548296
8 mg filmtabletta 500 tabletta PVC / AL buborékcsomagolásban - AIC n. 037548308
4 mg filmtabletta 9 tabletta PVC / AL-AIC buborékcsomagolásban n. 037548310
8 mg filmtabletta 9 tabletta PVC / AL-AIC buborékcsomagolásban n. 037548322
09.0 AZ ELSŐ ENGEDÉLYZÉS ÉS A JÓVÁHAGYÁS MEGÚJÍTÁSÁNAK DÁTUMA -
2008. november
2012. október
10.0 A SZÖVEG FELÜLVIZSGÁLÁSÁNAK DÁTUMA -
2015. augusztus