Szerk .: Dr. Giovanni Chetta
A biokémiától a biomechanikáig

Extra-celluláris mátrix (MEC)
Az ECM (extracelluláris mátrix) leírása - noha ma már keveset tudunk - elengedhetetlen ahhoz, hogy jobban megértsük a gerinc és a testtartás megváltozásának fontosságát az egészségben.
Minden sejtnek, mint minden többsejtű élő szervezetnek, éreznie kell és kölcsönhatásba kell lépnie a környezetével, hogy elvégezze létfontosságú funkcióit és fennmaradjon. Egy többsejtű szervezetben a sejteknek össze kell hangolniuk a különböző viselkedési formákat, mint egy emberi közösségben.

Az ECM -t általában úgy írják le, mint amely több nagy osztályú biomolekulából áll:
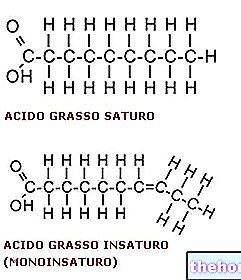
- Szerkezeti fehérjék (kollagén és elasztin)
- Speciális fehérjék (fibrillin, fibronektin, laminin stb.)
- Proteoglikánok (aggregánok, szindekánok) és glusaminoglikánok (hialuronánok, kondroitin -szulfátok, heparán -szulfátok stb.)
A szerkezeti fehérjék közül az i kollagén alkotják a glikoproteinek leginkább képviselt családját az állatvilágban. Ezek a legtöbb jelen lévő fehérje az ECM -ben (de nem a legfontosabbak), és a megfelelő kötőszövetek (porc, csont, fascia, inak, szalagok) alapvető alkotóelemei.
A kollagéneket többnyire fibroblasztok szintetizálják, de a hámsejtek is képesek szintetizálni.
A kollagénszálak folyamatosan kölcsönhatásba lépnek az ECM más nagy molekuláival, amelyek biológiai kontinuumot képeznek a sejt életében. A fibrillákhoz tartozó kollagének meghatározó szerepet játszanak a szinte feszültségnek ellenálló szerkezetek kialakításában és fenntartásában. rugalmatlan kollagén termelődik és újra metabolizálódik a mechanikai terhelés függvényében, és viszkoelasztikus tulajdonságai nagy hatással vannak az ember testtartására.
A kollagénszálak PG / GAG bevonatuknak köszönhetően (proteoglikánok / glükozaminoglikánok) bioszenzoros és biovezető tulajdonságokkal rendelkeznek. Valójában tudjuk, hogy minden olyan mechanikai erő, amely szerkezeti deformációt képes előidézni, megfeszíti a molekulák közötti kötéseket, ami enyhe elektromos fluxust, azaz a piezoelektromos áramot hoz létre (Athenstaedt, 1969). Ezért a háromdimenziós és mindenütt jelen lévő kollagénhálózatnak is megvan a sajátossága, hogy bioelektromos jeleket vezessen a tér három dimenziójában, a kollagénszálak és a sejtek közötti relatív elrendezés alapján, afferens irányban (az ECM-től a sejtekig) vagy fordítva fordítva efferens.
Mindez egy valós idejű MEC-sejt kommunikációs rendszert jelent, és az ilyen elektromágneses biojelek fontos biokémiai változásokhoz vezethetnek, például abban az esetben, ha a "csont-oszteoklasztok nem képesek" megemészteni "piezoelektromos töltésű csontot (Oschman, 2000).
Végezetül ki kell emelni, hogy a sejt nem meglepő módon folyamatosan és jelentős energiaköltséggel (kb. 70%) termel anyagot, amelyet szükségszerűen ki kell üríteni a protokollagén (a kollagén biológiai prekurzora) kizárólagos tárolásán keresztül bizonyos vezikulákban ( Albergati, 2004).
A gerinces szövetek túlnyomó többsége két létfontosságú tulajdonság egyidejű jelenlétét igényli: az erő és a rugalmasság. Egy igazi hálózat rugalmas szálak, ezeknek a szöveteknek az ECM -ben található, lehetővé teszi, hogy az erős húzások után visszatérjenek a kezdeti körülményekhez Az elasztikus szálak képesek legalább ötszörösére növelni egy szerv vagy annak egy részének nyújthatóságát. Hosszú, rugalmatlan kollagénszálak vannak elhelyezve az elasztikus szálak között azzal a pontos feladattal, hogy korlátozzák a "túlzott deformációt a szövetek húzása által." az aorta teljes száraz tömegének több mint 50% -át teszi ki), a szalagokban, a tüdőben és a bőrben.
Az ECM nagyszámú (és még mindig nem pontosan meghatározott) speciális, nem kollagén fehérjét tartalmaz, amelyek jellemzően specifikus kötődési helyekkel rendelkeznek más ECM molekulákhoz és sejtfelszíni receptorokhoz. Ily módon ezeknek a fehérjéknek minden egyes összetevője a kapcsolatok "erősítőjeként" működik, mind a hasonló, mind a különböző molekulák között, és végtelen biokémiai hálózatot hoz létre, amely képes millió és millió biokémiai információ létrehozására, módosítására, variálására és szaporítására akár távolról is (és az energia).
Az extracelluláris mátrix fontos "speciális fehérje" a fibronektin, minden gerincesben megtalálható nagy molekulatömegű glikoprotein. Úgy tűnik, hogy a fibronektin különböző módon képes befolyásolni a sejtek növekedését, az intercelluláris adhéziót és az ECM segítségével a sejtvándorlást (a sejt naponta akár 5 cm -rel is képes mozogni - Albergati, 2004) stb. A legismertebb, III. Típusú izoform kötődik az integrinekhez . Az utóbbiak a transzmembrán fehérjék családja, amelyek mechanoreceptorokként működnek: szelektíven és modulálható módon transzdukálják a mechanikus húzásokat és lökéseket az ECM -ből a sejt belsejében és fordítva, a citoplazmában a citoszkeletont és más fehérjék, amelyek szabályozzák a sejtek tapadását, növekedését és migrációját (Hynes, 2002).
A glükózaminoglikánok (GAGS) és a proteoglikánok (PG) erősen hidratált, gélszerű anyagot képeznek a kötőszövetekben, amelyekben a fibrilláris fehérjék elhelyezkednek és beágyazódnak. Ez a poliszacharid gélforma egyrészt képes az ECM -nek ellenállni a jelentős nyomóerőknek, másrészt lehetővé teszi a tápanyagok, metabolitok és hormonok gyors, állandó és szelektív diffúzióját a vér és a szövetek között.
A glükózaminoglikánok poliszacharid láncai térfogatilag túl merevek ahhoz, hogy a polipeptidláncokra jellemző kompakt gömbszerkezetek belsejébe hajtsanak, ráadásul erősen hidrofilek. Ezen okok miatt (és valószínűleg más, számunkra ismeretlen okok miatt) a GAG -ok hajlamosak rendkívül konformációkat feltételezni. a tömegükhöz képest nagy térfogatot foglalnak el, és így alacsony koncentrációban is jelentős mennyiségű gélt képeznek. ezek között meghatározó szerepet játszik a Na +, amely a teljes ozmotikus kapacitást biztosítja, és hatalmas mennyiségű vizet fog el az ECM -ben. Ily módon duzzanatok (turgorok) keletkeznek, amelyek lehetővé teszik az ECM számára, hogy ellenálljon még a fontos nyomóerőknek is (ennek köszönhetően például a csípő porcai fiziológiai körülmények között tökéletesen ellenállnak a több száz légköri nyomásnak).
A kötőszöveten belül a GAG-ok a globális tömeg kevesebb, mint 10-12% -át teszik ki, de jellemzőiknek köszönhetően sok extracelluláris teret töltenek ki, különböző méretű és sűrűségű elektromos töltésű hidratált gél pórusait képezve, így szelektívként kulcspontok vagy "szerverek", amelyeken keresztül a MEC -n belüli molekulák és sejtek forgalmát szabályozzák méretük, súlyuk és elektromos töltésük alapján.
A hialuronsav (hialuronán, hialuronát) a GAG-ok közül talán a legegyszerűbb. Kísérleti és molekuláris-biológiai adatok megerősítik, hogy alapvető szerepet játszik a csontok és az ízületek szintjén a jelentős nyomásokkal szemben. : üres tereket hoz létre a sejtek között, amelyekbe a későbbi szakaszokban vándorolnak (Albergati, 2004).
Nem minden PG -t választ ki az ECM, egyesek a plazmamembránok szerves összetevői (Alberts, 2002).
Az extra-celluláris mátrix ezért nagyon összetett hálózatnak tekinthető, amelyben a fehérjék, a PGS és a GAG-ok számtalan funkciót látnak el, beleértve a strukturális támogatást és minden szövet és szervi tevékenység szabályozását. A globális sejtes homeosztázist olyan mechanizmusok komplexumának kell tekinteni, amelyek a sejt belsejében vagy az ECM -en kívül keletkezhetnek és fejlődhetnek; utóbbi esetben a sejt képviselheti a köztes vagy végső célpontot. Az extracelluláris komponensek amellett, hogy a sejtállvány fizikai támasztószerkezeteit képviselik, valódi helyszínekként szolgálnak mind az endocelluláris környezetet, mind a szerveket és rendszereket érintő létfontosságú folyamatok elindításához, fejlesztéséhez és befejezéséhez. Egy végtelen biokémiai hálóval állunk szemben, amely millió és millió információ létrehozására, modulálására, variálására és terjedésére képes, még távolról is.
A test minden sejtje folyamatosan kölcsönhatásba lép az ECM -mel, mind mechanikai, mind kémiai, mind energetikai szempontból, "drámai" hatással a szövetek statikus és dinamikus felépítésére. P. A. Bacci szerint az intersticiális mátrix valóban a vitális reakciók anyját képviseli, azt a helyet, ahol mindenekelőtt az anyag és az energia cseréje zajlik. Minden szövet össze van kötve és funkcionálisan integrálva van egymással nem zárt, hanem nyitott rendszerekben; folyamatos cserék zajlanak közöttük, amelyek történhetnek mind helyileg, mind szisztematikusan, kihasználva a biokémiai, biofizikai és elektromágneses üzeneteket, vagyis felhasználva a különböző energiaformákat.
Mint F. G.A sejt és az extracelluláris mátrix két, látszólag különálló világot képvisel, amelyeknek szükségszerűen az élet teljes időtartama alatt kölcsönhatásba kell lépniük bármelyik pillanatban ahhoz, hogy helyesen és szinergikusan működjenek. Ehhez rendkívüli jelsorozatra van szükség, amelyet ugyanolyan hihetetlen molekuláris-biológiai tevékenységek sora követ.
További cikkek az "Extra -celluláris mátrix - szerkezete és funkciói" témában
- A scoliosis kezelése
- Scoliosis - okok és következmények
- Scoliosis diagnózis
- A scoliosis előrejelzése
- Kötőszövet és kötőszövet
- Csatlakozó sáv - Jellemzők és funkciók
- Testtartás és feszültség
- Az ember mozgása és a lábtámasz fontossága
- A helyes nadrágtartó és záróelemek fontossága
- Idiopátiás scoliosis - a mítoszok eloszlatása
- A scoliosis és a terápiás protokoll klinikai esete
- A kezelés eredményei Klinikai eset scoliosis
- A scoliosis mint természetes hozzáállás - Bibliográfia


















.jpg)