Szerkezet és funkciók
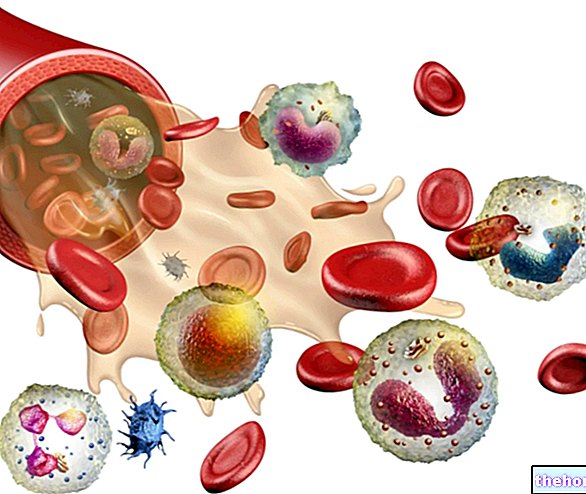
A hemoglobin a vörösvértestekben található metalloprotein, amely felelős az oxigén szállításáért a véráramban. Valójában az oxigén csak mérsékelten oldódik vízben; ezért a vérben oldott mennyiség (a teljes mennyiség kevesebb, mint 2% -a) nem elegendő a szövetek anyagcsereigényeinek kielégítésére. Nyilvánvaló tehát, hogy szükség van egy konkrét hordozóra.
A véráramban az oxigén nem tud közvetlenül és visszafordíthatóan kötődni a fehérjékhez, mint a fémek, például a réz és a vas esetében. Nem meglepő, hogy a hemoglobin minden fehérje alegységének közepén, fehérjehéjba csomagolva találjuk az ún. csoport EME, fémes szívvel, amelyet Fe2 + oxidációs állapotú (redukált állapotú) vasatom jelent, amely reverzibilis módon megköti az oxigént.
Vérvizsgálat
- Normál hemoglobin értékek a vérben: 13-17 g / 100 ml
A nőknél az értékek átlagosan 5-10% -kal alacsonyabbak, mint a férfiaknál.
A magas hemoglobin lehetséges okai
- Policitémiák
- Hosszabb tartózkodás a magas talajon
- Krónikus tüdőbetegségek
- Szívbetegség
- Véradopping (eritropoetin és származékai vagy hatásukat utánzó anyagok használata)
Az alacsony hemoglobin lehetséges okai
- Anémia
- Vashiány (vashiány)
- Bőséges vérzés
- Karcinómák
- Terhesség
- Thalassémiák
- Burns
A vér oxigéntartalmát tehát a plazmában oldott kis mennyiség és a hemoglobin vashoz kötött frakció összegzése adja.
A vérben lévő oxigén több mint 98% -a kötődik a hemoglobinhoz, amely viszont a vörösvértestekben kiosztott véráramban kering, hemoglobin nélkül ezért az eritrociták nem tudták ellátni a vér oxigénszállító szerepét.
Tekintettel ennek a fémnek a központi szerepére, a hemoglobin szintéziséhez megfelelő vasbevitelre van szükség az étrendben. A szervezetben jelen lévő vas körülbelül 70% -a valójában a hemoglobin hem -csoportjaiban található.
A hemoglobin 4 alegységből áll, amelyek szerkezetileg nagyon hasonlítanak a mioglobinhoz *.
* Míg a hemoglobin oxigént szállít a tüdőből a szövetekbe, addig a mioglobin a hemoglobin által kibocsátott oxigént a különböző sejtszervekbe (pl. Mitokondriumokba) viszi.

A hemoglobin egy nagyméretű és összetett metalloprotein, amelyet négy, gömb alakú fehérje lánc jellemez, illetve Fe2 +-ot tartalmazó hemcsoport köré tekerve.
Ezért minden hemoglobin -molekulához négy hem -csoportot találunk, amelyek a relatív gömbfehérje -láncba vannak csomagolva. Mivel minden hemoglobin molekulában négy vasatom található, minden hemoglobin molekula négy oxigénatomot köthet magához a reverzibilis reakció szerint:
Hb + 4O2 ← → Hb (O2) 4
Mint a legtöbb ember tudja, a hemoglobin feladata az, hogy oxigént vegyen be a tüdőbe, engedje el a sejteknek, amelyeknek szüksége van rá, vegyen el tőlük szén -dioxidot, és engedje el a tüdőbe, ahol a chilo újra kezdődik.
A tüdő alveolusok kapillárisaiban történő véráramlás során a hemoglobin oxigént köt magához, amely ezt követően a perifériás keringésben lévő szövetekbe szabadul fel. Ez a csere azért következik be, mert az oxigénkötések az EME csoport vasával labilak és érzékenyek számos tényezőre, amelyek közül a legfontosabb az oxigén feszültsége vagy parciális nyomása.
Az oxigén megkötése a hemoglobinhoz és a Bohr -hatás
A tüdőben a plazma oxigénfeszültsége növekszik az alveolusokból a vérbe történő diffúzió miatt (↑ PO2); ez a növekedés azt eredményezi, hogy a hemoglobin lelkesen kötődik az oxigénhez; ennek ellenkezője fordul elő a perifériás szövetekben, ahol csökken a vérben az oldott oxigén koncentrációja (↓ PO2) és nő a szén -dioxid parciális nyomása (↑ CO2); ez arra készteti a hemoglobint, hogy oxigént szabadítson fel, és CO2 -vel töltődjön fel. A koncepció lehető leegyszerűsítése, minél több szén -dioxid van a vérben, annál kevesebb oxigén marad kötve a hemoglobinhoz.
Bár a vérben fizikailag feloldott oxigén mennyisége nagyon alacsony, ezért alapvető szerepet játszik. Valójában ez a mennyiség nagymértékben befolyásolja az oxigén és a hemoglobin közötti kötés erősségét (valamint "fontos referenciaértéket jelent a pulmonális lélegeztetés szabályozásában").
Összefoglalva mindent egy grafikonon, a hemoglobinhoz kapcsolódó oxigén mennyisége a pO2 -hoz viszonyítva növekszik egy szigmoid görbét követően:

Az a tény, hogy a plató régió ilyen nagy, fontos biztonsági tételt jelent a hemoglobin maximális telítettsége során a tüdőbe való bejutás során. Bár a pO2 az alveoláris szinten általában 100 Hgmm -rel egyenlő, figyelve az ábrát, még ha az oxigén parciális nyomása is egyenlő 70 Hgmm -rel (egyes betegségek tipikus előfordulása vagy magas tengerszint feletti magasság esetén), a telített hemoglobin százalékos értéke 100%közelében marad.
A maximális lejtés tartományában, amikor az oxigén parciális feszültsége 40 Hgmm alá csökken, a hemoglobin oxigénkötő képessége hirtelen csökken.
Nyugalmi körülmények között az intracelluláris folyadékokban a PO2 megközelítőleg 40 Hgmm; ezen a helyen a gázok törvényei miatt a plazmában oldott oxigén a kapilláris membránon áthaladva az O2 szegényebb szövetei felé diffundál, következésképpen az O2 plazmafeszültsége tovább csökken, és ez elősegíti az oxigén felszabadulását a hemoglobinból. . Az intenzív fizikai megterhelés során viszont a szövetekben az oxigénfeszültség 15 Hgmm -re vagy kevesebbre csökken, aminek következtében a vér oxigénhiánya nagymértékben csökken.
Az elhangzottak szerint nyugalmi körülmények között jelentős mennyiségű oxigénnel telített hemoglobin távozik a szövetekből, és szükség esetén rendelkezésre áll (például, hogy megbirkózzon az egyes sejtek anyagcseréjének hirtelen növekedésével).
A fenti képen látható folytonos vonalat hemoglobin disszociációs görbének nevezzük; jellemzően in vitro 7,4 pH -n és 37 ° C hőmérsékleten határozzák meg.
A Bohr -hatás hatással van mind az O2 bevitelére tüdőszinten, mind annak felszabadulására szöveti szinten.
Ahol több oldott szén -dioxid található bikarbonát formájában, a hemoglobin könnyebben szabadítja fel az oxigént, és szén -dioxiddal (bikarbonát formájában) töltődik fel.

Ugyanez a hatás érhető el a vér savanyításával: minél jobban csökken a vér pH -értéke, és annál kevesebb oxigén marad kötve a hemoglobinhoz; nem meglepő, hogy a vérben a szén -dioxid elsősorban szénsav formájában oldódik, amely disszociál.



Felfedezője tiszteletére a pH vagy a szén -dioxid oxigén -disszociációra gyakorolt hatását Bohr -hatásnak nevezik.
A várakozásoknak megfelelően savas környezetben a hemoglobin könnyebben bocsátja ki az oxigént, míg bázikus környezetben erősebb a kötés az oxigénnel.

A hemoglobin oxigén iránti affinitását módosítani képes egyéb tényezők közé tartozik a hőmérséklet. Különösen a hemoglobin oxigén iránti affinitása csökken a testhőmérséklet emelkedésével. Ez különösen előnyös a téli és tavaszi hónapokban, mivel a tüdővér hőmérséklete ( a külső környezet levegője) alacsonyabb, mint a szövetekben, ahol az oxigén felszabadulását elősegítik.

2.3 A difoszfoglicerát a glikolízis közbenső terméke, amely befolyásolja a hemoglobin oxigén iránti affinitását. Ha koncentrációja a vörösvértesteken belül megnő, a hemoglobin oxigén iránti affinitása csökken, ezáltal elősegítve az oxigén szövetekbe történő felszabadulását. Nem meglepő módon az eritrocita koncentráció 2,3-difoszfoglicerát-tartalom növekedése, például vérszegénység, szív- és tüdőelégtelenség esetén, valamint a magas tengerszint feletti tartózkodás során.
Általánosságban elmondható, hogy a 2,3 -biszfoszfoglicerát hatása viszonylag lassú, különösen ha összehasonlítjuk a pH, a hőmérséklet és a szén -dioxid parciális nyomásának változására adott gyors reakcióval.

A Bohr -hatás nagyon fontos az intenzív izommunka során; ilyen körülmények között a stressznek leginkább kitett szövetekben a szén -dioxid hőmérséklete és nyomása, tehát a vér savassága lokálisan emelkedik. Amint fentebb kifejtettük, mindez kedvez az oxigén felszabadulásának a szövetekhez, jobbra tolva a hemoglobin disszociációs görbéjét.