Hatóanyagok: Norelgestromin / Ethinylestradiol
EVRA transzdermális tapasz 203 mikrogramm norelgesztromin / 24 óra + 33,9 mikrogramm etinilösztradiol / 24 óra
Miért alkalmazzák az Evra -t? Mire való?
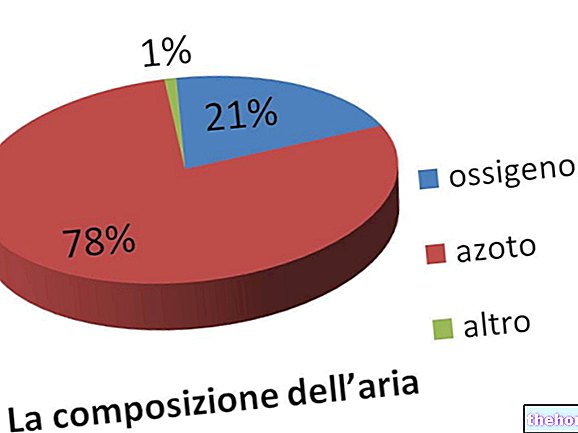
Az EVRA kétféle nemi hormont tartalmaz, a norelgestromin nevű progesztint és az etinil -ösztradiol nevű ösztrogént.
Mivel két hormont tartalmaz, az EVRA -t "kombinált hormonális fogamzásgátlónak" nevezik.
A terhesség megelőzésére szolgál.
Ellenjavallatok Mikor az Evra nem alkalmazható
Mielőtt elkezdené használni az EVRA -t, olvassa el a 2. szakaszban található információkat a vérrögökről. Különösen fontos, hogy olvassa el a vérrög tüneteit (lásd 2. pont „Vérrögök”).
Ne alkalmazza az EVRA -t:
Ne használja az EVRA -t, ha az alább felsorolt állapotok bármelyike fennáll Önnél. Ha az alább felsorolt állapotok bármelyike fennáll Önnél, forduljon orvosához. Kezelőorvosa megbeszéli Önnel az Ön számára megfelelőbb fogamzásgátló módszereket.
- ha vérrög van (vagy volt valaha) a lábának ereiben (mélyvénás trombózis, DVT), a tüdőben (tüdőembólia, PE) vagy más szervekben;
- ha tudja, hogy olyan rendellenessége van, amely befolyásolja a véralvadást, például fehérje C hiány, S fehérje hiány, antitrombin III hiány, V faktor Leiden vagy antifoszfolipid antitestek;
- ha műtéten kell átesnie, vagy ha hosszú ideig feküdni fog;
- ha valaha szívrohama vagy szélütése volt;
- ha Önnek (vagy volt valaha) angina pectoris (súlyos mellkasi fájdalmat okozó állapot, amely a szívroham első jele lehet) vagy átmeneti iszkémiás rohama (TIA - ideiglenes stroke -tünetek);
- - ha az alábbi betegségek bármelyikében szenved, amelyek növelhetik az artériák vérrögképződésének kockázatát: hiperhomociszteinémia néven ismert betegség
- ha Önnek van (vagy volt valaha) olyan típusú migrénje, amelyet „aurás migrénnek” neveznek;
- ha allergiás a norelgestrominra, az etinil -ösztradiolra vagy a gyógyszer (6. pontban felsorolt) egyéb összetevőjére
- ha azt mondták, hogy emlő-, méh-, méhnyak- vagy hüvelyrákja lehet
- ha valaha májdaganata vagy májbetegsége volt, mert a máj nem működik megfelelően
- ha megmagyarázhatatlan hüvelyi vérzése van. Ne használja ezt a gyógyszert, ha a fent felsorolt helyzetek bármelyikében találja magát. Ha nem biztos benne, kérdezze meg kezelőorvosát, gyógyszerészét vagy a gondozását végző egészségügyi szakembert a gyógyszer alkalmazása előtt.
Mikor kell különös gondosságot alkalmazni az EVRA -val
Mikor kell orvoshoz fordulni?
Sürgősen forduljon orvoshoz
Ha olyan vérrögképződésre utaló jeleket észlel, amelyek arra utalhatnak, hogy vérrögben szenved a lábában (mélyvénás trombózis), vérrög a tüdőben (tüdőembólia), szívroham vagy stroke (lásd alább "Vérrög (trombózis)").
Az alkalmazással kapcsolatos óvintézkedések Mit kell tudnia az Evra szedése előtt
A gyógyszer alkalmazása előtt konzultálnia kell orvosával.
Tájékoztassa kezelőorvosát, ha az alábbiak közül bármelyik vonatkozik Önre.
Ha ez az állapot megjelenik vagy súlyosbodik az EVRA alkalmazása során, tájékoztassa kezelőorvosát.
- ha Crohn -betegsége vagy fekélyes vastagbélgyulladása (krónikus gyulladásos bélbetegsége) van; ha szisztémás lupus erythematosus (SLE, a természetes védekezőrendszert érintő betegség) van;
- ha hemolitikus urémiás szindrómájában (HUS, veseelégtelenséget okozó véralvadási zavar) szenved;
- ha sarlósejtes vérszegénységben szenved (a vörösvértestek örökletes betegsége);
- ha magas a vérzsírszintje (hipertrigliceridémia) pancreatitis (hasnyálmirigy -gyulladás);
- ha műtéten kell átesnie, vagy ha hosszú ideig feküdni fog;
- ha most szült, nagyobb a vérrögképződés kockázata. Kérdezze meg kezelőorvosát, hogy gyermekvállalása után mennyi idő múlva kezdheti el a [kitalált név] szedését;
- ha "a bőr alatti vénák gyulladása (felületes tromboflebitisz) van;
- ha visszerek vannak.
VÉRRÖGÖK
A kombinált hormonális fogamzásgátlók, mint például az EVRA alkalmazása növeli a vérrögképződés kockázatát ahhoz képest, mint ha nem használna.Ritka esetekben a vérrög elzárhatja az ereket és súlyos problémákat okozhat.
Vérrögök alakulhatnak ki
- vénákban ("vénás trombózis", "vénás thromboembolia" vagy VTE)
- az artériákban („artériás trombózis”, „artériás thromboembolia” vagy ATE).
A vérrögökből való felépülés nem mindig teljes. Ritkán hosszan tartó súlyos hatások jelentkezhetnek, vagy nagyon ritkán halálosak is lehetnek.
Fontos megjegyezni, hogy az EVRA -val kapcsolatos káros vérrögök általános kockázata alacsony.
HOGYAN FELISMERJÜK A VÉRRÖGGET
Azonnal forduljon orvoshoz, ha az alábbi jelek vagy tünetek bármelyikét észleli.
- fájdalom vagy érzékenység a lábában, amely csak állva vagy járáskor érezhető
- fokozott hőérzet az érintett lábon
- a láb bőrének színének megváltozása, például sápadt, vörös vagy kék
- hirtelen és megmagyarázhatatlan légszomj vagy gyors légzés;
- hirtelen köhögés nyilvánvaló ok nélkül, esetleg vér kibocsátását okozva;
- éles mellkasi fájdalom, amely mély légzéssel fokozódhat;
- súlyos szédülés vagy szédülés;
- gyors vagy szabálytalan szívverés;
- súlyos fájdalom a gyomorban
- mellkasi fájdalom, kellemetlen érzés, nyomásérzet vagy nehézség
- szorító vagy teltségérzet a mellkasban, karban vagy a mellkas alatt;
- teltségérzet, emésztési zavar vagy fulladás;
- kellemetlen érzés a felsőtestben, amely a hátba, az állkapocsba, a torokba, a karokba és a gyomorba sugároz;
- izzadás, hányinger, hányás vagy szédülés;
- extrém gyengeség, szorongás vagy légszomj;
- gyors vagy szabálytalan szívverés
- hirtelen az arc, a kar vagy a láb zsibbadása vagy gyengesége, különösen a test egyik oldalán;
- hirtelen zavartság, beszéd- vagy megértési nehézség;
- hirtelen látászavar az egyik vagy mindkét szemben;
- hirtelen járási nehézség, szédülés, egyensúly vagy koordináció elvesztése;
- hirtelen, súlyos vagy elhúzódó migrén, ismeretlen ok nélkül;
- eszméletvesztés vagy ájulás rohamokkal vagy anélkül.
- az egyik végtag duzzanata és halványkék elszíneződése;
- súlyos hasi fájdalom (akut has)
VÉRRÉSZEK VÉNÁBAN
Mi történhet, ha vérrög képződik a vénában?
- A kombinált hormonális fogamzásgátlók alkalmazását összefüggésbe hozták a vénákban kialakuló vérrögképződés (vénás trombózis) kockázatával. Ezek a mellékhatások azonban ritkák. A legtöbb esetben a kombinált hormonális fogamzásgátló alkalmazás első évében jelentkeznek.
- Ha vérrög képződik a láb vagy a láb vénájában, az mélyvénás trombózist (DVT) okozhat.
- Ha vérrög utazik a lábszárból, és a tüdőben marad, az „tüdőembóliát” okozhat.
- Nagyon ritkán vérrög képződhet egy másik szervben, például a szemben (retina véna trombózis).
Mikor a legnagyobb a vérrögképződés kockázata a vénában?
A vérrög kialakulásának kockázata a vénában a legnagyobb a kombinált hormonális fogamzásgátló első alkalmazásának első évében. A kockázat még nagyobb lehet, ha 4 vagy több hetes szünet után újrakezdi a kombinált hormonális fogamzásgátló (ugyanazon vagy más gyógyszer) szedését.
Az első év után a kockázat csökken, de mindig valamivel magasabb, mint ha nem használna kombinált hormonális fogamzásgátlót.
Ha abbahagyja az EVRA szedését, a vérrögök kialakulásának kockázata néhány héten belül normalizálódik.
Mi a kockázata a vérrög kialakulásának?
A kockázat a VTE természetes kockázatától és a kombinált hormonális fogamzásgátló típusától függ.
Az EVRA -val együtt alacsony a vérrögképződés kialakulásának kockázata a lábában vagy a tüdőben (DVT vagy PE).
- 10 000 olyan nő közül, akik nem használnak kombinált hormonális fogamzásgátlót és nem terhesek, körülbelül 2 -en alakulnak ki vérrögök egy év alatt.
- 10 000 olyan nő közül, akik levonorgesztrelt, noretiszteront vagy norgesztimátot tartalmazó kombinált hormonális fogamzásgátlót használnak, körülbelül 5-7-en alakulnak ki vérrögök egy év alatt.
- 10 000 nőből, akik etonorgesztrelt vagy norelgesztromint tartalmazó kombinált hormonális fogamzásgátlót, például EVRA-t használnak, körülbelül 6-12 nőnél alakul ki vérrög egy év alatt.
- A vérrögképződés kockázata az Ön kórtörténetétől függ
Vérrögképződés kockázata egy év alatt
Nők, akik nem használnak kombinált hormontablettát / tapaszt / gyűrűt, és nem terhesek
10 000 nőből körülbelül 2
Nők, akik levonorgesztrelt, noretiszteront vagy norgesztimátot tartalmazó kombinált hormonális fogamzásgátló tablettát használnak
10 000 nőből körülbelül 5-7
Az EVRA -t használó nők
10 000 nőből körülbelül 6-12
Tényezők, amelyek növelik a vérrög kialakulásának kockázatát a vénában
Az EVRA -val történő vérrögképződés kockázata alacsony, de bizonyos állapotok miatt fokozódik. Kockázata nagyobb:
- ha súlyosan túlsúlyos (testtömeg -index vagy 30 kg / m2 feletti BMI);
- ha egy közeli hozzátartozójánál vérrög keletkezett a lábában, a tüdőben vagy más szervben fiatalon (kevesebb, mint 50 év). Ebben az esetben öröklött véralvadási zavara lehet;
- ha műtétre készül, vagy ha hosszú ideig kell feküdnie sérülés vagy betegség miatt, vagy ha gipszben van a lába. Előfordulhat, hogy néhány héttel a műtét előtt vagy a műtét során abba kell hagynia az EVRA szedését. ha Önnek abba kell hagynia az EVRA szedését, kérdezze meg kezelőorvosát, hogy mikor kezdheti újra a szedését;
- ahogy öregszik (különösen 35 év felett);
- ha kevesebb, mint néhány hete szült.
A vérrög kialakulásának kockázata növekszik, minél több ilyen típusú betegsége van.
A légi utazás (több mint 4 óra) átmenetileg növelheti a vérrögképződés kockázatát, különösen, ha fennáll a felsorolt egyéb kockázati tényezők egy része.
Fontos, hogy tájékoztassa kezelőorvosát, ha ezek bármelyike vonatkozik Önre, akkor is, ha nem biztos benne. Kezelőorvosa dönthet úgy, hogy abba kell hagynia az EVRA alkalmazását.
Tájékoztassa kezelőorvosát, ha a fenti állapotok bármelyike megváltozik az EVRA alkalmazása során, például, ha közeli hozzátartozója ismeretlen okból trombózist szenved, vagy ha sokat hízik.
VÉRRÉSZEK ARTERYBEN
Mi történhet, ha vérrög képződik az "artériában"?
A vénákban kialakuló vérrögökhöz hasonlóan az artériás vérrögök is súlyos problémákat okozhatnak, például szívrohamot vagy stroke -ot okozhatnak.
Tényezők, amelyek növelik a vérrög kialakulásának kockázatát az artériában
Fontos megjegyezni, hogy az EVRA alkalmazásával összefüggő szívroham vagy stroke kockázata nagyon alacsony, de növelheti:
- az életkor növekedésével (35 év felett);
- ha dohányzik. Ha kombinált hormonális fogamzásgátlót, például EVRA -t használ, tanácsos abbahagyni a dohányzást. Ha nem tudja abbahagyni a dohányzást és 35 évesnél idősebb, kezelőorvosa másfajta fogamzásgátló alkalmazását javasolhatja Önnek; ha túlsúlyos;
- ha magas a vérnyomása;
- ha közvetlen családtagja szívinfarktust vagy stroke -ot kapott fiatalon (kevesebb, mint 50 év). Ebben az esetben a szívroham vagy a stroke kockázata is nagy lehet;
- ha Önnek vagy közeli hozzátartozójának magas a vérzsírszintje (koleszterin vagy trigliceridek);
- ha migrénben szenved, különösen aurás migrénben;
- ha bármilyen szívproblémája van (szelephiba, szívritmuszavar, amit pitvarfibrillációnak neveznek);
- ha cukorbeteg.
Ha ezen állapotok közül egynél több vagy Önnél különösen súlyos, akkor a vérrög kialakulásának kockázata még nagyobb lehet.
Tájékoztassa kezelőorvosát, ha a fenti állapotok bármelyike megváltozik az EVRA alkalmazása során, például ha elkezd dohányozni, ha közeli hozzátartozója ismeretlen okból trombózist szenved, vagy ha sokat hízik.
Ezenkívül beszéljen kezelőorvosával, gyógyszerészével vagy a gondozását végző egészségügyi szakemberrel az EVRA alkalmazása előtt, ha az alábbi állapotok bármelyike fennáll Önnél, vagy ha ezek az állapotok kialakulnak vagy súlyosbodnak: ha úgy gondolja, hogy terhes
- ha fejfájása súlyosbodik vagy gyakrabban jelentkezik
- ha súlya 90 kg vagy több
- - ha magas vagy emelkedő vérnyomása van
- ha epehólyag -betegsége van, beleértve az epeköveket vagy az epehólyag -gyulladást
- ha "porfíriának" nevezett vérbetegségben szenved
- ha olyan idegrendszeri betegsége van, amely hirtelen testmozgásokat okoz, "Sydenham chorea"
- ha a terhesség alatt hólyagos kiütései voltak („terhességi herpesz”)
- ha halláskárosodásban szenved
- ha cukorbeteg
- ha depressziós
- ha epilepsziás vagy bármilyen más rohamokat okozó betegsége van
- ha májproblémái vannak, beleértve a bőr és a szemfehérje besárgulását (sárgaság)
- ha "terhességi foltjai" vannak vagy voltak. Ezek sárgásbarna foltok, különösen az arcon ("chloasma"). Előfordulhat, hogy ezek a foltok nem szűnnek meg teljesen az EVRA abbahagyása után. Védje bőrét a napfénytől vagy az ultraibolya sugárzástól. Ezzel megelőzheti a foltok megjelenését vagy rosszabbodását.
- ha veseproblémái vannak.
Ha nem biztos abban, hogy a fenti állapotok bármelyike vonatkozik -e Önre, beszéljen kezelőorvosával vagy gyógyszerészével az EVRA alkalmazása előtt.
Szexuális úton terjedő betegségek
Ez a gyógyszer nem fogja megvédeni Önt a HIV -fertőzéstől (AIDS) vagy más nemi úton terjedő betegségektől. Ezek közé tartozik a chlamydia, a genitális herpesz, az acuminata szemölcs, a gonorrhoea, a hepatitis B, a szifilisz. Mindig használjon óvszert, hogy megvédje magát az ilyen betegségektől.
Klinikai vizsgálatok
Ha vér- vagy vizeletvizsgálatra van szüksége, mondja el orvosának vagy a biológiai mintát gyűjtő személynek, hogy EVRA -t használ, mivel a hormonális fogamzásgátlók befolyásolhatják egyes vizsgálati eredményeket.
Gyermekek és serdülők
Az EVRA -t nem vizsgálták gyermekeknél és 18 év alatti serdülőknél. Az EVRA nem alkalmazható olyan gyermekeknél és serdülőknél, akiknél még nem volt első menstruáció.
Kölcsönhatások Milyen gyógyszerek vagy élelmiszerek változtathatják meg az Evra hatását
Feltétlenül tájékoztassa kezelőorvosát vagy gyógyszerészét a jelenleg vagy nemrégiben szedett, valamint szedni tervezett egyéb gyógyszereiről.
Egyes gyógyszerek és gyógynövények befolyásolhatják az EVRA hatékonyságát, ebben az esetben teherbe eshet.
Tájékoztassa kezelőorvosát, ha az alábbiakat szedi:
- bizonyos antiretrovirális gyógyszerek a HIV / AIDS kezelésére (például nelfinavir, ritonavir, nevirapin, efavirenz)
- fertőzések kezelésére használt gyógyszerek (például rifampin, rifabutin és griseofulvin, penicillinek és tetraciklinek)
- görcsrohamok kezelésére szolgáló gyógyszerek (néhány példa a topiramát, fenorbarbitál, fenitoin, karbamazepin, primidon, oxikarbazepin, felbamát, eslikarbazepin -acetát és rufinamid)
- foszaprepitant (hányinger kezelésére szolgáló gyógyszer)
- boszentán (a pulmonális artériák magas vérnyomásának kezelésére szolgáló gyógyszer)
- Orbáncfű (orbáncfű) (depresszió kezelésére használt gyógynövény).
Ha ezen gyógyszerek bármelyikét szedi, akkor kiegészítő fogamzásgátló módszert is alkalmaznia kell (pl. Óvszer, rekeszizom vagy spermicid hab). Ezen gyógyszerek egy részének zavaró hatása a szedés abbahagyása után akár 28 napig is eltarthat. Kérdezze meg kezelőorvosát vagy gyógyszerészét egy másik fogamzásgátló módszerről, ha az EVRA -t a fent felsorolt gyógyszerekkel együtt alkalmazza.
Az EVRA csökkentheti egyes gyógyszerek hatását, például:
- ciklosporint tartalmazó gyógyszerek
- lamotrigin, epilepszia elleni gyógyszer - ez növelheti a görcsök (görcsök) kockázatát
Előfordulhat, hogy kezelőorvosának módosítania kell más gyógyszerek adagját. Kérjen tanácsot kezelőorvosától vagy gyógyszerészétől, mielőtt bármilyen gyógyszert elkezdene szedni.
Figyelmeztetések Fontos tudni, hogy:
Terhesség és szoptatás
- Ne használja ezt a gyógyszert, ha terhes vagy úgy gondolja, hogy terhes
- Ha teherbe esik, azonnal hagyja abba a gyógyszer alkalmazását
- Ne használja ezt a gyógyszert, ha szoptat vagy szoptatni tervez
Ha Ön terhes vagy terhességet tervez, kérje ki kezelőorvosa vagy gyógyszerésze tanácsát, mielőtt elkezdi szedni ezt a gyógyszert.
A készítmény hatásai a gépjárművezetéshez és gépek kezeléséhez szükséges képességekre
A gyógyszer alkalmazása közben gépjárművet vezethet és gépeket kezelhet.
A kombinált hormonális fogamzásgátlók használatával kapcsolatos kockázatok
Az alábbi információk a kombinált fogamzásgátló tablettákra vonatkozó információkon alapulnak. Mivel az EVRA transzdermális tapasz a kombinált fogamzásgátló tablettákban használt hormonokhoz hasonló hormonokat tartalmaz, valószínűleg ugyanazok a kockázatok is. Minden kombinált fogamzásgátló tabletta olyan kockázatokkal jár, amelyek fogyatékosságot vagy halált okozhatnak.
Egy transzdermális tapasz, például az EVRA nem bizonyítottan biztonságosabb, mint a szájon át szedett kombinált hormonális fogamzásgátló tabletta.
Kombinált hormonális fogamzásgátlók és rák
A méhnyakrák
A méhnyakrák gyakoribb a kombinált hormonális fogamzásgátlót szedő nőknél. Ennek azonban más okai is lehetnek, beleértve a szexuális úton terjedő betegségeket.
Mellrák
Megfigyelték, hogy azok a nők, akik kombinált hormonális fogamzásgátlót alkalmaznak, gyakrabban fejlesztenek mellrákot, mint azok, akik nem. Lehetséges azonban, hogy ennek nem a kombinált hormonális fogamzásgátló az oka. Előfordulhat, hogy a kombinált hormonális fogamzásgátlót szedő nők gyakrabban keresik fel orvosukat. Ez azt jelentheti, hogy nagyobb az esély a mellrák diagnosztizálására. A kombinált hormonális fogamzásgátlók használatának abbahagyása után fokozatosan csökken az emlőrák kockázata. Tíz év után az emlőrák esélye megegyezik azokkal a nőkkel, akik soha nem használtak kombinált hormonális fogamzásgátlót.
Májrák
A kombinált hormonális fogamzásgátlót alkalmazó nőknél ritkán jelentettek nem rákos eseteket, és még ritkábban májdaganatok rákos eseteit. Ez a fajta daganat belső vérzést okozhat, súlyos hasi fájdalommal. Ha ez megtörténik, azonnal forduljon orvosához.
Adagolás, az alkalmazás módja és ideje Az Evra alkalmazása: Adagolás
Ezt a gyógyszert mindig pontosan az orvos vagy a gyógyszerész által elmondottaknak megfelelően alkalmazza.
Ha nem, akkor nagyobb a kockázata a teherbeesésnek
Ha nem biztos benne, forduljon orvosához vagy gyógyszerészéhez
Tartson más nem hormonális fogamzásgátlókat (például óvszert, habot vagy spermicid szivacsot) tartalék módszerekként arra az esetre, ha hibákat követ el a tapasz használata közben.
Hány tapaszt használjon
1., 2. és 3. hét: Csak egy tapaszt helyezzen fel, és tartsa pontosan hét napig
4. hét: ezen a héten ne használja a tapaszt.
Ha az előző ciklus során nem használt hormonális fogamzásgátlót
Ezt a gyógyszert a következő ciklus első napján kezdheti el.
Ha egy vagy több nap telt el a menstruáció kezdete óta, beszéljen orvosával a nem hormonális fogamzásgátló ideiglenes alkalmazásáról.
Ha az orális fogamzásgátló tablettáról az EVRA -ra vált
Ha orális fogamzásgátló tablettáról EVRA -ra vált:
- várja meg a menstruációját
- helyezze fel az első tapaszt a menstruáció első 24 órájában.
Ha a tapaszt a menstruáció 1. napja után alkalmazzák:
Nem hormonális fogamzásgátlót is használ a 8. napig, vagyis a tapasz cseréjekor. Ha a menstruációja nem jelenik meg az utolsó fogamzásgátló tabletta bevételét követő 5 napon belül, beszéljen orvosával, mielőtt elkezdi szedni ezt a gyógyszert.
Ha a csak progesztogént tartalmazó tablettáról, implantátumról vagy injekciós módszerről EVRA-ra vált
- Ezt a gyógyszert bármelyik nap elkezdheti a csak progesztogén tabletták abbahagyása vagy az implantátum eltávolításának napján, vagy a következő injekció tervezett napján.
- A tapaszt csak a progesztogén tartalmú tabletták használatának abbahagyását követő első napon, vagy az implantátum eltávolítása után, vagy a következő injekció napján helyezze fel.
- Szintén használjon nem hormonális fogamzásgátlót a 8. napig, vagyis a tapasz cseréjekor.
Vetélés vagy abortusz után a terhesség 20. hete előtt
- Beszéljen orvosával
- Ezt a gyógyszert azonnal elkezdheti
Ha egy vagy több nap telt el a vetélés vagy az abortusz óta, amikor elkezdi szedni ezt a gyógyszert, beszéljen orvosával a nem hormonális fogamzásgátló ideiglenes alkalmazásáról.
Vetélés vagy terhesség utáni abortusz után 20 hetes terhesség után
- Beszéljen orvosával
- Ön dönthet úgy, hogy elkezdi szedni ezt a gyógyszert az indukált abortusz vagy vetélés utáni 21. napon, vagy a menstruáció első napján, attól függően, hogy melyik következik be előbb.
Szülés után
- Beszéljen orvosával
- Ha gyermeke született, és nem szoptat, ne használja ezt a gyógyszert a szülés után négy hétig
- Ha a szülés után több mint négy héttel kezdődik, az első 7 napban a gyógyszer mellett használjon másik nem hormonális fogamzásgátlót
- Ha a szülés után szexelt, várjon az első menstruációval, vagy konzultáljon orvosával, hogy megbizonyosodjon arról, hogy nem terhes, mielőtt elkezdené szedni ezt a gyógyszert
- ha szoptat
- Beszéljen orvosával
- Ne használja ezt a gyógyszert, ha szoptat (lásd 2. pont terhesség és szoptatás).
Fontos információk, amelyeket figyelembe kell venni a tapasz használatakor
- Az EVRA -t minden héten ugyanazon a napon cseréli. A tapasz 7 napig hat
- Soha ne hagyja, hogy 7 egymást követő napnál tovább teljen a tapasz használata nélkül
- Egyszerre csak egy tapaszt használjon
- Semmilyen módon ne vágja le és ne módosítsa a tapaszt
- Kerülje a tapasz felhordását vörös, irritált vagy vágott bőrre
- A tapasznak megfelelően kell tapadnia a bőrhöz, hogy megfelelően működjön
- Erősen nyomja meg a tapaszt, amíg szélei jól tapadnak
- Ne használjon krémet, olajat, krémet, talkumot vagy sminket a bőrön, ahol a tapaszt felhelyezi, vagy a tapasz közelében. Ez valójában a tapasz leválásához vezethet
- Ne helyezzen új tapaszt a bőr ugyanazon területére, mint az imént levett tapaszt. Ellenkező esetben nagyobb az irritáció esélye.
- Minden nap ellenőrizze, hogy nem tapadt -e le a tapasz.
- Ne hagyja abba a tapaszok használatát, még akkor sem, ha csak ritkán szexel.
HOGYAN KELL HASZNÁLNI A TAPASZTOT?
Ha először használja az EVRA -t, várjon a menstruációig.
- Az első tapaszt a menstruáció első 24 órájában helyezze fel
- Ha a tapaszt a menstruáció 1. napja után alkalmazzák, akkor a tapasz cseréjekor a 8. napig nem hormonális fogamzásgátló módszert kell alkalmaznia.
- Az első tapasz felhelyezésének napja az 1. nap lesz. A "Patch Change Day" ugyanazon a napon lesz, minden héten.
Válasszon egy helyet a testén, amelyre felhelyezi a tapaszt.
- A tapaszt mindig tiszta, száraz és szőrtelen bőrre kell felhordani
- Vigye fel a tapaszt a fenékre, a hasra, a külső felkarra vagy a hát felső részére, ahol a szűk ruházat nem fogja dörzsölni.
- Soha ne tegye a tapaszt a mellére.
Ujjaival nyissa ki a fóliatasakot.
- Nyissa ki úgy, hogy széttépi a szélét (ne használjon ollót)
- Most fogja meg erősen a tapasz egyik sarkát, és óvatosan távolítsa el a tapasz tasakjából
- Néha a tapaszok a tasak belsejébe tapadhatnak: vigyázzon, hogy a tapasz eltávolítása közben ne húzza le véletlenül a fóliát
- Most, amint az ábrán látható, húzza le az átlátszó védőfólia felét.
- Kerülje a tapadó felület érintését.
- Helyezze a tapaszt a bőrre.
- Csak ezután húzza le a védőfólia másik felét
- Nyomja meg erősen a tapaszt a tenyerével 10 másodpercig
- Ügyeljen arra, hogy a szélei szorosan illeszkedjenek.
A tapaszt 7 napig (egy hétig) hordja.
- A „Patch Change Day” napon, azaz a 8. napon távolítsa el a használt tapaszt
- Azonnal helyezzen fel egy új tapaszt.
- A 15. napon (3. héten) távolítsa el a használt tapaszt
- Tegyen fel egy új tapaszt.
Összesen három hét van a tapaszok viselésére.
Az irritáció elkerülése érdekében ne helyezze az új tapaszt pontosan ugyanarra a helyre, mint az előző tapaszt.
Ne használjon tapaszokat a 4. héten (22. nap - 28. nap).
- Ebben az időszakban kell a menstruáció
- Ezen a héten védve lesz a terhességtől, de csak akkor, ha időben elkezdi használni a következő tapaszt.
A következő négyhetes ciklus elindításához
- Tegyen fel egy új tapaszt a szokásos "Patch Change Day" napján, amely a 28. nap másnapja
- Nem mindegy, hogy a menstruáció melyik napján kezdődik vagy ér véget.
Ha a "Foltcsere napját" a hét másik napjára kívánja módosítani, beszéljen orvosával.
Be kell fejeznie az aktuális ciklust, és a megfelelő napon el kell távolítania a harmadik tapaszt. A 4. héten választhat egy új "Patch Change Day" -t, és aznap felhelyezheti az első tapaszt. A tapasz viselése nélkül nem szabad több mint 7 egymást követő napon át mennie.
Ha késleltetni szeretné a menstruációját, akkor a 4. hét elején (22. nap) is helyezzen fel tapaszt. Foltos vagy intermenstruális vérzése lehet. Ne viseljen 6 -nál több tapaszt (tehát legfeljebb 6 hétig). ha 6 egymást követő tapaszt viselt (azaz 6 egymást követő héten), ne helyezze fel a 7. hét tapaszt. 7 nap elteltével helyezzen be egy új tapaszt, és kezdje újra a ciklust, tekintve az 1. napnak. menstruációd.
Napi tevékenységek a tapasz használata közben
- A szokásos tevékenységek, például fürdés, zuhanyozás, szauna vagy testmozgás, nem befolyásolhatják a tapasz hatékonyságát.
- A tapaszt úgy tervezték, hogy a helyén maradjon az ilyen típusú tevékenységek során
- Célszerű azonban ellenőrizni, hogy a tapasz nem szakadt -e le, miután részt vett ezekben a tevékenységekben
Ha a javítást egy másik helyre kell felhelyeznie a "Patch Change Day" -től eltérő napon
Ha a használt tapasz kényelmetlenné válik vagy irritációt okoz:
- lehúzhatja, és kicserélheti egy másik helyre felhelyezett új tapaszra a következő "Patch Change Day" -ig
- egyszerre csak egy tapaszt kell használnia.
Ha nehezen emlékszik az EVRA tapasz cseréjére
Beszéljen orvosával, gyógyszerészével vagy egészségügyi szakemberével arról, hogyan könnyítheti meg a tapaszok cseréjét, vagy más fogamzásgátló módszer alkalmazásáról.
Ha a tapasz leválik vagy leválik Kevesebb mint egy nap (legfeljebb 24 óra):
próbálja meg azonnal újra felhelyezni, vagy azonnal helyezzen fel egy új tapaszt, további fogamzásgátló módszer nem szükséges
- már nem tartja be
- önmagához vagy más felülethez rögzítette magát
- egyéb anyagok tapadtak hozzá
- ez a második alkalom, amikor meglazul vagy leválik.
Több mint egy napig (24 órán keresztül vagy tovább), vagy ha nem biztos abban, hogy meddig:
- azonnal kezdjen új, négyhetes ciklust egy új tapasz felhelyezésével
- most lesz az új 1. nap és egy új „Patch Change Day”
- az új ciklus első hetében nem hormonális fogamzásgátló módszert kell alkalmaznia
Teherbe eshet, ha nem tartja be ezeket az utasításokat.
Ha elfelejtette kicserélni a transzdermális tapaszt
Bármely tapasz felhelyezési ciklus elején (1. hét (1. nap)):
Ha elfelejti felhelyezni a tapaszt, különösen nagy a kockázata a teherbeesésnek.
- Ezért egy héten keresztül nem hormonális fogamzásgátló módszert kell alkalmaznia
- Vigye fel az új ciklus első tapaszt, amint eszébe jut
- Most új "javításnap" és új nap lesz.
A tapasz felhelyezési ciklusának közepén (2. vagy 3. hét):
Ha egy vagy két napra (legfeljebb 48 órára) elfelejtette kicserélni a tapaszt:
- helyezzen fel új tapaszt, amint eszébe jut
- helyezze fel a következő tapaszt a szokásos "Patch Change Day" -re. Nincs szükség további fogamzásgátlásra.
Több mint két napig (48 óra vagy több):
- ha több mint 2 napig elfelejti kicserélni a tapaszt, teherbe eshet
- kezdjen egy új, négyhetes ciklust, amint eszébe jut, az új tapasz felhelyezése mostantól eltérő "Patch Change Day" -et és egy új 1. napot tartalmaz
- az új ciklus első hetében további fogamzásgátló módszert kell alkalmaznia.
A tapasz felhelyezési ciklusának végén (4. hét):
Ha elfelejtette eltávolítani a tapaszt:
- távolítsa el a tapaszt, amint eszébe jut
- a következő ciklust a szokásos "Patch Change Day" napján kezdi, ami a 28. nap másnapja.
Nincs szükség további fogamzásgátlásra.
Ha nincs vérzése vagy szabálytalan vérzése az EVRA -val
Ez a gyógyszer váratlan hüvelyi vérzést vagy foltosodást okozhat a tapasz viselése során
- Ez általában az első néhány ciklus után véget ér
- A tapaszok használatával kapcsolatos hibák foltosodást vagy enyhe vérzést okozhatnak
- Folytassa a gyógyszer alkalmazását, és ha a vérzés tovább tart, mint az első három ciklus, beszéljen kezelőorvosával vagy gyógyszerészével.
Ha a menstruációja nem jelenik meg azon a héten, amikor nem visel EVRA -t (4. hét), akkor folytassa az új tapasz felhelyezését a szokásos "Patch Change Day" napján.
- Ha helyesen használja ezt a gyógyszert, és nincs menstruációja, ez nem feltétlenül jelenti azt, hogy terhes
- Ha azonban a menstruációja két egymást követő ciklusban nem fordul elő, beszéljen kezelőorvosával vagy gyógyszerészével, mert terhes lehet.
Túladagolás Mi a teendő, ha túl sok Evra -t vett be?
Ha az előírtnál több EVRA -t alkalmazott (egyszerre több EVRA -tapaszt)
Távolítsa el a tapaszokat, és azonnal forduljon orvosához. A túl sok javítás a következőket okozhatja:
- rossz közérzet (hányinger, hányás)
- hüvelyi vérzés.
Ha idő előtt abbahagyja az EVRA szedését
Előfordulhat, hogy szabálytalan, világos menstruációja van, vagy egyáltalán nincs. Ez általában az első 3 hónapban fordul elő, különösen akkor, ha a menstruációja nem volt rendszeres, mielőtt elkezdte szedni ezt a gyógyszert.
Ha bármilyen további kérdése van a gyógyszer alkalmazásával kapcsolatban, kérdezze meg orvosát, gyógyszerészét vagy a nővért.
Mellékhatások Mik az Evra mellékhatásai?
Mint minden gyógyszer, így az EVRA is okozhat mellékhatásokat, amelyek azonban nem mindenkinél jelentkeznek. Ha Önnél bármilyen mellékhatás jelentkezik, különösen, ha súlyos vagy tartós, vagy ha olyan változás következik be az egészségében, amelyről úgy gondolja, hogy az EVRA okozhatja, kérjük, értesítse orvosát.
Minden kombinált hormonális fogamzásgátlót szedő nőnél fokozott a kockázata a vérrögök kialakulásának a vénákban (vénás thromboembolia (VTE)) vagy az artériákban (artériás thromboembolia (ATE)). A "kombinált hormonális fogamzásgátlók szedésének" különböző kockázataival kapcsolatos részletesebb információkért lásd a 2. pontot "Tudnivalók az EVRA alkalmazása előtt".
Nagyon gyakori mellékhatások (10 nő közül több mint 1 -et érint):
- Fejfájás
- Hányinger
- Kellemetlen érzés a mellben.
Gyakori mellékhatások (10 nő közül kevesebb mint 1 -et érint):
- Hüvelyi gombás fertőzések, néha candidiasisnak nevezik
- Hangulatzavarok, például depresszió, hangulatváltozások, hangulatváltozások, szorongás, sírás
- Szédülés
- Migrén
- Gyomorfájdalom vagy puffadás
- Hányás vagy hasmenés
- Akne, kiütés, viszketés vagy bőrirritáció
- Izomgörcsök
- Mellproblémák, például mellfájdalom, megnagyobbodás vagy csomók
- Változások a menstruációs vérzés jellemzőiben, méhgörcsök, fájdalmas időszakok, hüvelyváladék
- Az alkalmazás helyén fellépő reakciók, például bőrpír, irritáció, viszketés vagy kiütés Fáradtság vagy általános rossz közérzet
- Súlygyarapodás.
Nem gyakori mellékhatások (100 nő közül kevesebb mint 1 -et érint):
- Allergiás reakció, csalánkiütés
- Duzzanat a vízvisszatartás miatt
- Magas zsírszint a vérben (például koleszterin vagy trigliceridek)
- Alvászavarok (álmatlanság)
- A libidó elvesztése
- Ekcéma, bőrpír
- Az anyatej rendellenes termelése
- Premenstruációs szindróma
- Hüvelyi szárazság
- Egyéb reakciók a tapasz felhelyezésének helyén
- Duzzanat
- Magas vérnyomás vagy emelkedett vérnyomás
- Fokozott étvágy
- Hajhullás
- Érzékenység a napfényre.
Ritka mellékhatások (1000 nő közül kevesebb mint 1 -et érint):
- káros vérrögök a vénában vagy az artériában, például: lábszárban (DVT)
- egy tüdőben (PE)
- szívroham
- stroke
- mini-stroke vagy ideiglenes stroke-szerű tünetek, átmeneti ischaemiás roham (TIA) néven
- vérrögök a májban, a gyomorban / a belekben, a vesékben vagy a szemben.
- A vérrög kialakulásának esélye nagyobb lehet, ha más olyan állapota van, amely növeli ezt a kockázatot
- Mell-, méhnyak- vagy májrák
- Problémák, amelyeket a tapasz bőrrel való érintkezése okoz, például kiütések hólyagokkal vagy fekélyekkel
- Nem rákos (jóindulatú) emlő- vagy májdaganatok
- Méh mióma (méh)
- Düh vagy csalódottság érzése
- Fokozott libidó
- Az íz megváltoztatása
- Kontaktlencse viselési problémák
- Hirtelen éles vérnyomásemelkedés (hipertóniás krízis)
- Az epehólyag vagy a vastagbél gyulladása
- Megváltozott sejtek a méhnyakban
- Barnás foltok vagy foltok az arcon
- Epekövek vagy epevezeték -elzáródás
- A bőr és a szemfehérje sárgulása
- Rendellenes vércukorszint vagy inzulinszint
- Az arc, a száj, a torok vagy a nyelv duzzanata
- Kiütések fájdalmas vörös csomókkal a lábszáron és a lábakon
- Viszkető
- Pikkelyes, pelyhes, viszkető és vörös bőr
- A szoptatást elnyomták
- Hüvelyváladék
- Folyadékvisszatartás a lábakban
- Folyadékvisszatartás
- A karok, kezek, lábak vagy lábak duzzanata.
Ha gyomorpanaszai vannak
- Az EVRA által kibocsátott hormonok mennyiségét nem befolyásolhatja hányás vagy hasmenés
- Nem kell további fogamzásgátlást használnia, ha gyomorpanasza van.
Az első 3 ciklus során foltosodás, enyhe vérzés, mellkasi kellemetlen érzés vagy rossz közérzet jelentkezhet. A probléma általában elmúlik, de ha továbbra is fennáll, kérdezze meg kezelőorvosát vagy gyógyszerészét.
Ha Önnél bármilyen mellékhatás jelentkezik, tájékoztassa erről kezelőorvosát, gyógyszerészét vagy a gondozását végző egészségügyi szakembert, beleértve a betegtájékoztatóban fel nem sorolt bármilyen lehetséges mellékhatást is.
Lejárat és megőrzés
A gyógyszer gyermekektől elzárva tartandó!
A csomagoláson feltüntetett lejárati idő (EXP) után ne alkalmazza ezt a gyógyszert. A lejárati idő az adott hónap utolsó napjára vonatkozik.
Az eredeti csomagolásban tárolandó, hogy megvédje a tapaszokat a fénytől és a nedvességtől.
Hűtőszekrényben nem fagyasztható.
A használt tapaszok még aktív hormonokat tartalmaznak. A környezet védelme érdekében gondosan ártalmatlanítani kell őket. A használt tapasz megsemmisítéséhez:
- emelje fel a megsemmisítésre használt címkét a tasak külső oldalán
- helyezze a használt tapaszt az ártalmatlanítás címkéjébe, nyissa ki úgy, hogy a ragadós felület lefedje az árnyékos területet
- zárja le a címkét a használt tapasz lezárásával, és távolítsa el a gyermekektől elzárva.
Semmilyen gyógyszert ne dobjon a szennyvízbe vagy a háztartási hulladékba. Kérdezze meg gyógyszerészét, hogy mit tegyen a már nem használt gyógyszereivel. Ez elősegíti a környezet védelmét.
Forrás betegtájékoztató: AIFA (Olasz Gyógyszerügynökség). A tartalom 2016 januárjában jelent meg. A jelenlévő információk nem feltétlenül naprakészek.
A legfrissebb verzióhoz való hozzáféréshez ajánlatos az AIFA (Olasz Gyógyszerügynökség) webhelyét elérni. Jogi nyilatkozat és hasznos információk.
01.0 A GYÓGYSZER MEGNEVEZÉSE
EVRA transzdermális tapasz 203 mcg / 24 óra + 33,9 mcg / 24 óra
02.0 MINŐSÉGI ÉS MENNYISÉGI ÖSSZETÉTEL
Minden 20 cm2 -es transzdermális tapasz 6 mg norelgestromint (NGMN) és 600 mcg etinilösztradiolt (EE) tartalmaz.
Minden transzdermális tapasz átlagosan 203 mcg NGMN -t és 33,9 mcg EE -t bocsát ki 24 óra alatt.A gyógyszeres expozíciót jobban jellemzi a farmakokinetikai profil (lásd 5.2 pont).
A segédanyagok teljes listáját lásd a 6.1 pontban.
03.0 GYÓGYSZERFORMA
Transzdermális tapasz.
Vékony, mátrixos transzdermális tapasz, amely három rétegből áll.
Az erősítő réteg külső része bézs színű, és "EVRA" felirattal van ellátva.
04.0 KLINIKAI INFORMÁCIÓK
04.1 Terápiás javallatok
Női fogamzásgátlás.
Az EVRA fogamzóképes korú nőknek készült. Hatékonyságát és biztonságosságát 18 és 45 év közötti nőknél állapították meg.
Az EVRA felírására vonatkozó döntésnek figyelembe kell vennie az egyes nők jelenlegi kockázati tényezőit, különösen a vénás thromboemboliával (VTE) kapcsolatos kockázatokat, valamint az EVRA -val és más kombinált kombinált kombinált készítményekkel összefüggő VTE kockázatának összehasonlítását (lásd 4.3 és 4.4 pont).
04.2 Adagolás és alkalmazás
Adagolás
A maximális fogamzásgátló hatás elérése érdekében tájékoztassa a betegeket arról, hogy pontosan az előírt módon kell használniuk az EVRA -t. Az első lépésekhez lásd az alábbi „Első lépések az EVRA -val” című részt.
Egyszerre csak egy transzdermális tapaszt szabad viselni.
Minden használt transzdermális tapaszt el kell távolítani, és azonnal ki kell cserélni egy újat a hét ugyanazon napján (a váltás napján) a ciklus 8. és 15. napján. A transzdermális tapaszt bármikor megváltoztathatja a változás napján. A negyedik héten, a ciklus 22. napjától kezdődően a transzdermális tapaszt nem használják.
Egy új fogamzásgátló ciklus a következő napon kezdődik transzdermális tapasz nélkül; a következő EVRA transzdermális tapaszt is fel kell helyezni, ha nincs vérzés, vagy ha a vérzés még nem állt le.
Soha több mint 7 nap nem telhet el transzdermális tapasz nélkül a ciklusok között.Ha több mint 7 nap telik el, előfordulhat, hogy a felhasználó nem védett a terhességtől. Ebben az esetben ezért nem hormonális fogamzásgátlót kell egyidejűleg használni 7 napig. Az ovuláció kockázata minden nap növekszik az ajánlott fogamzásgátló időszakon túl. Abban az esetben, ha ilyen hosszan tartó, transzdermális tapasz nélküli szexuális életet folytat, mérlegelni kell a terhesség lehetőségét.
Különleges populációk
Testtömege 90 kg vagy annál nagyobb
A fogamzásgátló hatás csökkenhet 90 kg vagy annál nagyobb súlyú nőknél.
Veseelégtelenség
Az EVRA -t nem vizsgálták veseelégtelenségben szenvedő nőknél. Az adag módosítása nem szükséges, de mivel az orvosi szakirodalom azt sugallja, hogy az etinilösztradiol szabad frakciója magasabb, az EVRA -t ezen gondosan ellenőrzött populációnak kell beadni.
Májelégtelenség
Az EVRA -t nem vizsgálták májelégtelenségben szenvedő nőknél. Az EVRA ellenjavallt májkárosodásban szenvedő nőknél (lásd 4.3 pont).
Posztmenopauzális nők
Az EVRA nem javallott posztmenopauzás nőknél, és nem alkalmazható hormonpótló terápiaként.
Gyermekpopuláció
A biztonságosságot és a hatásosságot 18 év alatti serdülőknél nem állapították meg. Az EVRA alkalmazása a menarche előtti gyermekek és serdülők esetében nem releváns.
Az alkalmazás módja
Az EVRA -t tiszta, száraz, szőrtelen, ép és egészséges bőrre kell felvinni a fenékre, a hasra, a felkar külső karjára vagy a felső törzsre olyan helyen, ahol nem fogja dörzsölni szűk ruházat. vagy vörös, irritált vagy vágott bőrre Az egymást követő EVRA transzdermális tapaszokat a bőr különböző részeire kell felhelyezni az irritáció elkerülése érdekében, de ugyanazon anatómiai területen maradhatnak.
Erősen nyomja a transzdermális tapaszt, amíg a szélei jól tapadnak.
A transzdermális tapasz tapadási tulajdonságaiba való beavatkozás megakadályozása érdekében nem szabad sminket, krémet, testápolót, talkumot vagy más helyi terméket alkalmazni arra a bőrfelületre, ahol a transzdermális tapaszt felhelyezték, vagy ahol fel kívánják helyezni. .
Javasoljuk, hogy a felhasználók minden nap szemrevételezéssel vizsgálják meg a transzdermális tapaszt, hogy biztosítsák a megfelelő tapadást.
Az EVRA transzdermális tapaszt nem szabad levágni, megsérteni vagy megváltoztatni, mivel az veszélyeztetheti a fogamzásgátló hatékonyságát.
A használt transzdermális tapaszokat óvatosan kell megsemmisíteni a 6.6 pontban leírtak szerint.
Hogyan kell elkezdeni az EVRA -t?
Ha az előző ciklusban nem alkalmaztak hormonális fogamzásgátlót
A fogamzásgátlás az EVRA -val a menstruáció első napján kezdődik. Egyetlen transzdermális tapaszt kell felhelyezni és egy teljes héten (7 nap) viselni. Az első transzdermális tapasz felhelyezésének napja (1. nap / kezdő nap) határozza meg a következő cserenapokat. A transzdermális tapasz cseréjének napja minden héten ugyanaz lesz (a ciklus 8., 15., 22. napja és a következő ciklus 1. napja). A transzdermális tapaszt nem használják a negyedik héten, a ciklus 22. napjától kezdve.
Csak az első kezelési ciklusban, ha az 1. ciklus terápiája a menstruáció első napja után kezdődik, nem hormonális fogamzásgátlót kell használni egyidejűleg az első 7 egymást követő napon.
Ha áttér a kombinált orális fogamzásgátlóra
Az EVRA -kezelést az elvonási vérzés első napján kell elkezdeni. Ha az utolsó aktív (hormonokat tartalmazó) tabletta bevételét követő 5 napon belül nincs elvonási vérzés, a kezelés megkezdése előtt ki kell zárni a terhesség lehetőségét. az elvonási vérzés első napja után kezdődik, nem hormonális fogamzásgátló eszközöket kell használni az EVRA-val együtt 7 napon keresztül.
Ha több mint 7 nap telt el az utolsó aktív fogamzásgátló tabletta bevétele óta, lehetséges, hogy a nő peteérést kapott. Ezért tájékoztassa Önt, hogy az EVRA -kezelés megkezdése előtt konzultálnia kell orvosával. Ha a nő szexuális érintkezésben volt egy ilyen meghosszabbított tablettamentes időszak alatt, akkor figyelembe kell venni a terhesség lehetőségét.
Ha csak progesztogént tartalmazó módszerről vált át
A felhasználó bármelyik napon válthat a csak progesztogént tartalmazó tablettáról (implantátum esetén az eltávolítás napjától és attól a naptól, amikor az injekciót be kellett adni injekciós fogamzásgátló módszer esetén), azonban az első 7 napig további fogamzásgátló módszert kell alkalmaznia.
Indukált vagy spontán abortusz után
A terhesség 20. hete előtt bekövetkezett indukált vagy spontán vetélést követően a felhasználó azonnal elkezdheti használni az EVRA -t. Ha az EVRA -t azonnal elkezdik, nincs szükség további fogamzásgátló intézkedésekre. Kérjük, vegye figyelembe, hogy az ovuláció az indukált vagy spontán abortusz után 10 napon belül bekövetkezhet .
Abban az esetben, ha a terhesség 20. hetében vagy később következik be az indukált vagy spontán vetélés, az EVRA -t az abortusz utáni 21. napon, vagy az első spontán menstruáció első napján lehet elkezdeni, attól függően, hogy melyik következik be előbb. az abortusz utáni 21. nap (a terhesség 20. hetében).
Szülés után
Azok a felhasználók, akik nem szoptatnak, kezdjék el a fogamzásgátló kezelést az EVRA -val legkorábban 4 héttel a szülés után. Később jelentkezzen, és tájékoztassa a felhasználót arról, hogy az első 7 napon további gátló módszert kell alkalmazni, de ha már megtörtént a közösülés, zárja ki a terhesség lehetőségét, mielőtt elkezdené az EVRA -t, vagy várja meg az első időszakot.
Szoptató nőknél lásd a 4.6 pontot.
Mi a teendő, ha a transzdermális tapasz részben vagy teljesen leválik?
Ha az EVRA transzdermális tapasz részben vagy teljesen leválik, és leválik, a leszállított gyógyszer mennyisége nem lesz elegendő.
Ha az EVRA még csak részben is leválik:
• egy napnál rövidebb ideig (legfeljebb 24 óra): újra fel kell helyezni ugyanazon a helyen, vagy azonnal le kell cserélni egy új EVRA transzdermális tapaszra. Egyéb fogamzásgátló intézkedésekre nincs szükség. Helyezze fel a következő EVRA transzdermális tapaszt a szokásos "változás napján".
• több mint egy napig (24 órán keresztül vagy tovább), vagy ha a felhasználó nem tudja, hogy a transzdermális tapasz mikor emelkedett le vagy vált le: előfordulhat, hogy a felhasználó nem védett a terhesség ellen. A felhasználónak le kell állítania a fogamzásgátló ciklust, és azonnal el kell kezdenie egy újat, új EVRA transzdermális tapasz felhelyezésével. Most új „1. nap” és új „váltási nap” van. Egyidejűleg nem hormonális fogamzásgátló módszert is alkalmazni kell csak az új ciklus első 7 napjára.
A transzdermális tapaszt nem szabad újra felhelyezni, ha már nem tapadó, azonnal cserélje ki egy újat. Semmilyen más ragasztót vagy kötést nem szabad használni az EVRA transzdermális tapasz rögzítéséhez.
Késések esetén az EVRA transzdermális tapaszok következő cseréjében
Bármely transzdermális tapaszt tartalmazó ciklus elején (első hét / 1. nap):
Előfordulhat, hogy a felhasználó nem védett a terhességgel szemben. Amint eszébe jut, fel kell helyeznie az új ciklus első transzdermális tapaszát. Most új "változás napja" és új "1. nap" van. Hormonális a kezelés első 7 napjában az új ciklus Abban az esetben, ha ilyen hosszan tartó, transzdermális tapasz nélküli szexuális életet folytat, mérlegelni kell a terhesség lehetőségét.
Ciklus közepén (második hét / 8. nap vagy harmadik hét / 15. nap):
• egy -két napig (legfeljebb 48 óráig): A felhasználónak azonnal fel kell helyeznie egy új EVRA transzdermális tapaszt. A következő EVRA transzdermális tapaszt a szokásos "cserélési napon" kell felhelyezni. Ha az első napot megelőző 7 nap során a transzdermális tapaszt nem helyezték fel, a felhasználó megfelelően viselte a tapaszt, nincs szükség további fogamzásgátló intézkedésekre.
• több mint két napig (48 órán keresztül vagy tovább): előfordulhat, hogy a felhasználó nem védett a terhességgel szemben. Abba kell hagynia a jelenlegi fogamzásgátló ciklust, és azonnal el kell kezdenie egy új, négyhetes ciklust egy új EVRA transzdermális tapasz alkalmazásával. legyen egy új "1. nap" és egy új "cserenap". Nem hormonális fogamzásgátlót kell használni egyidejűleg az új ciklus első 7 egymást követő napján.
• a ciklus végén (4. hét / 22. nap): Ha a felhasználó nem távolítja el az EVRA transzdermális tapaszt a 4. hét elején (22. nap), akkor a lehető leghamarabb el kell távolítania. A következő ciklust a szokásos "cserenappal" kell kezdeni, azaz a 28. nap utáni napon. További fogamzásgátló intézkedések nem szükségesek.
A csere napjának megváltoztatásához
Ha a felhasználó egyszer el akarja halasztani a menstruációját, akkor a 4. hét elején (22. nap) kell felhelyeznie egy másik transzdermális tapaszt, így nem tartja be a tapaszmentes intervallumot.A transzdermális tapasz 6 egymást követő héten történő viselése után 7 napos tapaszmentes intervallumot kell tartani. Ezután folytatódik az EVRA rendszeres alkalmazása.
Ha a felhasználó meg akarja változtatni a váltás napját, akkor a megfelelő cikluson kell befejeznie a harmadik EVRA transzdermális tapasz eltávolítását a megfelelő napon. A transzdermális tapasz nélküli intervallumban az első EVRA transzdermális tapasz felhelyezésével új váltási napot választhat a következő ciklusban, amint elérkezik a kívánt nap. Soha több mint 7 nap nem telhet el a transzdermális tapasz nélkül. Minél rövidebb a tapaszmentes intervallum, annál nagyobb a kockázata annak, hogy a felhasználónak nem lesz elvonási vérzése, helyette metrorrhagia és foltosodás lesz a következő kezelési ciklus során.
Enyhe bőrirritáció esetén
Ha a transzdermális tapasz használata "zavaró irritációt okoz, akkor a következő cserélési nap eléréséig új transzdermális tapaszt lehet felhelyezni egy másik részre". Egyszerre csak egy transzdermális tapaszt szabad használni.
04.3 Ellenjavallatok
Kombinált hormonális fogamzásgátlók (kombinált hormonális fogamzásgátlók, COC) nem használható az alábbi feltételek mellett. Ha ezen tünetek bármelyike jelentkezik az EVRA alkalmazása során, azonnal hagyja abba a használatot.
• Vénás thromboembolia (VTE) jelenléte vagy kockázata
• Vénás thromboembolia - jelenlegi (véralvadásgátló bevitel mellett) vagy korábbi VTE (pl. Mélyvénás trombózis [DVT] vagy tüdőembólia [PE])
• Ismert örökletes vagy szerzett hajlam a vénás tromboembóliára, például rezisztencia az aktivált C -fehérjével (beleértve a Leiden V faktorral), antitrombin III -hiány, C -fehérjehiány, S -proteinhiány
• Nagy műtét hosszan tartó immobilizációval (lásd 4.4 pont)
• Nagy a vénás thromboembolia kockázata, több kockázati tényező jelenléte miatt (lásd 4.4 pont)
• Artériás thromboembolia (ATE) jelenléte vagy kockázata
• Artériás thromboembolia - jelenlegi vagy korábbi artériás thromboembolia (pl. Miokardiális infarktus) vagy prodromális állapotok (pl. Angina pectoris)
• Cerebrovascularis betegség - jelenlegi vagy korábbi stroke vagy prodromális állapotok (pl. Átmeneti ischaemiás roham)átmeneti ischaemiás roham, TIA))
• Ismert örökletes vagy szerzett hajlam az artériás thromboemboliára, például hiperhomociszteinémia és antifoszfolipid antitestek (antikardiolipin antitestek, lupus antikoagulánsok)
• Fokális neurológiai tünetekkel járó migrén
• Nagy az artériás thromboembolia kockázata több kockázati tényező jelenléte miatt (lásd 4.4 pont), vagy olyan súlyos kockázati tényező jelenléte miatt, mint:
• cukorbetegség érrendszeri tünetekkel
• súlyos magas vérnyomás
• súlyos dyslipoproteinemia
• Túlérzékenység a hatóanyagokkal vagy a 6.1 pontban felsorolt bármely segédanyaggal szemben.
• Ismert vagy feltételezett mellrák
• Endometriális rák vagy más ismert vagy feltételezett ösztrogénfüggő daganat
• Akut vagy krónikus hepatocelluláris betegséggel összefüggésben megváltozott májfunkció
• Májadenómák vagy karcinómák
• Nem diagnosztizált rendellenes genitális vérzés
04.4 Különleges figyelmeztetések és a használathoz szükséges óvintézkedések
Figyelmeztetések
Ha az alább felsorolt állapotok vagy kockázati tényezők bármelyike fennáll, az EVRA alkalmasságát meg kell beszélni a nővel.
Ezen kockázati tényezők vagy állapotok bármelyikének súlyosbodása vagy első megjelenése esetén a nőnek fel kell vennie a kapcsolatot orvosával, hogy eldöntse, abba kell -e hagyni az EVRA alkalmazását.
Nincs klinikai bizonyíték arra, hogy a transzdermális tapasz bármilyen szempontból biztonságosabb, mint a COC.
Az EVRA nem javallt terhesség alatt (lásd 4.6 pont).
A vénás thromboembolia (VTE) kockázata
Bármilyen kombinált hormonális fogamzásgátló (COC) alkalmazása a vénás thromboembolia (VTE) kockázatának növekedését eredményezi a használathoz képest. A levonorgesztrelt, norgesztimátot vagy noretiszteront tartalmazó termékek alacsonyabb VTE -kockázathoz társulnak. Az EVRA is kettős lehet. Az alacsonyabb VTE -kockázattal járó termékek használatától eltérő döntést csak a nővel folytatott megbeszélések után szabad meghozni annak biztosítása érdekében, hogy megértse az EVRA -val kapcsolatos VTE kockázatát. tényezők befolyásolják ezt a kockázatot, és az a tény, hogy a VTE kialakulásának kockázata a használat első évében a legmagasabb.
10 000 nő közül körülbelül 2 -nek, akik nem használnak kombinált kombinált kombinációt, és nem terhesek, VTE alakul ki egy év alatt. Egy egyedülálló nő esetében azonban a kockázat sokkal magasabb lehet, az alapul szolgáló kockázati tényezőktől függően (lásd alább).
Becslések szerint 10 000 olyan nő közül, akik alacsony dózisú levonorgesztrelt tartalmazó CHC-t használnak, körülbelül 6 [1] -ben alakul ki VTE egy év alatt. Tanulmányok azt sugallták, hogy a VTE előfordulási gyakorisága az EVRA-t szedő nőknél akár kétszer nagyobb, mint a levonorgesztrelt tartalmazó COC-k esetében. Ezek az értékek körülbelül 6-12 VTE évente 10 000 EVRA-t használó nő esetében.
[1] A 10 000 nőre / évre eső 5-7 tartomány medián értéke, a levonorgesztrelt tartalmazó COC-k körülbelül 2,3-3,6 közötti relatív kockázatán alapul, a nem használthoz képest
Mindkét esetben a VTE -k száma évente alacsonyabb, mint a terhes vagy szülés utáni nőknél várható.
A VTE az esetek 1-2% -ában halálos kimenetelű lehet.
Nagyon ritkán jelentettek trombózist más erekben, például máj-, mesenterikus, vese- vagy retina -vénákban és artériákban a CHC -t alkalmazó betegeknél.
A VTE kockázati tényezői
A vénás tromboembóliás szövődmények kockázata a kombinált kombinált kombinációban részesülőknél jelentősen megnőhet, ha további kockázati tényezők vannak jelen, különösen, ha egynél több kockázati tényező van (lásd a táblázatot).
Az EVRA ellenjavallt, ha egy nőnek számos kockázati tényezője van, amelyek növelik a vénás trombózis kockázatát (lásd 4.3 pont). Ha egy nőnek több kockázati tényezője van, lehetséges, hogy a megnövekedett kockázat nagyobb, mint az egyes tényezők összege; ebben az esetben figyelembe kell venni a VTE teljes kockázatát. Ha az előny / kockázat arány negatívnak tekinthető COC -t nem szabad felírni (lásd 4.3 pont).
Táblázat: A VTE kockázati tényezői
Nincs egyetértés a visszerek és a felszíni thrombophlebitis lehetséges szerepében a vénás trombózis kialakulásában és progressziójában.
Figyelembe kell venni a tromboembólia fokozott kockázatát a terhesség alatt, különösen a gyermekágyi időszak 6 hetes időszakában (a "Terhesség és szoptatás" témával kapcsolatos információkat lásd a 4.6 pontban.
A VTE tünetei (mélyvénás trombózis és tüdőembólia)
Ha ilyen tünetek jelentkeznek, a nőknek azonnal orvoshoz kell fordulniuk, és tájékoztatniuk kell őket, hogy kombinált kombinált fogamzásgátlót szednek.
A mélyvénás trombózis (DVT) tünetei a következők lehetnek:
• a láb és / vagy a láb egyoldalú duzzanata vagy a láb vénája mentén;
• fájdalom vagy érzékenység a lábban, amely csak állva vagy járáskor érezhető;
• fokozott hőérzet az érintett lábon; vörös vagy elszíneződött bőr a lábán.
A tüdőembólia (PE) tünetei a következők lehetnek:
• hirtelen és megmagyarázhatatlan légszomj és gyors légzés;
• hirtelen köhögés, amely hemoptysissel járhat;
• éles fájdalom a mellkasban;
• súlyos szédülés vagy szédülés;
• gyors vagy szabálytalan szívverés.
Ezen tünetek némelyike (például a „légszomj” és a „köhögés”) nem specifikus, és tévesen értelmezhető gyakoribb vagy kevésbé súlyos eseményként (pl. Légúti fertőzések).
Az erek elzáródásának egyéb jelei lehetnek: hirtelen fájdalom, duzzanat vagy az egyik végtag halványkék elszíneződése.
Ha az elzáródás a szemben történik, a tünetek a látás fájdalommentes homályosodásától a látásvesztésig terjedhetnek. Néha a látásvesztés szinte azonnal bekövetkezik.
Az artériás thromboembolia (ATE) kockázata
Az epidemiológiai vizsgálatok összefüggésbe hozták a CHC -k alkalmazását az artériás thromboembolia (miokardiális infarktus) vagy az agyi érrendszeri balesetek (pl. Átmeneti ischaemiás roham, stroke) fokozott kockázatával.
Az ATE kockázati tényezői
Az artériás tromboembóliás szövődmények vagy cerebrovaszkuláris balesetek kockázata a kombinált kombinált kombinációban részesülőknél megnő a kockázati tényezők jelenlétében (lásd a táblázatot). Az EVRA ellenjavallt, ha egy nőnek van egy súlyos kockázati tényezője vagy több ATE kockázati tényezője, amelyek növelik az artériás trombózis kockázatát (lásd 4.3 pont). Ha egy nőnek több kockázati tényezője van, lehetséges, hogy a kockázat növekedése nagyobb, mint az egyes tényezők összege; ebben az esetben a teljes kockázatát kell figyelembe venni. Ha az előny / kockázat egyensúly negatívnak tekinthető, nem szabad kombinált kombinált gyógyszert felírni (lásd 4.3 pont).
Táblázat: Az ATE kockázati tényezői
Az ATE tünetei
Ha ilyen tünetek jelentkeznek, a nőknek haladéktalanul fel kell venniük a kapcsolatot egy egészségügyi szakemberrel, és tájékoztatniuk kell őket, hogy kombinált kombinált fogamzásgátlót szednek.
Az agyi érrendszeri baleset tünetei a következők lehetnek:
• az arc, a kar vagy a láb hirtelen zsibbadása vagy gyengesége, különösen a test egyik oldalán;
• hirtelen járási nehézség, szédülés, egyensúly vagy koordináció elvesztése;
• hirtelen zavartság, beszéd- vagy megértési nehézség;
• hirtelen látászavar az egyik vagy mindkét szemben;
• hirtelen, súlyos vagy elhúzódó, ismeretlen okú migrén;
• eszméletvesztés vagy ájulás görcsökkel vagy anélkül.
Az ideiglenes tünetek arra utalnak, hogy ez egy átmeneti ischaemiás roham (TIA).
A szívinfarktus tünetei a következők lehetnek:
• fájdalom, kellemetlen érzés, nyomás, nehézség, szorító érzés vagy teltség a mellkasban, karban vagy a mellkas alatt;
• a hátba, állkapocsba, torokba, karba, gyomorba sugárzó kellemetlen érzés;
• teltségérzet, emésztési zavar vagy fulladás;
• izzadás, hányinger, hányás vagy szédülés;
• extrém gyengeség, szorongás vagy légszomj;
• gyors vagy rendszertelen szívverés.
A kombinált fogamzásgátlót alkalmazó nőknek trombózis lehetséges tünetei esetén fel kell venniük a kapcsolatot orvosukkal. Kezdjen megfelelő fogamzásgátlást az antikoaguláns terápia (kumarinok) teratogenitása miatt.
Daganatok
Egyes epidemiológiai vizsgálatokban a méhnyakrák megnövekedett kockázatáról számoltak be hosszú távú COC-használóknál, de továbbra is ellentmondásos, hogy ez a megállapítás milyen mértékben tulajdonítható a szexuális viselkedés zavaró hatásának és más tényezőknek, például az emberi papillomavírusnak (HPV ).
54 epidemiológiai vizsgálat metaanalízise valamivel nagyobb kockázatot (RR = 1,24) jelentett az emlőrák diagnosztizálásáról a jelenleg COC-t használó nők körében. A túlzott kockázat fokozatosan eltűnik a COC -használat abbahagyását követő 10 év során. A COC -t használó nőknél diagnosztizált emlőrák klinikailag kevésbé fejlett, mint azoknál a rákos megbetegedéseknél, akik soha nem szedtek COC -t: A megfigyelt magasabb kockázati minta annak köszönhető, hogy a COC -kezelésben részesülőknél korai időben diagnosztizálták a mellrákot, a biológiai hatásokat. COC -k, vagy mindkettő kombinációja.
Ritka esetekben jóindulatú májdaganatokról, és még ritkább esetekben rosszindulatú májdaganatokról számoltak be a COC -használók körében. Izolált esetekben ezek a daganatok életveszélyes intraabdominális vérzésekhez vezettek. Ezért vegye figyelembe a májrák lehetőségét a differenciáldiagnosztikában, ha egy EVRA-felhasználó súlyos felső hasi fájdalmat, májnagyobbodást vagy intraabdominális vérzés jeleit észleli.
Más feltételek
• A fogamzásgátló hatás csökkenhet 90 kg vagy annál nagyobb súlyú nőknél (lásd 4.2 és 5.1 pont).
• A hipertrigliceridémiában szenvedő nőknek vagy a családban előfordult nőknek fokozott a hasnyálmirigy -gyulladás kockázata kombinált hormonális fogamzásgátlók alkalmazása közben.
• Bár sok hormonális fogamzásgátlót szedő nőnél kismértékű vérnyomásemelkedésről számoltak be, klinikailag jelentős emelkedés ritka. A hormonális fogamzásgátlók alkalmazása és a klinikai magas vérnyomás között nincs végleges kapcsolat. Ha a kombinált hormonális fogamzásgátló alkalmazása során, fennálló magas vérnyomás jelenlétében, folyamatosan magas vérnyomás vagy jelentős vérnyomás-emelkedés nem reagál megfelelően a vérnyomáscsökkentő kezelésre, hagyja abba a kombinált hormonális fogamzásgátló alkalmazását. Ez a használat folytatható, ha lehetséges a vérnyomáscsökkentő terápia segítségével normotenzív értékeket elérni.
• Az alábbi állapotok megjelenését vagy romlását jelentették mind a terhesség, mind a COC alkalmazása során. A COC -kezeléssel való összefüggés bizonyítékai azonban nem meggyőzőek: sárgaság és / vagy viszketés, amelyek kolesztiázissal járnak együtt; porfíria; szisztémás lupus erythematosus; hemolitikus urémiás szindróma; Sydenham chorea; herpes gestationis; otosclerosishoz kapcsolódó halláskárosodás.
• Akut vagy krónikus májműködési zavarok szükségessé tehetik a kombinált hormonális fogamzásgátlók felfüggesztését, amíg a májfunkció markerei vissza nem térnek a normál értékekhez.
• Bár a kombinált hormonális fogamzásgátlók hatással lehetnek a perifériás inzulinrezisztenciára és a glükóztoleranciára, nincs bizonyíték arra, hogy a kombinált hormonális fogamzásgátlás alkalmazása során módosítani kellene a kezelési rendet cukorbetegeknél. A cukorbetegeket azonban gondosan figyelni kell, különösen az EVRA használatának korai szakaszában.
• Endokén depresszió, epilepszia, Crohn -betegség és fekélyes vastagbélgyulladás súlyosbodásáról számoltak be a COC alkalmazása során.
• Időnként chloasma léphet fel hormonális fogamzásgátlás alkalmazásával, különösen azoknál a felhasználóknál, akiknek kórelőzményében chloasma gravidarum szerepel. A chloasma gyakran nem teljesen visszafordítható.
Orvosi vizsgálatok / látogatások
Mielőtt elkezdené vagy folytatná az EVRA alkalmazását, fel kell venni a teljes kórtörténetet (beleértve a családi anamnézist is), és ki kell zárni a terhességet. Meg kell mérni a vérnyomást, és el kell végezni az ellenjavallatok alapján végzett klinikai vizsgálatot (lásd 4.3 pont) és figyelmeztetésekre (lásd 4.4 pont). Fontos felhívni a nők figyelmét a vénás vagy artériás trombózisra vonatkozó információkra, beleértve az EVRA -val kapcsolatos kockázatot más kombinált kombinált kombinációkkal összehasonlítva, a VTE és az ATE tüneteit, az ismert kockázati tényezőket és az esetleges teendőket trombózis gyanúja miatt.
A nőt arra is figyelmeztetni kell, hogy figyelmesen olvassa el a betegtájékoztatót, és kövesse annak tanácsait. A vizsgálatok gyakoriságának és típusának megállapított iránymutatásokon kell alapulnia, és azokat az egyes nőkhöz kell igazítani.
A nőket tájékoztatni kell, hogy az orális fogamzásgátlók nem védenek a HIV -fertőzések (AIDS) és más nemi betegségek ellen.
Szabálytalan vérzés
Mint minden kombinált hormonális fogamzásgátló esetében, szabálytalan vérveszteség (foltosodás vagy áttöréses vérzés) fordulhat elő, különösen a használat első hónapjaiban. Emiatt a szabálytalan vérveszteségről szóló orvosi vélemény csak akkor lesz hasznos, ha körülbelül egy három ciklusos kiigazítási időszakot végeznek el. Fontolja meg az EVRA-t. Fontolja meg a nem hormonális okokat, és szükség esetén tegye meg a megfelelő diagnosztikai intézkedéseket, hogy kizárja a szerves betegségek vagy terhesség jelenlétét. Ezek az intézkedések magukban foglalhatják a curettage-t is. Egyes nőknél előfordulhat, hogy nem vérzik a szuszpenzió a transzdermális tapasz használati időköze. Ha az EVRA -t a 4.2 pontban leírtak szerint szedte, nem valószínű, hogy a nő terhes. Ha azonban az EVRA -t nem az ezen utasítások szerint szedték az első kihagyott vérzés előtt, vagy ha a nő két egymást követő elvonási vérzést hagyott ki, akkor az EVRA alkalmazása előtt ki kell zárni a terhességet.
Egyes felhasználóknál amenorrhoea vagy oligomenorrhea jelentkezhet a hormonális fogamzásgátlás abbahagyása után, különösen akkor, ha ezek a feltételek már fennálltak.
04.5 Kölcsönhatások más gyógyszerekkel és más interakciók
jegyzet: A lehetséges kölcsönhatások azonosítása érdekében tanulmányozza az egyidejűleg alkalmazott gyógyszerek felírási információit.
Más gyógyszerek hatása az EVRA -ra
Az orális fogamzásgátlók és más gyógyszerek közötti kölcsönhatások vérveszteséghez és / vagy a fogamzásgátló védelem kudarcához vezethetnek. Az alábbi kölcsönhatásokról számoltak be az irodalomban.
A máj anyagcseréje
Interakciókat figyelhetnek meg a májenzimeket indukáló gyógyszerekkel, amelyek a nemi hormonok (például fenobarbitál, primidon, rifampicin, rifabutin, boszentán, (fos) aprepitant), egyes epilepsziaellenes szerek (pl. Karbamazepin), eslikarbazepin-acetát, felbamát fokozódásához vezethetnek , oxikarbazepin, fenitoin, rufinamid, topiramát) és néhány HIV kezelésére szolgáló gyógyszer (pl. nelfinavir, ritonavir, nevirapin, efavirenz), esetleg griseofulvin és orbáncfüvet tartalmazó készítmények (Hypericum perforatum). A maximális enzimindukció általában körülbelül 10 nap múlva következik be, de a kezelés abbahagyása után legalább 4 hétig fennmaradhat.
Ne használjon orbáncfüvet tartalmazó gyógynövénykészítményeket (Hypericum perforatum) az EVRA használata közben.
Beavatkozás az enterohepatikus körbe
A fogamzásgátlás meghiúsulásának eseteit is jelentették antibiotikumokkal, például penicillinekkel és tetraciklinekkel. Ennek a hatásnak a mechanizmusa még nem világos. Egy farmakokinetikai interakciós vizsgálatban a tetraciklin -hidroklorid 500 mg szájon át történő beadása, naponta négyszer, 3 napon keresztül az EVRA alkalmazási időszaka előtt és 7 napon keresztül ezen időszak alatt, nem befolyásolta jelentősen a norelgesztromin vagy az etinil -ösztradiol farmakokinetikáját.
Menedzsment
Azok a nők, akik rövid ideig kezelnek a fenti osztályok valamelyikébe tartozó gyógyszerekkel vagy májenzimeket indukáló hatóanyagokkal (kivéve a rifampicint), ideiglenesen gátló módszert kell alkalmazniuk az EVRA mellett, azaz az egyidejű alkalmazás ideje alatt ezeknek a gyógyszereknek és 7 napig a kezelés abbahagyása után. A rifampicinnel kezelt nők esetében az EVRA mellett a rifampicin -periódussal együtt és annak abbahagyását követő 28 napon keresztül gátló módszert kell alkalmazni.
Azoknál a nőknél, akik hosszú ideig kezelik a fenti osztályok valamelyikébe tartozó gyógyszereket, ajánlott egy másik hatékony, nem hormonális fogamzásgátló módszert alkalmazni.
Az antibiotikum -kezelésben részesülő nőknek (a rifampicin kivételével, lásd fent) a gátló módszert kell alkalmazniuk a gyógyszer abbahagyása után legfeljebb 7 napig.
Ha az egyidejű gyógyszeres kezelés a tapaszkezelési hét végén is folytatódik, az új tapaszt azonnal fel kell helyezni, új kezelést kell kezdeni, a szokásos tapaszmentes időköz betartása nélkül.
Az etinilösztradiol metabolizmusának gátlása
Kimutatták, hogy az etorikoxib növeli az etinil -ösztradiol plazmaszintjét (50-60%), ha háromfázisú orális hormonális fogamzásgátlóval együtt alkalmazzák. Az etorikoxib a szulfotranszferáz aktivitás gátlásával növeli az etinilösztradiol szintjét, ezáltal gátolja az etinilösztradiol metabolizmusát.
Az EVRA hatása más gyógyszerekre
A hormonális fogamzásgátlók befolyásolhatják egyes hatóanyagok anyagcseréjét. Következésképpen a plazma- és szövetkoncentrációk növekedhetnek (pl. Ciklosporin). Előfordulhat, hogy az egyidejűleg alkalmazott gyógyszer adagját módosítani kell.
Lamotrigin: A kombinált hormonális fogamzásgátlók együttes alkalmazásakor a lamotrigin plazmakoncentrációjának jelentős csökkenését mutatták, valószínűleg a lamotrigin-glükuronidáció indukciója miatt. Ez csökkentheti a görcsök kontrollját, ezért szükségessé válhat a lamotrigin adagjának módosítása.
Laboratóriumi teszt
A fogamzásgátló hatású szteroid hormonok alkalmazása befolyásolhatja egyes laboratóriumi vizsgálatok eredményeit, beleértve a máj, a pajzsmirigy, a mellékvese és a veseműködés biokémiai paramétereit, a fehérjék (hordozók) plazmaszintjét, mint például a vérkötő globulin-kortikoszteroidok és lipid / lipoprotein frakciók, a szénhidrát -anyagcsere paraméterei, valamint a koaguláció és a fibrinolízis paraméterei Az eltérések általában a normál laboratóriumi határokon belül maradnak.
04.6 Terhesség és szoptatás
Terhesség
Az EVRA nem javallt terhesség alatt.
Az epidemiológiai vizsgálatok azt mutatják, hogy nem nagyobb a születési rendellenességek kockázata azoknál a gyermekeknél, akik olyan nőknél születtek, akik terhesség előtt szedtek COC -t. Ezenkívül a legújabb vizsgálatok nem mutattak ki teratogén hatást, ha a terhesség korai szakaszában véletlenül COC -ket alkalmaznak.
Az EVRA -val kezelt nők terhességre gyakorolt hatásairól rendelkezésre álló korlátozott adatok nem vonnak le következtetéseket a transzdermális tapasz terhesség alatti biztonságosságára vonatkozóan.
Állatkísérletek nemkívánatos hatásokat mutattak a terhesség és a szoptatás ideje alatt (lásd 5.3 pont). Ezen állatkísérletek alapján nem zárható ki a hatóanyagok hormonális hatása miatt fellépő nemkívánatos hatások. A terhesség alatti COC -kkel kapcsolatos általános tapasztalatok azonban nem bizonyítottak valódi káros hatást az emberekre.
Ha teherbe esik az EVRA szedése alatt, azonnal hagyja abba az EVRA alkalmazását.
Az EVRA folytatásakor figyelembe kell venni a VTE kockázatát a szülés utáni időszakban (lásd 4.2 és 4.4 pont).
Etetési idő
A szoptatást befolyásolhatják a kombinált hormonális fogamzásgátlók, mivel ezek csökkenthetik az anyatej mennyiségét és megváltoztathatják az anyatej összetételét, ezért az EVRA alkalmazása nem ajánlott azoknak az anyáknak, akik szoptatnak, amíg a csecsemőt teljesen el nem választják.
Termékenység
Nőknél az EVRA abbahagyása után késhet a fogamzás.
04.7 Hatások a gépjárművezetéshez és gépek kezeléséhez szükséges képességekre
Az EVRA nincs vagy csak elhanyagolható mértékben befolyásolja a gépjárművezetéshez és gépek kezeléséhez szükséges képességeket.
04.8 Nemkívánatos hatások
A biztonsági profil összefoglalása
A klinikai vizsgálatok során leggyakrabban jelentett mellékhatások a fejfájás, az émelygés és a mellkasi kényelmetlenség voltak, és a nők körülbelül 21,0% -ánál, 16,6% -ánál, illetve 15,9% -ánál fordultak elő.
A kezelés elején fellépő, de általában az első három kúra után megszűnő mellékhatások közé tartozik a vérzés, a mellkasi kellemetlen érzés és a hányinger.
Néhány mellékhatás leírása
Az artériás és vénás trombotikus és thromboemboliás események, köztük a miokardiális infarktus, a stroke, az átmeneti iszkémiás rohamok, a vénás trombózis és a tüdőembólia fokozott kockázatát figyelték meg a kombinált kombinált kombinációt alkalmazó betegeknél, és ezt a kockázatot részletesebben tárgyalja a 4.4 pont.
Táblázat a mellékhatások listájával
A biztonságosságot 3332 szexuálisan aktív nőben értékelték, akik részt vettek a fázis III klinikai vizsgálatában, amelynek célja a fogamzásgátlás hatékonyságának értékelése. Ezek a betegek hat vagy 13 fogamzásgátló ciklust (EVRA vagy összehasonlító orális fogamzásgátló) kaptak., Legalább egy adag vizsgálatot végeztek Az alábbi 1. táblázat a klinikai vizsgálatokban és a forgalomba hozatalt követően jelentett mellékhatásokat tükrözi. MedDRA egyezmény a gyakoriságról: nagyon gyakori (≥ 1/10); gyakori (≥ 1/100 év
04.9 Túladagolás
Nagy mennyiségű orális fogamzásgátló véletlen lenyelése után nem jelentettek súlyos mellékhatásokat. A túladagolás hányingert és hányást okozhat. Egyes nőknél hüvelyi vérzés léphet fel. Túladagolás gyanúja esetén szüntesse meg a transzdermális fogamzásgátlás minden rendszerét és tüneti kezelést.
05.0 FARMAKOLÓGIAI TULAJDONSÁGOK
05.1 Farmakodinámiás tulajdonságok
Farmakoterápiás csoport: nemi hormonok és a nemi szervek modulátorai, progesztogének és ösztrogének, rögzített kapcsolat. ATC kód: G03AA13.
A cselekvés mechanizmusa
Az EVRA a gonadotropin -elnyomó mechanizmuson keresztül hat az etinilösztradiol és a norelgesztromin ösztrogén és progesztin hatása révén. Az elsődleges hatásmechanizmus az ovuláció gátlása, de a méhnyak és a méhnyálkahártya elváltozásai is hozzájárulhatnak a készítmény hatékonyságához.
Klinikai hatékonyság és biztonság
Gyöngy indexek (lásd a táblázatot):
*: DSG 150 mcg + 20 mcg EE
**: 50 mcg LNG +30 mcg EE az 1-6. Napon, 75 mcg LNG + 40 mcg EE a 7-11. Napon, 125 mcg LNG + 30 mcg EE a 12-21. Napon
Feltáró elemzéseket végeztek annak megállapítására, hogy a III. Fázisú vizsgálatokban (n = 3319) a kor, a faj és a súly populációi jellemzői összefügghetnek -e a terhességgel. Az elemzések nem mutattak összefüggést az életkor és a faj között a terhességgel, de súly szerint az EVRA -val jelentett 15 terhességből 5 olyan nő volt, akiknek a kiindulási súlya 90 kg vagy annál nagyobb volt, ami
Nagyobb dózisú COC-k (50 mcg etinil-ösztradiol) alkalmazásával csökken az endometrium- és petefészekrák kockázata.Még meg kell erősíteni, hogy ez vonatkozik-e az alacsonyabb dózisú kombinált hormonális fogamzásgátlókra is.
05.2 Farmakokinetikai tulajdonságok
Abszorpció
Az EVRA alkalmazása után a szérum norelgestromin és etinil -ösztradiol szintje körülbelül 48 órán belül eléri a fennsíkot. egyensúlyi állapot A norelgestromin és az EE a transzdermális tapasz egyhetes alkalmazása során körülbelül 0,8 ng / ml, illetve 50 pg / ml. Többadagos vizsgálatokban a norelgestromin és az EE szérumkoncentrációja és AUC-értéke csak kismértékben emelkedett. az 1. ciklus 1. hetéig.
Az EVRA alkalmazása után a norelgesztromin és az etinil -ösztradiol felszívódását az edzőteremben (szauna, jakuzzi, futópad és egyéb aerob gyakorlatok) és hidegvizes fürdőben tapasztalt körülmények között tanulmányozták.Az eredmények azt mutatják, hogy a norelgestromin esetében nem volt jelentős kezelési hatás a CSS vagy az AUC szempontjából a normál használathoz képest. Az EE esetében a futópadhoz és más aerob testmozgáshoz képest enyhe növekedést figyeltek meg, de az ilyen kezeléseket követő CSS értékek a referencia tartományon belül maradtak, a hideg víz nem befolyásolta jelentősen ezeket a paramétereket.
Az EVRA-val végzett vizsgálat eredményei egyetlen transzdermális tapasz 7 napon és 10 napon keresztül történő hosszú távú használatáról azt mutatták, hogy a norelgesztromin és az etinil-ösztradiol célzott CSS-je fennmaradt az EVRA 3 napos meghosszabbítása során. (10 nap) azt sugallják, hogy a klinikai hatékonyságot akkor is fenn kell tartani, ha a tapaszt 2 napig elfelejtik.
terjesztés
A norelgestromin és a norgesztrel (a norelgestromin szérum metabolitja) erősen (> 97%) kötődnek a szérumfehérjékhez. A norelgesztromin az albuminhoz kötődik, és nem az SHBG -hez, míg a norgesztrel elsősorban az SHBG -hez kötődik, ami korlátozza annak biológiai aktivitását. Az etinil -ösztradiol erősen kötődik a szérumalbuminhoz.
Biotranszformáció
A norelgesztromint a máj metabolizálja, és metabolitjai közé tartozik a norgesztrel, amely nagymértékben kötődik az SHGB -hez, valamint különböző hidroxilezett és konjugált metabolitok. Az etinil -ösztradiolt emellett különböző hidroxilezett termékekké és glükuronidokkal és szulfátokkal konjugátumokká metabolizálják.
Kiküszöbölés
A transzdermális tapasz eltávolítása után a norelgestromin és az etinil-ösztradiol eliminációs felezési ideje körülbelül 28 óra, illetve 17 óra volt. A norelgestromin és az etinil -ösztradiol metabolitjai a vesén és a székleten keresztül eliminálódnak.
Transzdermális fogamzásgátlók kontra orális fogamzásgátlók
A kombinált transzdermális és orális hormonális fogamzásgátlók farmakokinetikai profiljai eltérőek, és óvatosan kell eljárni e két készítmény farmakokinetikai paramétereinek közvetlen összehasonlításakor.
Egy vizsgálatban, amelyben az EVRA-t összehasonlították a norgestimátot (a norelgestromin prekurzora) tartalmazó orális fogamzásgátlóval, 250 mcg / etinil-ösztradiollal, 35 mcg, a Cmax-értékek kétszer magasabbak voltak a norelgesztromin és az etinil-ösztradiol esetében az orális fogamzásgátlót szedő alanyoknál az EVRA-hoz képest, míg a teljes expozíció (AUC és Css) összehasonlítható volt az EVRA -val kezelt alanyokkal.
Az EVRA farmakokinetikai paramétereiben az egyének közötti variabilitás (% CV) nagyobb volt, mint az orális fogamzásgátlóknál.
Az életkor, a testsúly és a testfelület hatásai
Az életkor, testtömeg és testfelület hatását a norelgesztromin és az etinil -ösztradiol farmakokinetikájára 230 egészséges nőben értékelték kilenc farmakokinetikai vizsgálatban, egyetlen EVRA -alkalmazással 7 napon keresztül. Az életkor, a súly és a testfelület növekedése összefüggésben volt a Css és az AUC értékek enyhe csökkenése mind a norelgesztromin, mind az EE esetében. Az EVRA alkalmazása után azonban a norelgesztromin és az EE farmakokinetikájának általános változékonyságának csak kis százaléka (10-20%) hozható összefüggésbe néhány vagy egész a fenti demográfiai paramétereket.
05.3 A preklinikai biztonságossági adatok
A hagyományos klinikai vizsgálatok alapján a nem klinikai adatok nem támasztanak alá különleges kockázatot az emberre biztonságtechnológia, ismételt dózisú toxicitás, genotoxicitás és rákkeltő hatás. Ami a reproduktív toxicitást illeti, a norelgestromin magzati toxicitást mutatott nyulakban, azonban ennek a hatásnak a biztonsági határa kellően magas volt. Nincsenek adatok a norelgestromin és az etinil -ösztradiol kombinációjának reprodukciós toxicitásáról. A norgesztimát (a norelgestromin prekurzora) és az etinil -ösztradiol kombinációjára vonatkozó adatok azt mutatják, hogy a nőstény állatok termékenysége és hatékonysága csökken. Implantáció (patkányok), növekedés magzati reszorpcióban (patkányok, nyulak) és nagy dózisok esetén a nőstény születések (patkányok) életképességének és termékenységének csökkenésében. Ezen adatok relevanciája az emberi expozíció szempontjából nem ismert, mivel a hatásokat farmakodinámiás hatásoknak vagy ezen állatfajokra vonatkozó, már ismert természetű hatásoknak tekintették.
Az EVRA dermális hatásait vizsgáló tanulmányok azt mutatják, hogy ez a rendszer nem képes szenzibilizációt okozni, és csak enyhe irritációt okozhat, ha nyúl bőrére alkalmazzák.
06.0 GYÓGYSZERÉSZETI INFORMÁCIÓK
06.1 Segédanyagok
Megerősítő réteg
külső réteg kis sűrűségű pigmentált polietilénből, belső réteg poliészterből.
Közbenső réteg
poliizobutilén / ragasztó polibutén, kroszpovidon, nem szőtt poliészter szövet, lauril-laktát.
Harmadik réteg
polietilén -tereftalát (PET) film, polidimetil -sziloxán bevonat.
06.2 Inkompatibilitás
Nem releváns.
06.3 Érvényességi idő
2 év.
06.4 Különleges tárolási előírások
Az eredeti csomagolásban tárolandó, hogy megvédje a tapaszokat a fénytől és a nedvességtől.
Hűtőszekrényben nem fagyasztható.
06.5 A közvetlen csomagolás jellege és a csomag tartalma
Elsődleges csomagolóanyag
Minden tasak négy rétegből áll: egy kis sűrűségű polietilén fóliából (a legbelső réteg), egy alumínium fóliából, egy kis sűrűségű polietilén fóliából és egy fehérített papír külső rétegéből.
Másodlagos csomagolóanyag
A tasakokat kartondobozba csomagolják.
Minden csomag 3, 9 vagy 18 EVRA transzdermális tapaszt tartalmaz megerősített tasakokban.
A tasakokat hármas csoportokban átlátszó, perforált műanyag fóliába csomagolják, és kartondobozba csomagolják.
Nem feltétlenül mindegyik kiszerelés kerül kereskedelmi forgalomba.
06.6 Használati utasítás
A tapaszt azonnal fel kell helyezni a védőtasak eltávolítása után.
Az EVRA tapadási tulajdonságainak megzavarásának elkerülése érdekében ne vigyen fel krémet, lotiont vagy talkumot arra a bőrfelületre, ahol az EVRA transzdermális tapaszt fel kell helyezni.
Használat után a transzdermális tapasz még mindig jelentős mennyiségű hatóanyagot tartalmaz. Ezért a használt transzdermális tapaszt óvatosan el kell dobni. A törléshez használt címke. a tasak külső oldalán kell elhelyezni, fel kell emelni. A használt transzdermális tapaszt a nyitott eldobott címke belsejébe kell helyezni úgy, hogy a tapadós felület lefedje a tasak árnyékolt területét. A címkét ezután le kell zárni a használt transzdermális tapasz lezárásával. A fel nem használt gyógyszereket és az ezekből származó hulladékot a helyi előírásoknak megfelelően kell megsemmisíteni. A használt transzdermális tapaszokat nem szabad a WC -be vagy a hulladék eltávolításába dobni. folyadékok eszközei.
07.0 FORGALOMBA HOZATALI ENGEDÉLY
JANSSEN-CILAG INTERNATIONAL N.V.
Turnhoutseweg, 30
B-2340 Sör
Belgium
08.0 A FORGALOMBA HOZATALI ENGEDÉLY SZÁMA
EU/1/02/223/001
035684012
EU/1/02/223/002
035684024
EU/1/02/223/003
035684036
09.0 Az első forgalomba hozatali engedély kiadásának időpontja
Az első engedélyezés időpontja: 2002. augusztus 22
Az utolsó megújítás dátuma: 2012. augusztus 22
10.0 A SZÖVEG FELÜLVIZSGÁLÁSÁNAK DÁTUMA
01/2014