(szabadon lefordítva angol szövegből)
Mi az a biológiai gyógyszer?
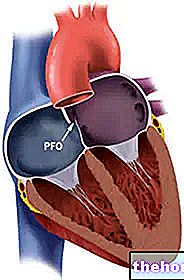
A biológiai gyógyszer olyan gyógyszer, amely élő szervezet által termelt vagy abból származó hatóanyagot tartalmaz. "Az inzulin például valójában biológiai gyógyszer, mivel jelenleg egy élő szervezet (például egy gomba vagy egy baktérium) szintetizálja, amely a genetikai rekombinációs technikáknak köszönhetően kifejezi a" hormon "szintéziséhez szükséges DNS -t.
Mi a biológiailag hasonló gyógyszer?
A bioszimiláris gyógyszer olyan gyógyszer, amely olyan hatóanyagot tartalmaz, amely nagyon hasonló ahhoz a biológiai gyógyszerhez, amelyet az illetékes intézetek már forgalomba hoztak a témában. Emiatt általában a két gyógyszert azonos dózisokban használják ugyanazon betegség kezelésére. Hasonló, ha nem azonos is az összetevők, valamint a hatóanyag neve.
Mindezek a hasonlóságok ellenére az egyik vagy a másik gyógyszer szedésének eldöntése kizárólag és kizárólag az orvostól függ; valójában kissé eltérő indikációk és mellékhatások lehetnek, amelyek miatt az egyik gyógyszer alkalmazása alkalmasabb, mint a másik.
Milyen kritériumokon alapul egy bioszimilária forgalomba hozatali engedélye?
Mint minden gyógyszer, a bioszimiláris gyógyszerek megvásárlása előtt „forgalomba hozatali engedélyt” is igényelnek. Ezt az engedélyt egy versenytárs szervezet, például az EMEA adja ki, miután értékelte a gyógyszer hatékonyságára, biztonságosságára és minőségére vonatkozó tanulmányok sorozatát. .
Az innovatív gyógyszerek bizonyos ideig védelmet élveznek a versennyel szemben. Ennyi idő elteltével más gyógyszergyárak is megszerezhetik a bioszimiláris gyógyszerek forgalmazására vonatkozó engedélyt.
Hogyan értékelik a biológiailag hasonló gyógyszereket?
Tekintettel arra, hogy a biológiailag hasonló gyógyszerek forgalomba hozatalának időpontjában a biológiai referencia -gyógyszert már több éve használják, "jelentős mennyiségű tanulmány és információ van ezzel kapcsolatban. Ezért nincs szükség további és ilyen hosszú értékelési folyamat. Továbbá, ha a terápiás javallatok eltérőek, a bioszimiláris gyógyszer hatékonyságát és biztonságosságát is igazolni kell a kezelendő új rendellenességre vagy betegségre hivatkozva.
Ezen szigorú vizsgálatok mellett a témával foglalkozó illetékes szervek megkövetelik, hogy a biológiailag hasonló gyógyszert ugyanazon minőségi előírások betartásával állítsák elő, mint minden más gyógyszer esetében. Nyilvánvaló, hogy ebben az értelemben sem hiányoznak a tárgyban hatályos jogszabályok betartásának pontos és időszakos ellenőrzései.
Hogyan ellenőrzik a biológiailag hasonló gyógyszerek biztonságosságát?
Minden gyógyszer - beleértve a hasonló gyógyszereket is - biztonságosságát a forgalomba hozatali engedély megadása után is gondosan figyelemmel kísérik. A törvény különösen megköveteli, hogy minden gyógyszeripari vállalat rendelkezzen biztonsági monitoring rendszerrel a forgalomba hozott új gyógyszerekre, beleértve az immunológiai jellegű válaszokat is ( lehetséges allergiás jelenségek) Nyilvánvaló, hogy az illetékes szervek még ebben az esetben is ellenőrzik, hogy ez az ellenőrző rendszer megfelel -e a hatályos jogszabályok által előírt szabványoknak.
Az ezen az oldalon közzétett, biológiailag hasonló gyógyszerekre vonatkozó információk elavultak vagy hiányosak lehetnek. Ezen információk helyes használatához tekintse meg a Jogi nyilatkozat és a hasznos információk oldalt.