Hatóanyagok: latanoproszt
Latanoprost Aurobindo 50 mikrogramm / ml szemcsepp, oldat
Miért használják a Latanoprost - általános gyógyszert? Mire való?
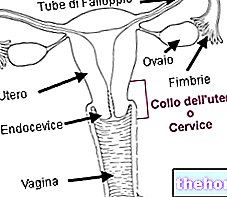
A Latanoprost Aurobindo egy szemcsepp, amelyet olyan betegeknél használnak, akiknek nyitott zugú glaukóma néven ismert állapotuk van, ami fokozott nyomást okoz a szemben. A Latanoprost Aurobindo hatóanyaga a prosztaglandinok néven ismert gyógyszerek csoportjába tartozik. A Latanoprost Aurobindo egy vérnyomáscsökkentő gyógyszer. a szemet úgy, hogy növeli a folyadék természetes áramlását a szem belsejéből a véráramba.
A Latanoprost Aurobindo -t emellett a megnövekedett szemnyomás és a glaukóma kezelésére is használják minden korú gyermek és csecsemő esetében.
A Latanoprost Aurobindo felnőtt nők és férfiak (beleértve az időseket is), valamint gyermekek születésétől 18 éves koráig alkalmazható. A Latanoprost Aurobindo alkalmazását koraszülött csecsemőknél (36 hetesnél fiatalabb korban) nem vizsgálták.
Ellenjavallatok Amikor a Latanoprost -ot nem szabad használni - Generikus gyógyszer
Ne alkalmazza a Latanoprost Aurobindo -t:
- ha allergiás a latanoprosztra a gyógyszer (6. pontban felsorolt) egyéb összetevőjére.
Az alkalmazással kapcsolatos óvintézkedések Mit kell tudnia a Latanoprost - Generic gyógyszer szedése előtt
A Latanoprost Aurobindo alkalmazása előtt beszéljen kezelőorvosával vagy gyógyszerészével:
- - ha Ön vagy gyermeke súlyos asztmában szenved, vagy az asztmája nincs megfelelően kontrollálva.
- ha Önnek vagy gyermekének glaukóma-típusa van, úgynevezett „krónikus zárt szögű glaukóma”.
- ha Önnek vagy gyermekének glaukóma van, annak ellenére, hogy nincs lencséjük vagy mesterséges lencséjük.
- ha Önnek vagy gyermekének glaukóma van, amelyet a szemkamra sarkában lévő pigmentek képeznek.
- ha Önnek vagy gyermekének glaukóma van, amelyet a szem gyulladása vagy új erek képződése okoz a szemben.
- ha Önnek vagy gyermekének veleszületett glaukóma van.
- ha szeme vagy gyermeke aphakiás (a lencse hiányzik a szeméből) vagy pszeudo-aphakiás, a hátsó lencsekapszula szakadásával vagy az elülső kamrában lévő lencsékkel.
- ha Önnek vagy gyermekének ismert kockázati tényezői vannak a cisztás makula ödéma vagy az írisz gyulladása (iritis / uveitis) előtt vagy után a szürkehályog műtét során,
- ha Önnek vagy gyermekének cukorbetegség következtében érrendszeri szemzavara vagy retina rendellenességei vannak.
- ha Önnek vagy gyermekének száraz a szeme; orvosa gondosan figyelemmel kíséri ezt a problémát,
- ha a szaruhártyát érintő rendellenességekben szenved; orvosa gondosan figyelemmel kíséri ezt a problémát.
- ha Ön vagy gyermeke a herpes simplex vírus (VHS) által okozott szemi vírusfertőzésben szenvedett vagy szenved jelenleg.
Nincs tapasztalat a keskeny szögű glaukóma-rohamok latanoprosztos kezelésében.
Kölcsönhatások Mely gyógyszerek vagy élelmiszerek módosíthatják a Latanoprost - Generic gyógyszer hatását
Feltétlenül tájékoztassa kezelőorvosát vagy gyógyszerészét a jelenleg vagy nemrégiben szedett, valamint szedni tervezett egyéb gyógyszereiről. A Latanoprost Aurobindo kölcsönhatásba léphet ezekkel a gyógyszerekkel.
A prosztaglandinok vagy prosztaglandinszármazékok (fokozott szemnyomás esetén alkalmazott) hatását befolyásolhatja a Latanoprost Aurobindo, ezek kombinációja Latanoprost Aurobindo -val nem ajánlott, mert a szemnyomás emelkedhet.
Figyelmeztetések Fontos tudni, hogy:
Terhesség, szoptatás és termékenység
Ha Ön terhes vagy szoptat, illetve ha fennáll Önnél a terhesség lehetősége vagy gyermeket szeretne, a gyógyszer alkalmazása előtt beszéljen kezelőorvosával vagy gyógyszerészével.
Terhesség
A magzat károsodhat. A Latanoprost Aurobindo nem alkalmazható terhesség alatt.
Etetési idő
A baba megsérülhet. A Latanoprost Aurobindo nem alkalmazható szoptatás alatt.
A készítmény hatásai a gépjárművezetéshez és gépek kezeléséhez szükséges képességekre
Más szemcseppekhez hasonlóan, ha látása homályossá válik a cseppek felhelyezésekor, várjon, amíg a zavarosság megszűnik, mielőtt vezetne vagy gépeket kezelne.
A Latanoprost Aurobindo benzalkónium -kloridot tartalmaz
A benzalkonium -klorid szemirritációt okozhat. Kerülje a puha kontaktlencsékkel való érintkezést. A szerelés előtt vegye ki a kontaktlencséket, és várjon legalább 15 percet, mielőtt újra felhelyezné.
Adagolás, az alkalmazás módja és ideje Hogyan kell alkalmazni a Latanoprost - Generikus gyógyszert: Adagolás
Ezt a gyógyszert mindig pontosan az orvos által elmondottaknak megfelelően alkalmazza. Ha kétségei vannak, forduljon orvosához vagy gyógyszerészéhez.
A szokásos adag felnőtteknek és gyermekeknek egy csepp a beteg szembe, naponta egyszer, lehetőleg este.
Legyen óvatos, amikor összenyomja a palackot, hogy csak egy csepp kerüljön az érintett szembe.
Ne használja a Latanoprost Aurobindo -t naponta többször, mivel a kezelés hatása gyengülhet, ha gyakrabban alkalmazzák.
Kövesse az alábbi utasításokat a Latanoprost Aurobindo helyes használatához:
- Mosson kezet, üljön vagy feküdjön kényelmesen,
- Távolítsa el a palack kupakját,
- Ujjával óvatosan húzza le a beteg szem alsó szemét,
- Helyezze a palack kifolyóját a szeme közelébe anélkül, hogy megérintené,
- Óvatosan nyomja össze az üveget, hogy egyetlen csepp a szembe essen, majd engedje el az alsó szemhéjat,
- Nyomja meg az ujját az érintett szem sarkában az orr oldalán. Várj egy percet csukott szemmel,
- Ismételje meg a műveletet a másik szemében, ha orvosa ezt mondta,
- Tegye vissza a kupakot az üvegre.
Ha elfelejtette alkalmazni a Latanoprost Aurobindo -t
Ne használjon dupla adag Latanoprost Aurobindo -t a kihagyott adag pótlására. Ha elfelejtette alkalmazni a szemcseppjét a szokásos időben, várja meg, amíg el nem jön a következő adag beadásának ideje.
Ne használjon adagot az elfelejtett adag pótlására.
Ha idő előtt abbahagyja a Latanoprost Aurobindo szedését
Addig használja a Latanoprost Aurobindo -t, amíg kezelőorvosa azt nem mondja, hogy hagyja abba.
Ha kontaktlencsét használ:
Ha kontaktlencsét használ, távolítsa el azokat a Latanoprost Aurobindo használata előtt. A Latanoprost Aurobindo használata után legalább 15 percig ne tegye vissza a kontaktlencséit. A Latanoprost Aurobindo tartósítószere, az úgynevezett benzalkonium -klorid szemirritációt okozhat, és elszínezheti a lágy kontaktlencséket.
Ha bármilyen további kérdése van a készítmény alkalmazásával kapcsolatban, kérdezze meg kezelőorvosát vagy gyógyszerészét.
Túladagolás Mi a teendő, ha túladagolt Latanoprost - Generic gyógyszert
Legyen óvatos, amikor összenyomja az üveget, hogy csak egy csepp kerüljön a beteg szembe.Ha túl sok cseppet adott a szemébe, enyhe irritációt érezhet. Ha a Latanoprost Aurobindo -t véletlenül lenyeli, forduljon orvosához.
Mellékhatások Melyek a Latanoprost - Generic gyógyszer mellékhatásai
Mint minden gyógyszer, így ez a gyógyszer is okozhat mellékhatásokat, amelyek azonban nem mindenkinél jelentkeznek.
A következő mellékhatásokat jelentették.
Nagyon gyakori mellékhatások (10 beteg közül több mint 1 beteget érinthet):
- a szem színének megváltozása (barnábbak és sötétebbek lesznek)
- vörös, vizes szemek, égő, bizsergő, viszkető érzés, mintha valami lenne a szemben
- a szempillák és a szemhéjak szemhéjának megnövekedett száma vagy elsötétülése, megvastagodása vagy meghosszabbodása.
Gyakori mellékhatások (10 beteg közül legfeljebb 1 beteget érinthet):
- átmeneti pontszerű hámeróziók, általában tünetek nélkül
- a szemhéjak szélének gyulladása
- szemirritáció.
Nem gyakori mellékhatások (100 beteg közül legfeljebb 1 beteget érinthet):
- a szemhéjak duzzanata,
- száraz szemek,
- a szaruhártya gyulladása,
- homályos látás,
- kötőhártya-gyulladás,
- kiütés.
Ritka mellékhatások (1000 -ből legfeljebb 1 beteget érinthet):
- a szemgyulladás bizonyos formái (iritis, uveitis)
- duzzanat és a szaruhártya károsodása (szaruhártya ödéma)
- duzzanat a szemüreg körül (periorbitális ödéma)
- a szempillák növekedése befelé, ami időnként szemirritációt okozhat (nem gyakori)
- hirtelen fellépő mellkasi merevség, amelyet izomgörcs és a hörgők nyálkahártyájának ödémája okoz, gyakran köhögéssel és köpetürítéssel (asztma) az asztma súlyosbodása és légzési nehézség (dyspnoe)
- a szemhéjak kiütése
- a szemhéjak bőrének sötét színezése
- makula ödéma.
Nagyon ritka mellékhatások (10 000 -ből legfeljebb 1 beteget érinthet):
- mellkasi fájdalom,
- az angina pectoris súlyosbodása fordulhat elő.
Egyéb mellékhatások, amelyeket a Latanoprost forgalomba hozatalát követően jelentettek (gyakorisága nem ismert):
- fejfájás,
- szédülés
- szívdobogásérzés,
- izom- és ízületi fájdalom
- folyadékkal töltött terület a szem színes részén (írisz ciszta)
- a herpes simplex vírus (VHS) által okozott szemi vírusfertőzés kialakulása.
Nagyon ritka esetekben néhány betegnél, akik súlyos sérülést szenvedtek a szem elülső részének (szaruhártya) tiszta rétegében, a kezelés során fehéres foltok jelentek meg a szaruhártyán a kalcium miatt.
További mellékhatások gyermekeknél
Gyermekeknél gyakrabban észlelt mellékhatások, mint felnőtteknél: orrfolyás és viszketés, láz.
Mellékhatások bejelentése
Ha Önnél bármilyen mellékhatás jelentkezik, tájékoztassa erről kezelőorvosát vagy gyógyszerészét. Ez a betegtájékoztatóban fel nem sorolt bármilyen lehetséges mellékhatásra is vonatkozik. A mellékhatásokat közvetlenül a hatóság részére is bejelentheti az V. függelékben található elérhetőségeken keresztül. A mellékhatások bejelentésével Ön is hozzájárulhat ahhoz, hogy minél több információ álljon rendelkezésre a gyógyszer biztonságosságáról.
Lejárat és megőrzés
A gyógyszer gyermekektől elzárva tartandó!
A dobozon feltüntetett lejárati idő (EXP) után ne alkalmazza ezt a gyógyszert. A lejárati idő az adott hónap utolsó napjára vonatkozik.
Hűtőszekrényben (2 ° C - 8 ° C) tárolandó.
Tartsa a tartályt a külső dobozban, hogy megvédje a gyógyszert a fénytől.
A tartály első felbontása után: legfeljebb 25 ° C -on tárolandó.
Négy héttel az első felbontás után a gyógyszert ki kell dobni, még akkor is, ha nem használták fel teljesen.
Semmilyen gyógyszert ne dobjon a szennyvízbe vagy a háztartási hulladékba. Kérdezze meg gyógyszerészét, hogy mit tegyen a már nem használt gyógyszereivel. Ez elősegíti a környezet védelmét.
Határidő "> Egyéb információ
Mit tartalmaz a Latanoprost Aurobindo?
- A készítmény hatóanyaga a latanoproszt.
- Egyéb összetevők: benzalkonium -klorid, egybázisú nátrium -foszfát -monohidrát, vízmentes kétbázisú nátrium -foszfát, nátrium -klorid, tisztított víz.
Egy ml szemcsepp 50 mikrogramm latanoprosztot tartalmaz.
Egy csepp körülbelül 1,5 mikrogramm latanoprosztot tartalmaz.
A Latanoprost Aurobindo külleme és a csomagolás leírása
A Latanoprost Aurobindo tiszta, színtelen szemcsepp oldat LDPE palackban, HPDE csavaros kupakkal.
Minden palack 2,5 ml szemcseppet tartalmaz, amely körülbelül 80 csepp oldatnak felel meg.
A Latanoprost Aurobindo 1, 3 és 6 palackos kiszerelésben kapható.
Nem feltétlenül mindegyik kiszerelés kerül kereskedelmi forgalomba.
Forrás betegtájékoztató: AIFA (Olasz Gyógyszerügynökség). A tartalom 2016 januárjában jelent meg. A jelenlévő információk nem feltétlenül naprakészek.
A legfrissebb verzióhoz való hozzáféréshez ajánlatos az AIFA (Olasz Gyógyszerügynökség) webhelyét elérni. Jogi nyilatkozat és hasznos információk.
01.0 A GYÓGYSZER MEGNEVEZÉSE -
LATANOPROST ACTAVIS 50 MCG / ML
02.0 MINŐSÉGI ÉS MENNYISÉGI ÖSSZETÉTEL -
Egy ml szemcsepp 50 mcg latanoprosztot tartalmaz.
Egy csepp körülbelül 1,5 mcg latanoprosztot tartalmaz.
Segédanyagok: 0,2 mg / ml benzalkonium -klorid.
A segédanyagok teljes listáját lásd a 6.1 pontban.
03.0 GYÓGYSZERFORMA -
Szemcseppek, oldat.
Az oldat tiszta, színtelen folyadék.
pH 6,4-7,0.
Osmolalitás: 240-290 mOsm / kg.
04.0 KLINIKAI INFORMÁCIÓK -
04.1 Terápiás javallatok -
A megnövekedett szemnyomás csökkentése nyílt szögű glaukómában és okuláris hipertóniában szenvedő betegeknél.
04.2 Adagolás és alkalmazás
Ajánlott adag felnőtteknek (beleértve az idős betegeket is):
Az ajánlott terápia naponta egyszer egy csepp a kezelendő szem (ek) ben.
A Latanoprost Actavis adagja nem haladhatja meg a napi egyszeri adagot, mivel a gyakoribb alkalmazás csökkenti az intraokuláris nyomásra gyakorolt hipotenzív hatást.
Ha egy adag kimarad, a kezelést a következő adaggal a szokásos módon kell folytatni.
Más szemcseppekhez hasonlóan, az esetleges szisztémás felszívódás csökkentése érdekében ajánlatos egy percig összenyomni a könnyzsákot a mediális canthus szintjén (punctalis occlusio). Ezt azonnal meg kell tenni az egyes cseppek csepegtetése után.
A kontaktlencséket a szemcseppek csepegtetése előtt el kell távolítani, és 15 perc múlva újra fel lehet használni.
Ha egynél több helyi szemészeti gyógyszert alkalmaznak, akkor a gyógyszereket legalább öt perc különbséggel kell beadni.
Gyermekek:
Gyermekek biztonságosságát és hatásosságát nem állapították meg, ezért a Latanoprost Actavis alkalmazása gyermekeknél nem javasolt.
04.3 Ellenjavallatok -
Túlérzékenység a latanoprosztra, a benzalkonium -kloridra vagy bármely más segédanyagra.
04.4 Különleges figyelmeztetések és a használattal kapcsolatos óvintézkedések -
A Latanoprost Actavis fokozatosan megváltoztathatja a szem színét azáltal, hogy növeli a barna pigment mennyiségét az íriszben. A kezelés megkezdése előtt a betegeket tájékoztatni kell a szem színének tartós változásáról. Az egyoldalú kezelés tartós heterokrómiát okozhat.
Ezt a szemszínváltozást leginkább azoknál a betegeknél figyelték meg, akiknek színtelen íriszük volt, pl. Kék-barna, szürkésbarna, sárga-barna és zöld-barna. A latanoprosztos vizsgálatok során a változás általában akkor jelentkezik. a kezelés első 8 hónapjában, ritkán a második vagy harmadik évben, és soha nem volt megfigyelhető a kezelés negyedik éve után. Az írisz pigmentáció előrehaladásának üteme idővel csökken, és 5 évig stabil. A pigmentáció növekedésének hatását 5 éven túl nem értékelték. Egy 5 éves nyílt biztonsági vizsgálatban a betegek 33 % -ánál alakult ki írisz pigmentáció (lásd 4.8 pont) ). Az írisz színének ez a változása a legtöbb esetben enyhe, és gyakran klinikailag nem észlelhető.Az incidencia 7-85% között van az egyenetlen színű íriszekkel rendelkező betegeknél, a legnagyobb előfordulási arány a sárgásbarna íriszben szenvedő betegeknél. Homogén kék szemű betegeknél és csak ritkán homogén szürke, zöld vagy barna szemű betegeknél nem észleltek változást.
A színváltozás oka a melanin növekedése az írisz stróma melanocitáiban, és nem a melanociták számának növekedése. Általában a pupilla körüli barna pigmentáció koncentrikusan terjed az érintett szem perifériás területe felé, de minden az írisz vagy annak területei barnábbá válhatnak. A kezelés felfüggesztése után az írisz pigmentációja nem növekedett tovább. Az eddigi klinikai vizsgálatok során ez a jelenség nem társult semmilyen tünethez vagy elváltozáshoz kóros.
A kezelés nem befolyásolta a szivárványhártya nevi vagy íveléit. A klinikai vizsgálatok nem tártak fel pigment felhalmozódást a sclerocornealis trabekulárisban vagy az elülső kamra bármely más részében. Az 5 éves klinikai tapasztalatok alapján az írisz pigmentációjának növekedése nem kimutatták, hogy meghatározza az esetleges negatív klinikai következményeket, és ha a szivárványhártya pigmentációja jelentkezik, a Latanoprost Actavis beadása folytatható, azonban a betegeket rendszeresen ellenőrizni kell, és ha a klinikai kép megkívánja, a Latanoprost Actavis -kezelést meg lehet szakítani.
"Korlátozott tapasztalat áll rendelkezésre a latanoproszt krónikus bezárt szögű glaukóma, nyílt látószögű glaukóma és pigment glaukóma betegek esetében. Nincs tapasztalat a latanoproszt gyulladásos és neovaszkuláris glaukóma, szemgyulladás vagy veleszületett glaukóma esetén." . A Latanoprost Actavis alig vagy egyáltalán nem hat a pupillára, de nincs tapasztalat a keskeny szögű glaukóma akut rohamairól. Ezért óvatosan kell eljárni a Latanoprost Actavis ilyen körülmények között történő alkalmazásával, amíg további tapasztalatokra nem tesz szert.
Korlátozott mennyiségű adat áll rendelkezésre a latanoproszt szürkehályog-műtét perioperatív szakaszában történő alkalmazásáról.A Latanoprost Actavis-t óvatosan kell alkalmazni ezeknél a betegeknél.
Makula ödéma eseteiről számoltak be (lásd 4.8 pont), különösen az aphakikus, pszeudofákiás betegeknél, akiknél a hátsó lencsekapszula megrepedt vagy az elülső kamra lencséi, valamint olyan betegeknél, akik ismert kockázati tényezőkkel rendelkeznek a cystoidos makulaödéma kialakulásához (például diabéteszes retinopátia és retina véna). elzáródás) A Latanoprost Actavis -t óvatosan kell alkalmazni aphakikus, pszeudofákiás betegeknél, ha a hátsó lencsekapszula megrepedt, vagy az elülső kamra lencséje, vagy olyan betegeknél, akiknél ismert kockázati tényezők vannak a cystoid makula ödéma kialakulásához.
Olyan betegeknél, akiknél ismertek az iritis / uveitis kockázati tényezői, a Latanoprost Actavis óvatosan alkalmazható.
Az asztmás betegekkel kapcsolatos tapasztalatok korlátozottak, de a forgalomba hozatalt követően néhány asztmás exacerbáció és / vagy nehézlégzés eseteiről számoltak be. Ezért az asztmás betegeket óvatosan kell kezelni, amíg elegendő tapasztalat nem áll rendelkezésre (lásd még a 4.8 pontot).
A periorbitális bőr elszíneződését figyelték meg, a legtöbb jelentés japán betegektől származik. Eddig az adatok azt mutatták, hogy ez a periorbitális bőrváltozás nem tartós, és bizonyos esetekben visszafordítható a Latanoprost Actavis -kezelés folytatása közben.
A latanoproszt fokozatosan megváltoztathatja a kezelt szemek és a környező területek szempilláit és haját; ezek a változások magukban foglalják a hossz, vastagság, pigmentáció, a szempillák vagy szőrszálak növekedését, a szempillák növekedési irányának megváltozását. A szempilla változásai a kezelés abbahagyása után visszafordíthatók.
A gyógyszer benzalkónium -kloridot tartalmaz, amely szemirritációt okozhat. Kerülje a puha kontaktlencsékkel való érintkezést. A felszerelés előtt távolítsa el a kontaktlencséket, és várjon legalább 15 percet, mielőtt visszahelyezné őket (lásd 4.2 pont). A benzalkonium -kloridról ismert, hogy megváltoztatja a lágy kontaktlencsék színét. A benzalkonium -kloridról beszámoltak arról, hogy pontszerű keratopátiát és / vagy toxikus fekélyes keratopátiát okoz, és szemirritációt okozhat. Gondos megfigyelésre van szükség a száraz szemű betegeknél, akik gyakran vagy hosszabb ideig használják a Latanoprost Actavis -t, vagy ha a szaruhártya sérült.
04.5 Kölcsönhatások más gyógyszerekkel és egyéb interakciók -
Nincsenek meggyőző adatok a gyógyszerkölcsönhatásokról.
Két prosztaglandin -analóg egyidejű szemészeti beadását követően az intraokuláris nyomás paradox növekedését jelentették. Ezért két vagy több prosztaglandin -analóg vagy prosztaglandin -származék alkalmazása nem ajánlott.
04.6 Terhesség és szoptatás -
Terhesség
A gyógyszer biztonságosságát emberi terhesség alatt nem igazolták. A terhesség alatt fennáll a farmakológiai kockázat, mind a magzatra, mind az újszülöttre nézve. Ezért a Latanoprost Actavis nem alkalmazható terhesség alatt.
Etetési idő
A latanoproszt és metabolitjai kiválasztódhatnak az anyatejbe, ezért a Latanoprost Actavis nem alkalmazható szoptató nőknél, vagy a szoptatást abba kell hagyni.
04.7 Hatások a gépjárművezetéshez és gépek kezeléséhez szükséges képességekre -
A gépjárművezetéshez és gépek kezeléséhez szükséges képességeket nem vizsgálták. Más szemészeti készítményekhez hasonlóan a cseppek csepegtetése átmeneti homályos látást is okozhat.
04.8 Nemkívánatos hatások -
A legtöbb mellékhatás a szemrendszert érinti: Egy nyílt, 5 éves latanoproszt-biztonsági vizsgálatban a betegek 33% -ánál alakult ki írisz pigmentáció (lásd 4.4 pont). Az egyéb szemészeti mellékhatások általában átmeneti jellegűek és az adagoláskor jelentkeznek.
A mellékhatásokat a gyakoriságuk szerint az alábbiak szerint osztályozzák: nagyon gyakori (≥1 / 10), gyakori (≥1 / 100 és
04.9 Túladagolás -
A szemirritáción és a kötőhártya -hiperémián kívül más szemészeti mellékhatás nem ismert a Latanoprost Actavis túladagolása esetén.
A Latanoprost Actavis véletlen lenyelése esetén az alábbi információk hasznosak lehetnek: Egy üveg 125 mcg latanoprosztot tartalmaz. Több mint 90% -a metabolizálódik az első átjutás során a májban. A 3 mcg / kg intravénás infúzió egészséges önkénteseknél nem okozott tüneteket, de az 5,5-10 mcg / kg dózis hányingert, hasi fájdalmat, szédülést, fáradtságot, hőhullámokat és izzadást okozott. A latanoprosztot intravénásán adták be majmoknak, legfeljebb 500 mcg / kg anélkül, hogy jelentős hatást gyakorolna a szív- és érrendszerre.
A latanoproszt intravénás alkalmazása majmoknál összefüggésben állt az átmeneti hörgőszűkülettel. A latanoproszt azonban, ha helyileg alkalmazzák a szembe, a klinikán alkalmazottnál 7 -szer nagyobb dózisban, nem okoz hörgőszűkületet mérsékelt hörgő asztmában szenvedő betegeknél.
A Latanoprost Actavis túladagolása esetén a kezelésnek tüneti kezelésnek kell lennie.
05.0 FARMAKOLÓGIAI TULAJDONSÁGOK -
05,1 "Farmakodinamikai tulajdonságok -
Farmakoterápiás csoport: glaukóma elleni szerek és miotikus készítmények, prosztaglandin-analógok.
ATC kód: S01E E01.
A latanoproszt hatóanyag, egy prosztaglandin F2α analóg, egy szelektív prosztanoid FP receptor agonista, amely csökkenti az intraokuláris nyomást a vizes humor kiáramlásának növelésével. Az intraokuláris nyomás csökkenése az emberekben körülbelül három -négy órával az alkalmazás után kezdődik, és a maximális hatást nyolckor éri el. tizenkét óráig. A nyomáscsökkentés legalább 24 órán keresztül fennmarad.
Állatokon és embereken végzett vizsgálatok azt mutatják, hogy a fő hatásmechanizmus a fokozott uveoszklerális kiáramlás, bár embereknél a könnyebb kiáramlás fokozódásáról (a kiáramlással szembeni ellenállás csökkenéséről) számoltak be.
Alapvető vizsgálatok igazolták a Latanoprost Actavis monoterápia hatékonyságát, emellett kombinált klinikai vizsgálatokat is végeztek.Ezek közé tartoznak a latanoproszt béta-adrenerg antagonistákkal (timolollal) kombinált hatékonyságát bemutató vizsgálatok. Rövid távú vizsgálatok (1 vagy 2 hét) a latanoproszt additív hatását jelzik, ha adrenerg agonistákkal (dipivalil-epinefrin) együtt alkalmazzák. szájon át (acetazolamid) és legalább részben kolinerg agonistákkal (pilokarpin) együtt adva.
Klinikai vizsgálatok kimutatták, hogy a latanoproszt nincs szignifikáns hatással a vizes humor képzésére. A latanoproszt nem volt hatással a vér / vizes gátra.
Majmokon végzett vizsgálatok kimutatták, hogy a latanoproszt klinikai dózisban adva nincs vagy csak elhanyagolható hatással van az intraokuláris vérkeringésre. A helyi kezelés során azonban enyhe vagy mérsékelt kötőhártya vagy episzklerális hiperémia fordulhat elő.
A latanoproszt krónikus kezelése majomszemben az extrakapsuláris lencse kivonása után nem befolyásolta a retina vérkeringését, amint azt fluoroangiográfiával igazolták.
A latanoproszt klinikai dózisokban történő alkalmazása után nem észleltek jelentős farmakológiai hatást a szív- és érrendszerre vagy a légzőrendszerre.
05,2 "Farmakokinetikai tulajdonságok -
A latanoproszt (p. 432.58) egy észterezett prodrug, amely izopropil -csoporttal rendelkezik, önmagában inaktív, és a hidrolízis után a savas formára biológiailag aktívvá válik.
A prodrug jól felszívódik a szaruhártyán, és teljesen hidrolizálódik a vizes humuszba való átjutás során.
Embereken végzett vizsgálatok azt mutatják, hogy a vizes humusz csúcskoncentrációi körülbelül két órával a helyi alkalmazás után érhetők el. A majmok helyi csepegtetése után a latanoproszt elsősorban az elülső szegmensben, a kötőhártyában és a szemhéjban oszlik el. Csak kis mennyiségű gyógyszer jut el a hátsó szegmenshez.
A latanoproszt -sav gyakorlatilag nem metabolizálódik a szemben. Az anyagcsere főként a májban történik. "Emberben" a plazma felezési ideje 17 perc. Állatkísérletek kimutatták, hogy a fő metabolitok, az 1,2 -dinor és az 1,2,3,4 -tetranor, állatmodellekben nem, vagy csak gyenge biológiai aktivitást fejtenek ki, és főként a vizelettel választódnak ki.
05.3 A preklinikai biztonságossági adatok -
A latanoproszt szem- és szisztémás toxicitását számos állatfajban értékelték. A latanoprosztot általában jól tolerálják, a klinikai dózis és a szisztémás toxicitás közötti biztonsági határ legalább 1000 -szeres. A Latanoprost Actavis nagy dózisa, amely a klinikai dózis / testtömeg-kilogramm körülbelül 100-szorosa, intravénásan adva érzéstelenített majmoknak, a légzésszám növekedését mutatta, amelyet valószínűleg rövid életű hörgőszűkület okozhat. Állatkísérletekben a latanoproszt nem mutatott szenzibilizáló tulajdonságokat.
Nyulaknál vagy majmoknál nem figyeltek meg mérgező hatást a szemen 100 mg / nap / nap dózisig (klinikai dózis körülbelül 1,5 mcg / szem / nap).
Majmoknál azonban kimutatták, hogy a latanoproszt fokozza az írisz pigmentációját.
Úgy tűnik, hogy a hiperpigmentációt az írisz stromális melanocitáiban a melanin termelésének stimulálása okozza; proliferációs elváltozásokat nem észleltek. Az írisz színének változása tartós lehet.
A krónikus szemtoxicitással kapcsolatos vizsgálatok kimutatták, hogy a 6 mcg / nap / nap latanoproszt adagolása a szemhéj peremének megnagyobbodását idézheti elő. Ez a hatás visszafordítható, és a klinikai dózisnál magasabb dózisok beadása után jelentkezik. Ezt a hatást emberekben nem találták.
A latanoproszt negatív volt a baktériumok fordított mutációs tesztjeiben, az egér limfóma génmutációs tesztjeiben és az egér mikronukleusz tesztben. Kromoszóma -rendellenességeket figyeltek meg in vitro emberi limfocitákon. Hasonló hatásokat figyeltek meg a prosztaglandin F2α, a természetben előforduló prosztaglandin esetében is; ez azt jelzi, hogy ezek a hatások osztályfüggőek.
További mutagén vizsgálatok in vitro / in vivo patkányokban, nem tervezett DNS -szintézis során negatív eredményeket adtak, és azt jelzik, hogy a latanoprosztnak nincs mutagén tulajdonsága. Az egereken és patkányokon végzett karcinogenitási vizsgálatok negatívak voltak.
Állatkísérletek kimutatták, hogy a latanoproszt nincs hatással a hímek vagy nőstények termékenységére. Patkányokon végzett embrionális toxicitási vizsgálatokban nem találtak embrionális toxicitást a latanoproszt intravénás adagjaival (5,50 és 250 mikrogramm / kg / nap). A latanoproszt azonban embrió-halálos hatásokat vált ki nyulaknál 5 mcg / kg / nap vagy annál nagyobb dózisban.
Az 5 mcg / kg / nap dózis (a klinikai dózis körülbelül 100 -szorosa) jelentős embrionális és magzati toxicitást okozott, amelyet a késleltetett felszívódás, az abortusz és a magzat súlyának csökkenése jellemez.
Nem találtak teratogén potenciált.
06.0 GYÓGYSZERÉSZETI INFORMÁCIÓK
06.1 Segédanyagok -
Benzalkonium -klorid, egybázisú nátrium -foszfát -monohidrát, vízmentes kétbázisú nátrium -foszfát, nátrium -klorid, tisztított víz.
06.2 Inkompatibilitás "-
Oktatás in vitro kimutatták, hogy csapadék képződik, ha tiomerzált tartalmazó szemcseppet latanoproszthoz kevernek. Ha ezeket a gyógyszereket alkalmazzák, a szemcseppeket legalább 5 perces időközönként kell beadni.
06.3 Érvényességi idő "-
Eltarthatóság: 24 hónap
Felhasználhatósági időtartam felbontás után: 4 hét.
06.4 Különleges tárolási előírások -
Hűtőszekrényben (2 ° C - 8 ° C) tárolandó.
A fénytől való védelem érdekében tartsa a tartályt a külső tokban.
A tartály első kinyitása után: + 25 ° C felett tárolandó. Négy héttel az első felbontás után a gyógyszert ki kell dobni, még akkor is, ha nem használták fel teljesen.
06.5 A közvetlen csomagolás jellege és a csomagolás tartalma -
LDPE palack HPDE csavaros kupakkal.
Minden palack 2,5 ml szemcseppet tartalmaz, amely körülbelül 80 csepp oldatnak felel meg.
Kiszerelés: 1 x 2,5 ml.
06.6 Használati és kezelési útmutató -
Nincsenek speciális utasítások.
07.0 A „FORGALOMBA HOZATALI ENGEDÉLY” TULAJDONOSA -
ACTAVIS Group PTC ehf - Reykjavíkurvegi 76-78, 220 Hafnarfjörð (Izland)
08.0 A FORGALOMBA HOZATALI ENGEDÉLY SZÁMA -
Latanoprost Actavis 50 mcg / ml szemcsepp, oldat 1 üveg 2,5 ml LDPE - AIC n. 039238011 / M
09.0 AZ ELSŐ ENGEDÉLYZÉS ÉS A JÓVÁHAGYÁS MEGÚJÍTÁSÁNAK DÁTUMA -
Elhatározás n. 1414/2009 (2009.10.29.) - G.U. n. 271. 2009. 11. 20
10.0 A SZÖVEG FELÜLVIZSGÁLÁSÁNAK DÁTUMA -
2011. július