Hatóanyagok: klaritromicin
Veclam 125 mg / 5 ml granulátum belsőleges szuszpenzióhoz
A Veclam csomagbetétek a következő csomagolási méretekhez kaphatók:- Veclam 125 mg / 5 ml granulátum belsőleges szuszpenzióhoz
- Veclam 250 mg / 5 ml granulátum belsőleges szuszpenzióhoz
- Veclam 250 mg bevont tabletta
- Veclam 500 mg bevont tabletta
- Veclam RM 500 mg módosított hatóanyag -leadású tabletta
- Veclam 500 mg granulátum belsőleges szuszpenzióhoz
- Veclam 500 mg / 10 ml por és oldószer oldatos infúzióhoz
Miért alkalmazzák a Veclam -ot? Mire való?
GYÓGYSZERÉSZETI KATEGÓRIA
Általános antibakteriális szer szisztémás használatra - Makrolidok
GYÓGYSZERJELZÉSEK
A klaritromicinre érzékeny kórokozók által okozott fertőzések kezelése. Az orrszarv-garat traktus fertőzései (mandulagyulladás, garatgyulladás), a melléküregek. Akut középfülgyulladás (AOM). Alsó légúti fertőzések: hörghurut, bakteriális tüdőgyulladás és atipikus tüdőgyulladás. Bőrfertőzések: impetigo, erysipelas, folliculitis, furunculosis és fertőzött sebek.
A Veclam 125 mg / 5 ml granulátum belsőleges szuszpenzióhoz 6 hónapos és 12 éves kor közötti gyermekek kezelésére javallt.
Ellenjavallatok Amikor a Veclam -ot nem szabad alkalmazni
Túlérzékenység a makrolid osztályú antibiotikumokkal vagy a "Összetétel" részben felsorolt bármely segédanyaggal szemben.
A klaritromicin és az alábbi gyógyszerek bármelyikének egyidejű alkalmazása ellenjavallt: asztemizol, ciszaprid, pimozid, terfenadin, mivel ezek QT -intervallum megnyúlást és szívritmuszavarokat okozhatnak, beleértve a kamrai tachycardiát, a kamrai fibrillációt és a torsades de pointes -t.
A klaritromicin és a tikagrelor vagy a ranolazin egyidejű alkalmazása ellenjavallt.
A klaritromicin és az ergotalkaloidok (ergotamin vagy dihidroergotamin) egyidejű alkalmazása, amely ergottoxicitáshoz vezethet, ellenjavallt (lásd "Interakciók" pont).
A klaritromicin és a midazolám szájon át történő egyidejű alkalmazása ellenjavallt (lásd "Interakciók" pont).
A Veclam nem alkalmazható olyan betegeknél, akiknél dokumentáltan dokumentált veleszületett vagy szerzett QT -intervallum meghosszabbodott, és kórtörténetében kamrai aritmiát észleltek (lásd "Különleges figyelmeztetések" fejezet).
A Veclam-ot nem szabad együtt adni a HMG-CoA reduktáz inhibitorokkal (sztatinokkal), amelyeket a CYP3A4 (lovasztatin és szimvasztatin) nagymértékben metabolizál, a myopathia, beleértve a rabdomiolízist, fokozott kockázata miatt (lásd "Interakciók" pont).
A Veclam nem adható hypokalaemiás betegeknek (a QT -intervallum megnyúlásának veszélye).
A Veclam nem alkalmazható olyan betegeknél, akik vesekárosodással járó súlyos májelégtelenségben szenvednek.
A többi erős CYP3A4 enzim inhibitorhoz hasonlóan a klaritromicint sem szabad kolchicinnel együtt alkalmazni (lásd "Különleges figyelmeztetések" fejezet).
Az alkalmazással kapcsolatos óvintézkedések Mit kell tudnia a Veclam szedése előtt?
Mivel a klaritromicin elsősorban a májban metabolizálódik és ürül ki, különösen óvatosnak kell lenni, amikor a gyógyszert károsodott májfunkciójú betegeknek, valamint mérsékelt vagy súlyos vesekárosodásban szenvedő betegeknek adják.
Halálos májelégtelenségről számoltak be klaritromicin alkalmazása során, egyes betegeknél korábban májbetegségben szenvedtek, vagy más hepatotoxikus gyógyszereket szedtek.
A beteget tanácsolni kell, hogy hagyja abba a kezelést, és forduljon orvosához, ha májbetegség jelei és tünetei, például étvágytalanság, sárgaság, sötét vizelet, viszketés vagy hasi fájdalom jelentkeznek.
Pseudomembranosus colitis eseteiről számoltak be szinte minden antibakteriális szer alkalmazásával, beleértve a makrolidokat is, amelyek súlyossága mérsékeltől életveszélyesig terjed. Clostridium difficile hasmenés (CDAD) eseteiről számoltak be. amely a mérsékelt hasmenéstől a végzetes vastagbélgyulladásig terjedhet. Az antibakteriális kezelés megváltoztatja a normális bélflórát, ami a C. difficile túlzott proliferációjához vezethet.
Minden olyan betegnél, aki hasmenésre panaszkodik az antibiotikumok bevétele után, értékelni kell a CDAD jelenlétét. Ezeknek a betegeknek alapos kórtörténeten kell részt venniük, mivel jelentések szerint CDAD előfordulhat az antibakteriális szerek bevételét követő két hónapban. Ezért a klaritromicin -kezelést a terápiás indikációtól függetlenül meg kell szakítani, mikrobiális tesztet kell végezni, és meg kell kezdeni a megfelelő kezelést. Kerülni kell az antiperisztaltikus szerek alkalmazását.
Kölcsönhatások Mely gyógyszerek vagy ételek módosíthatják a Veclam hatását
Tájékoztassa kezelőorvosát vagy gyógyszerészét, ha nemrégiben szedett más gyógyszereket, beleértve a vény nélkül kapható készítményeket is.
A következő gyógyszerek alkalmazása abszolút ellenjavallt a gyógyszerkölcsönhatásukból adódó lehetséges súlyos hatások miatt: asztemizol, ciszaprid, pimozid, terfenadin.
Egyidejű bevétele meghosszabbította a QT -intervallumot, szívritmuszavarokat, beleértve a kamrai tachycardiát, a kamrai fibrillációt és a torsades de pointes -t (lásd "Ellenjavallatok").
Néhány forgalomba hozatalt követő jelentés azt jelzi, hogy a klaritromicin és az ergotamin vagy a dihidroergotamin együttes alkalmazása akut ergottoxicitással (ergotizmussal) jár együtt, amelyet vasospasmus és a végtagok és más szövetek, köztük a központi idegrendszer ischaemiája jellemez. A klaritromicin és az ergot alkaloidok egyidejű alkalmazása ellenjavallt (lásd "Ellenjavallatok" fejezet).
A klaritromicin és a lovasztatin vagy a szimvasztatin egyidejű alkalmazása ellenjavallt, mivel ezeket a sztatinokat nagymértékben metabolizálja a CYP3A4, és a klaritromicinnel történő egyidejű kezelés növeli plazmakoncentrációjukat, ami növeli a myopathia, beleértve a rabdomiolízist, kockázatát (lásd "Ellenjavallatok" pont).
Beszámoltak rabdomiolízisről azoknál a betegeknél, akik klaritromicint szedtek egyidejűleg ezekkel a sztatinokkal. Ha a klaritromicin -kezelést nem lehet elkerülni, a lovasztatin- vagy szimvasztatin -kezelést a kezelés ideje alatt fel kell függeszteni.
Óvatosan kell eljárni, amikor a klaritromicint sztatinokkal együtt írják fel. Azokban a helyzetekben, amikor a klaritromicin és a sztatinok egyidejű alkalmazását nem lehet elkerülni, ajánlott a statinok legalacsonyabb regisztrált dózisát előírni A sztatin alkalmazásának lehetősége, amely nem függ a CYP3A metabolizmusától (pl. Fluvasztatin). A betegeket figyelni kell a myopathia jeleire és tüneteire.
Más gyógyszerek hatása a klaritromicinre:
A CYP3A -t indukáló gyógyszerek (pl. Rifampicin, fenitoin, karbamazepin, fenobarbitál, orbáncfű) kiválthatják a klaritromicin metabolizmusát. Ez a klaritromicin szubterápiás szintjeihez vezet, csökkent terápiás hatékonysággal. Azok a gyógyszerek, amelyek erősen előidézik a citokróm P450 metabolizmusát, mint például az efavirenz, a nevirapin, a rifampicin, a rifabutin és a rifapentin, felgyorsíthatják a klaritromicin metabolizmusát, és következésképpen csökkenthetik a klaritromicin plazmaszintjét. növeli a 14-OH-klaritromicin, a mikrobiológiai szempontból is aktív metabolit plazmaszintjét.
Egy farmakokinetikai vizsgálat kimutatta, hogy 200 mg ritonavir 8 óránként és 500 mg klaritromicin 12 óránként történő egyidejű alkalmazása a klaritromicin metabolizmusának jelentős gátlásához vezet. A 14-OH klaritromicin képződésének teljes gátlását figyelték meg.
Az etravirin csökkentette a klaritromicin -expozíciót; azonban az aktív metabolit, a 14-OH-klaritromicin koncentrációja megnőtt. Mivel a 14-OH-klaritromicin csökkent aktivitást mutat a Mycobacterium Avium Complex (MAC) ellen, a kórokozóval szembeni általános aktivitás megváltozhat, ezért a MAC kezelésében fontolóra kell venni a klaritromicin alternatíváit.
A napi 200 mg flukonazol és a naponta kétszer 500 mg klaritromicin 21 egészséges önkéntes egyidejű alkalmazása 33% -kal, illetve 18% -kal növelte a klaritromicin átlagos minimális koncentrációját (Cmin) és a görbe alatti területet (AUC). az aktív metabolitot, a 14-OH-klaritromicint nem befolyásolta jelentősen a flukonazol egyidejű alkalmazása.
A klaritromicin dózisának módosítása nem szükséges.
A klaritromicin hatása más gyógyszerekre:
A klaritromicin, amelyről ismert, hogy gátolja a CYP3A -t, és egy elsősorban CYP3A által metabolizált gyógyszer egyidejű alkalmazása a gyógyszerkoncentráció növekedésével járhat, ami fokozhatja vagy meghosszabbíthatja az egyidejűleg alkalmazott gyógyszer terápiás és káros hatásait.
A klaritromicint óvatosan kell alkalmazni azoknál a betegeknél, akik olyan gyógyszereket kapnak, amelyekről úgy gondolják, hogy a CYP3A enzim szubsztrátjai, különösen akkor, ha a CYP3A szubsztrátnak szűk a biztonsági határa (pl. Karbamazepin), és / vagy ha ez a szubsztrát nagymértékben metabolizálódik enzim.
Az egyidejű klaritromicin -kezelésben részesülő betegeknél mérlegelni kell az adagolás módosítását, és lehetőség szerint gondosan ellenőrizni kell az elsősorban CYP3A által metabolizált gyógyszerek szérumkoncentrációját.
Azok a gyógyszerek vagy gyógyszerosztályok, amelyeket ismert vagy feltételezett módon ugyanaz a CYP3A izoenzim metabolizál: rifabutin, szildenafil, szimvasztatin, szirolimusz, takrolimusz, terfenadin, triazolam és vinblasztin, de ez a lista nem teljes.
A citokróm P450 rendszeren belül hasonló mechanizmussal kölcsönhatásba lépő egyéb gyógyszerek a fenitoin, a teofillin és a valproát. Megnövekedett szérumszintről számoltak be. Egyéb torsades de pointes eseteket jelentettek klaritromicin és kinidin vagy disopiramid egyidejű alkalmazása után. A klaritromicin terápia alkalmazása során ellenőrizze ezen gyógyszerek szérumkoncentrációját.
A klaritromicin és a disopiramid egyidejű alkalmazása után hipoglikémiás eseteket jelentettek. A kezelés során ellenőrizni kell a vércukorszintet. A klaritromicin bizonyos hipoglikémiás gyógyszerekkel, például nategliniddel és repagliniddel történő egyidejű alkalmazása esetén a CYP3A enzim klaritromicin gátlása léphet fel, és hipoglikémiát okozhat. A glükózszint gondos monitorozása ajánlott.
Omeprazol
Egészséges felnőtt alanyok kaptak klaritromicint (500 mg 8 óránként) omeprazollal kombinálva (napi 40 milligramm). Az omeprazol kiindulási plazmakoncentrációja megnőtt (Cmax, AUC0-24 és T1 / 2 30%, 89% és 34 %) a klaritromicin egyidejű alkalmazása miatt.
A gyomor átlagos pH -értéke 24 óra alatt 5,2 volt, ha az omeprazolt önmagában adták, és 5,7 volt, amikor az omeprazolt klaritromicinnel együtt adták.
Szildenafil, tadalafil és vardenafil
Ezen foszfodiészteráz inhibitorok mindegyike metabolizálódik, legalább részben, a CYP3A által, és a CYP3A gátolható a klaritromicin egyidejű alkalmazásával. A klaritromicin és a szildenafil, tadalafil vagy vardenafil egyidejű alkalmazása nagy valószínűséggel fokozza a foszfodiészteráz -gátló expozícióját. Ezért fontolóra kell venni a szildenafil, a tadalafil és a vardenafil adagjának csökkentését, ha ezeket a gyógyszereket klaritromicinnel együtt adják.
A klinikai vizsgálatok eredményei azt mutatták, hogy a karbamazepin és a teofillin plazmaszintje szerény, de statisztikailag szignifikáns mértékben megemelkedhet, ha ezeket klaritromicinnel együtt alkalmazzák.
Tolterodina
A tolterodin fő metabolikus útja a citokróm P450 (CYP2D6) 2D6 izoformáján halad át. Azonban egy CYP2D6 nélküli populáció alcsoportban az azonosított metabolikus útvonal a CYP3A. Ebben a populáció alcsoportban a CYP3A gátlás. Szignifikánsan magasabb szérum tolterodin koncentrációt eredményez . CYP3A inhibitorok jelenlétében szükség lehet a tolterodin dózisának csökkentésére, valamint a klaritromicin dózisának csökkentésére azon betegek körében, akiknél a CYP2D6 gyengén metabolizálódik.
Egyéb gyógyszerkölcsönhatások:
Óvatosság ajánlott klaritromicin és más ototoxikus gyógyszerek, különösen aminoglikozidok egyidejű alkalmazásakor (lásd "Figyelmeztetések" pont).
A kolchicin mind a CYP3A, mind a kiáramló transzporter P-glikoprotein (Pgp) szubsztrátja. A klaritromicinről és más makrolidokról ismert, hogy gátolják a CYP3A-t és a Pgp-t. A klaritromicin és a kolhicin egyidejű alkalmazásakor a CYP3A gátlása és / vagy a klaritromicin által okozott Pgp fokozott kolhicin expozíció. Figyelje a betegeket a kolhicin toxicitás klinikai tünetei tekintetében (lásd "Használati óvintézkedések" fejezet).
A klaritromicinnel és digoxinnal kezelt betegeknél az utóbbiak szérumkoncentrációja megnőtt, ezért a digoxin szintjét ellenőrizni kell a zidovudin egyensúlyi állapotában.
Mivel a klaritromicin látszólag zavarja az egyidejűleg szájon át adott zidovudin felszívódását, ez a kölcsönhatás erősen elkerülhető a klaritromicin és a zidovudin dózisának legalább 4 órás intervallummal történő növelésével.
Ez a kölcsönhatás nem jelenik meg HIV -fertőzött gyermekbetegeknél, ha a klaritromicint granulált formában, a zidovudinnal vagy a didanozinnal egyidejűleg veszik be.
Fenitoin és valproát:
Spontán vagy publikált jelentések érkeztek arról, hogy a CYP3A -gátlók, köztük a klaritromicin kölcsönhatásba lépnek olyan gyógyszerekkel, amelyeket nem tekintünk a CYP3A által metabolizálhatónak (pl. Fenitoin és valproát). Ezeknek a gyógyszereknek a szérumszint meghatározása javasolt, ha klaritromicinnel együtt alkalmazzák. A szérum emelkedett szintjeiről számoltak be.
Kétirányú gyógyszerkölcsönhatások:
A klaritromicin és az atazanavir, mint az itrakonazol és a szakinavir, a CYP3A szubsztrátjai és gátlói, és bizonyítékok vannak a kétirányú kölcsönhatásokra ezen gyógyszerek között.
Óvatosság szükséges a klaritromicin és a CYP3A4 által metabolizált kalciumcsatorna -blokkolók (pl. Verapamil, amlodipin, diltiazem) egyidejű alkalmazásakor a hipotenzió veszélye miatt. A klaritromicin, valamint a kalciumcsatorna -blokkolók plazmakoncentrációja az interakció miatt megnőhet.Klaritromicint és verapamilt egyidejűleg szedő betegeknél hipotenziót, bradiaritmiát és tejsavas acidózist figyeltek meg.
Figyelmeztetések Fontos tudni, hogy:
Óvatosan kell eljárni azoknál a betegeknél, akik súlyos veseelégtelenségben szenvednek (lásd "Adagolás, alkalmazás és idő" fejezet). Mivel a klaritromicin főként a májban ürül, különleges óvatossággal kell eljárni, amikor az antibiotikumot májkárosodásban szenvedő betegeknek és mérsékelt vagy súlyos vesekárosodásban szenvedő betegeknek adják be.
Úgy tűnik, hogy a klaritromicin plazmaszintje nem változik érezhetően hemodialízissel vagy peritoneális dialízissel.
A legtöbb antibakteriális szer, beleértve a makrolidokat, alkalmazása pszeudomembranosus colitist és enyhe vagy nagyon súlyos Clostridium difficile hasmenést okozhat. A kolchicin és a klaritromicin együttes alkalmazása során jelentették a kolchicin toxicitás forgalomba hozatal utáni eseteit, különösen idős betegeknél. veseelégtelenségben szenvedő betegeknél jelentettek eseteket, és ezek közül néhány betegnél halálozást jelentettek (lásd "Interakciók" pont).
A klaritromicin és a kolhicin egyidejű alkalmazása ellenjavallt (lásd "Ellenjavallatok" pont).
Óvatosság ajánlott klaritromicin és triazolobenzodiazepinek, például triazolam és injekciós midazolám egyidejű alkalmazásakor (lásd "Interakciók" pont). Óvatosság szükséges a klaritromicin és más ototoxikus gyógyszerek, különösen az aminoglikozidok egyidejű alkalmazásakor. Ezért tanácsos rendszeresen ellenőrizni a vestibularis és hallási funkciót a kezelés alatt és után.
A QT -intervallum megnyúlásának kockázata miatt a klaritromicint óvatosan kell alkalmazni koszorúér -betegségben, súlyos szívelégtelenségben, hipomagnesémiában, bradycardiában szenvedő betegeknél.
A Streptococcus pneumoniae makrolidokkal szembeni rezisztenciájának előrejelzésében fontos, hogy a klaritromicin felírása előtt érzékenységi tesztet végezzenek a közösségben szerzett tüdőgyulladás kezelésére.
A közepes és közepes fokú bőr- és lágyrészfertőzéseket leggyakrabban a Staphylococcus aureus és a Streptococcus pyogenes okozza, amelyek mindketten rezisztensek lehetnek a makrolidokkal szemben. Ezután érzékenységi tesztet kell végezni. Azokban az esetekben, amikor a béta-laktám antibiotikumok nem alkalmazhatók (pl. Allergia), előnyösebb más antibiotikumokat, például klindamicint használni.
Súlyos akut túlérzékenységi reakciók, például anafilaxia, Stevens-Johnson-szindróma, toxikus epidermális nekrolízis és DRESS-szindróma esetén a klaritromicin-kezelést azonnal abba kell hagyni, és a megfelelő kezelést azonnal el kell kezdeni.
A klaritromicin és a lovasztatin vagy a szimvasztatin egyidejű alkalmazása ellenjavallt (lásd az "Ellenjavallatok" pontot). Óvatosan kell eljárni, amikor a klaritromicint más sztatinokkal együtt írják fel. Klaritromicint és sztatinokat szedő betegeknél jelentettek rabdomiolízist. A betegeket monitorozni kell a myopathia jelei és tünetei szempontjából. Azokban a helyzetekben, amikor a klaritromicin és a sztatinok egyidejű alkalmazása nem kerülhető el, ajánlott a statinok legalacsonyabb regisztrált adagját előírni.A CYP3A enzim (pl. Fluvasztatin) metabolizmusától független sztatin alkalmazásának lehetőségét mérlegelni kell (lásd "Interakciók" pont).
"A klaritromicin és az orális hipoglikémiás szerek (például szulfonil -karbamidok) és / vagy az inzulin egyidejű alkalmazása súlyos hypoglykaemiához vezethet. A C" súlyos vérzés kockázata, valamint a nemzetközi normalizált arány (INR) és a protrombin idő jelentős növekedése a klaritromicin alkalmazása esetén. warfarinnal együtt adva (lásd "Interakciók" pont).
A gyógyszer hosszú távú használata, hasonlóan más antibiotikumokhoz, szuperfertőzést okozhat rezisztens baktériumoktól vagy gombáktól. Ha túlfertőzések alakulnak ki, a kezelést abba kell hagyni, és azonnal meg kell kezdeni a megfelelő terápiát. Figyelmet kell fordítani a klaritromicin és más makrolidok, linkomicin és klindamicin közötti keresztrezisztencia lehetőségére.
Fontos információk egyes összetevőkről
A Veclam granulátum belsőleges szuszpenzióhoz szacharózt tartalmaz. Azok a betegek, akiket orvosuk "bizonyos cukrok intoleranciájával" diagnosztizál, kapcsolatba kell lépnie vele a gyógyszer szedése előtt.
Amikor cukorbetegeknek rendelnek Veclam granulátumot belsőleges szuszpenzióhoz, figyelembe kell venni a szacharóztartalmat.
A gyógyszer nem ellenjavallt a lisztérzékenységben szenvedők számára.
A Veclam granulátum belsőleges szuszpenzióhoz ricinusolajat is tartalmaz, ami gyomorpanaszokat és hasmenést okozhat.
Terhesség és szoptatás
Mielőtt bármilyen gyógyszert elkezdene szedni, kérdezze meg kezelőorvosát vagy gyógyszerészét. A klaritromicint nem szabad terhes nőknek felírni „gondos előny / kockázat értékelés” nélkül, különösen a terhesség első trimeszterében (lásd „Különleges figyelmeztetések” pont).
A klaritromicin olyan mennyiségben választódik ki az anyatejbe, hogy az újszülöttekre / csecsemőkre gyakorolt hatás valószínű.
Hatások a gépjárművezetéshez és gépek kezeléséhez szükséges képességekre
Nincsenek adatok a klaritromicin gépjárművezetéshez és gépek kezeléséhez szükséges képességekre gyakorolt hatásáról. Mielőtt a beteg vezetne vagy gépeket kezelne, mérlegelni kell a szédülés, a szédülés, a zavartság és a tájékozódásveszély kockázatát, amely az alkalmazás után előfordulhat.
Adagolás és alkalmazás A Veclam alkalmazásának módja: Adagolás
6 hónapos és 12 éves gyermekek
A klaritromicin ajánlott napi adagja 6 hónapos és 12 év közötti gyermekek esetében 7,5 mg / kg, amelyet naponta kétszer kell beadni nem mikobakteriális fertőzések esetén. A kezelés szokásos időtartama 5-10 nap, az érintett kórokozóktól és a helyzet súlyosságától függően.
Adagolási séma Veclam 125 mg / 5 ml granulátum belsőleges szuszpenzióhoz Kanál használata:
A szuszpenzió elkészítése: A Veclam szuszpenzió elkészítéséhez adjon vizet a palackban lévő granulátumhoz a palackon lévő piros vonalig.
Jól rázza fel. Adjon hozzá több vizet, hogy visszajusson a vezetékbe.
Az így elkészített szuszpenzió koncentrációja 2,5%, és szobahőmérsékleten 14 napig tárolható.
Minden használat előtt jól rázza fel.
Veseelégtelenségben szenvedő betegeknél, akik kreatinin clearance értéke kisebb, mint 30 ml / perc, a klaritromicin adagját felére kell csökkenteni. Ezeknél a betegeknél a kezelést nem szabad 14 napnál tovább folytatni.
Túladagolás Mi a teendő, ha túl sok Veclam -ot vett be?
Ha véletlenül lenyeli / beveszi a Veclam túlzott adagját, azonnal értesítse orvosát, vagy menjen a legközelebbi kórházba.
Emésztőrendszeri zavarok léphetnek fel, ha nagy mennyiségű klaritromicint szednek. A túladagolás esetén fellépő mellékhatásokat a felszívódott gyógyszer azonnali megszüntetésével és megfelelő támogató terápiákkal kell kezelni. Más makrolidokhoz hasonlóan a klaritromicin szérumszintje sem szűnik meg hemodialízissel vagy peritoneális dialízissel, ezért beavatkozni kell a lehető leghamarabb megpróbálja megszüntetni a még nem felszívódó gyógyszert a megfelelő tüneti terápiával egyidejűleg.
Ha bármilyen kérdése van a Veclam alkalmazásával kapcsolatban, kérdezze meg kezelőorvosát vagy gyógyszerészét.
Mellékhatások Melyek a Veclam mellékhatásai?
Mint minden gyógyszer, így a Veclam is okozhat mellékhatásokat, amelyek azonban nem mindenkinél jelentkeznek. Az alábbiakban felsoroljuk a Veclam mellékhatásait.
nak nek. A biztonsági profil összefoglalása
A klaritromicin -terápiával kapcsolatos leggyakoribb és leggyakoribb mellékhatások mind felnőtt, mind gyermekgyógyászati betegeknél a hasi fájdalom, hasmenés, hányinger, hányás és ízérzés. Ezek a mellékhatások általában közepes intenzitásúak, és összhangban vannak a makrolid antibiotikumok ismert biztonsági profiljával.
A klinikai vizsgálatok során nincsenek szignifikáns különbségek ezen gasztrointesztinális mellékhatások előfordulási gyakoriságában a már meglévő mycobacterium fertőzésben szenvedő betegek vagy azok nélkül.
b. A mellékhatások összefoglaló táblázata
Az alábbi táblázat összefoglalja a klaritromicin azonnali hatóanyag-leadású tablettákkal, granulátumokkal az orális szuszpenzióhoz és a módosított hatóanyag-leadású tablettákkal végzett klinikai vizsgálatok során és a forgalomba hozatalt követően jelentett mellékhatásokat.
A klaritromicinnel kapcsolatban állónak ítélt mellékhatásokat szervtípus és gyakoriság szerint jelentik a következő megállapodás szerint: nagyon gyakori (≥1 / 10), gyakori (≥1 / 100,
* Mivel ezeket a reakciókat önként jelentették egy határozatlan méretű populációból, nem mindig lehetséges a gyakoriság valódi becslése, vagy ok-okozati összefüggés megállapítása a gyógyszer expozíciójával. kezelés klaritromicinnel
** A bejelentett rabdomiolízis esetek egy részében a klaritromicint sztatinokkal, fibrátokkal, kolhicinnel vagy allopurinollal egyidejűleg alkalmazták.
1 Mellékhatás, amelyet csak az infúziós oldathoz készült por és oldószer készítmény esetében jelentettek
2 Mellékhatást csak az orális szuszpenzió granulátumánál jelentettek
3 A mellékhatásokról csak az azonnali hatóanyag -leadású tabletták esetében számoltak be
4, 6, 8,9 Lásd a) pont
5, 7, 10 Lásd c) pont
c. A kiválasztott mellékhatások leírása
A jelentett rabdomiolízis esetek egy részében a klaritromicint sztatinokkal, fibrátokkal, kolhicinnel vagy allopurinollal együtt alkalmazták.
A klaritromicin és a triazolam egyidejű alkalmazásakor a forgalomba hozatalt követően beszámoltak gyógyszerkölcsönhatásokról és központi idegrendszeri (CNS) hatásokról (pl. Aluszékonyság és zavartság). Javasolt, hogy a beteget fokozott farmakológiai hatásokra figyelemmel kísérjék központi idegrendszeri szinten.
d. Gyermekpopulációk
Klinikai vizsgálatokat végeztek a klaritromicin-alapú gyermek szuszpenzió 6 hónapos és 12 éves kor közötti gyermekeknek történő beadásával. Következésképpen a 12 év alatti gyermekeknek fel kell venniük a gyermek szuszpenziót.
A mellékhatások gyakorisága, típusa és súlyossága várhatóan hasonló lesz a felnőtteknél tapasztaltakhoz.
Mellékhatások bejelentése
Ha Önnél bármilyen mellékhatás jelentkezik, tájékoztassa erről kezelőorvosát vagy gyógyszerészét. Ez a betegtájékoztatóban fel nem sorolt bármilyen lehetséges mellékhatásra is vonatkozik. A nemkívánatos hatások közvetlenül a "www.agenziafarmaco.gov.it/it/responsabili" nemzeti jelentési rendszeren keresztül is jelenthetők. A mellékhatások bejelentésével Ön is hozzájárulhat ahhoz, hogy minél több információ álljon rendelkezésre a gyógyszer biztonságosságáról. "
Lejárat és megőrzés
Lejárati idő: Lásd a csomagoláson feltüntetett lejárati dátumot.
A feltüntetett lejárati idő az ép csomagolású termékre vonatkozik, helyesen tárolva.
Ez a gyógyszer nem igényel különleges tárolási körülményeket.
FIGYELEM: Ne használja a gyógyszert a csomagoláson feltüntetett lejárati idő után.
A gyógyszereket nem szabad a szennyvízzel vagy a háztartási hulladékkal együtt megsemmisíteni. Kérdezze meg gyógyszerészét, hogy mit tegyen a már nem használt gyógyszereivel. Ez elősegíti a környezet védelmét.
A gyógyszer gyermekektől elzárva tartandó!
Összetétel és gyógyszerforma
FOGALMAZÁS:
100 ml feloldott szuszpenzió a következőket tartalmazza:
Hatóanyag: 2,5 g klaritromicin
Segédanyagok: Carbopol 974, povidon, hipromellóz -ftalát, ricinusolaj, szilikagél, szacharóz, xantángumi, kevert gyümölcs aroma, kálium -szorbát, citromsav, titán -dioxid, maltodextrin, víz.
GYÓGYSZERFORMA ÉS TARTALOM
Granulátum belsőleges szuszpenzióhoz - 100 ml -es műanyag palack adagolóval.
Forrás betegtájékoztató: AIFA (Olasz Gyógyszerügynökség). A tartalom 2016 januárjában jelent meg. A jelenlévő információk nem feltétlenül naprakészek.
A legfrissebb verzióhoz való hozzáféréshez ajánlatos az AIFA (Olasz Gyógyszerügynökség) webhelyét elérni. Jogi nyilatkozat és hasznos információk.
01.0 A GYÓGYSZER MEGNEVEZÉSE
VECLAM
02.0 MINŐSÉGI ÉS MENNYISÉGI ÖSSZETÉTEL
- Veclam 250 mg bevont tabletta:
Minden bevont tabletta tartalmaz:
Aktív elv:
klaritromicin 250 mg.
Nátriumtartalom: 3,4 mg tablettánként
- Veclam 500 mg bevont tabletta:
Minden bevont tabletta tartalmaz:
Aktív elv:
klaritromicin 500 mg.
Nátriumtartalom: 6,1 mg tablettánként
- Veclam 125 mg / 5 ml granulátum belsőleges szuszpenzióhoz:
100 ml feloldott szuszpenzió a következőket tartalmazza:
Aktív elv:
2,50 g klaritromicin.
Ismert hatású segédanyagok: szacharóz 550 mg / ml;
ricinusolaj 3,2 mg / ml.
- Veclam 250 mg / 5 ml granulátum belsőleges szuszpenzióhoz:
100 ml feloldott szuszpenzió a következőket tartalmazza:
Aktív elv:
klaritromicin 5,00 g.
Ismert hatású segédanyagok: szacharóz 455 mg / ml;
ricinusolaj 6,4 mg / ml.
- Veclam 250 mg granulátum belsőleges szuszpenzióhoz:
Minden tasak tartalma:
Aktív elv:
klaritromicin 250 mg.
Ismert hatású segédanyagok: tasakonként 1591 mg szacharóz;
ricinusolaj 32,1 mg tasakonként.
- Veclam 500 mg granulátum belsőleges szuszpenzióhoz:
Minden tasak tartalma:
Aktív elv:
klaritromicin 500 mg.
Ismert hatású segédanyagok: 3182 mg szacharóz tasakonként;
ricinusolaj 64,2 mg tasakonként.
- Veclam 500 mg / 10 ml por és oldószer oldatos infúzióhoz:
Minden injekciós üveg steril por oldatos infúzióhoz tartalmaz:
Aktív elv
klaritromicin 500 mg.
- Veclam RM 500 mg módosított hatóanyag -leadású tabletta:
Minden módosított hatóanyag-leadású tabletta tartalmaz:
Aktív elv:
klaritromicin 500 mg.
Nátriumtartalom 15,3 mg tablettánként
Ismert hatású segédanyagok: laktóz (115 mg tablettánként).
A segédanyagok teljes listáját lásd a 6.1 pontban.
03.0 GYÓGYSZERFORMA
- Bevonatos tabletta.
- Granulátum belsőleges szuszpenzióhoz.
- Por és oldószer oldatos infúzióhoz.
- Módosított felszabadulású tabletták.
04.0 KLINIKAI INFORMÁCIÓK
04.1 Terápiás javallatok
Meg kell fontolni az antibakteriális szerek megfelelő alkalmazására vonatkozó hivatalos útmutatást.
A Veclam felnőttek és 12 évesnél idősebb gyermekek kezelésére javallt.
A Veclam 125 mg / 5 ml granulátum belsőleges szuszpenzióhoz és a Veclam 250 mg / 5 ml granulátum belsőleges szuszpenzióhoz 6 hónapos és 12 éves kor közötti gyermekek kezelésére javallt.
Minden gyógyszerforma esetében:
A klaritromicinre érzékeny kórokozók által okozott fertőzések kezelése. Az orrszarv-garat traktus fertőzései (mandulagyulladás, garatgyulladás), a melléküregek. Alsó légúti fertőzések: hörghurut, bakteriális tüdőgyulladás és atipikus tüdőgyulladás. Bőrfertőzések: impetigo, erysipelas, folliculitis, furunculosis és fertőzött sebek.
Ezenkívül a Veclam 125 mg / 5 ml granulátum belsőleges szuszpenzióhoz és a Veclam 250 mg / 5 ml granulátum belsőleges szuszpenzióhoz:
Akut középfülgyulladás (AOM).
Ezenkívül a Veclam 250 mg bevont tabletta és a Veclam 250 mg granulátum belsőleges szuszpenzióhoz:
Akut és krónikus odontostomatológiai fertőzések, amelyeket érzékeny csírák tartanak fenn.
Ezenkívül a Veclam 500 mg bevont tabletta, a Veclam 250 mg granulátum belsőleges szuszpenzióhoz és a Veclam 500 mg granulátum belsőleges szuszpenzióhoz:
A Mycobacterium avium vagy a Mycobacterium intracellulare által okozott lokális vagy diffúz mycobacterium fertőzések.
A Mycobacterium chelonae, fortuitum vagy kansasii okozta lokális fertőzések.
A klaritromicin a gyomorsav csökkenésének jelenlétében javallt a Helicobacter pylori felszámolásában, ennek következtében csökken a peptikus fekély kiújulása.
04.2 Adagolás és alkalmazás
12 év feletti gyermekeknél: mint a felnőtteknél.
A kezelés szokásos időtartama 5-14 nap, kivéve a közösségben szerzett tüdőgyulladás és arcüreggyulladás kezelését, amely 6-14 napig tart.
12 év alatti gyermekeknél: használjon Veclam 125 mg / 5 ml granulátumot belsőleges szuszpenzióhoz vagy Veclam 250 mg / 5 ml granulátumot belsőleges szuszpenzióhoz.
A kezelés szokásos időtartama 5-10 nap.
A Veclam bevont tabletta, a Veclam módosított hatóanyag -leadású tabletta vagy a Veclam por és oldószer oldatos infúzióhoz nem ajánlott 12 év alatti gyermekek számára.
Veclam 250 mg bevont tabletta, Veclam 500 mg bevont tabletta, Veclam 250 mg granulátum belsőleges szuszpenzióhoz e Veclam 500 mg granulátum belsőleges szuszpenzióhoz:
A klaritromicin ajánlott adagja felnőtteknél és 12 évesnél idősebb gyermekeknél 1 tabletta vagy 1 tasak 250 mg 12 óránként.
Súlyos fertőzések esetén az adag 12 óránként 500 mg -ra emelhető.
A kezelés szokásos időtartama 5-14 nap, kivéve a közösségben szerzett tüdőgyulladás és arcüreggyulladás kezelését, amely 6-14 napig tart.
Vesekárosodásban szenvedő betegek: veseelégtelenségben szenvedő betegeknél, akiknél a kreatinin clearance kevesebb, mint 30 ml / perc, az adagot felére kell csökkenteni, például 250 mg -ot naponta egyszer vagy 250 mg -ot naponta kétszer súlyos fertőzések esetén.
Ilyen betegeknél az adagolást nem szabad 14 napon túl folytatni.
Mikobakteriális fertőzésben szenvedő betegeknél a kezdő adag naponta kétszer 500 mg. Ha 3-4 héten belül nem tapasztalható klinikai javulás vagy bakteriológiai bizonyíték, a napi dózist napi kétszer 1000 mg-ra lehet emelni.
A Mycobacterium Avium Complex által terjesztett fertőzések AIDS -ben szenvedő betegeknél történő kezelésében ajánlatos a kezelést addig folytatni, amíg klinikai vagy mikrobiológiai eredményeket nem kapnak, és minden esetben a kezelőorvos döntése szerint. A klaritromicint más gyógyszerekkel együtt kell alkalmazni. antimikrobiális gyógyszerek.
Odontostomatológiai fertőzések esetén az ajánlott adag 250 mg 12 óránként 5 napig.
Adagolási rend a Helicobacter pylori felszámolásához:
Hármas terápia:
A klaritromicin 500 mg naponta kétszer, napi 20 mg omeprazollal és 1000 mg amoxicillinnel naponta kétszer, 7-10 napon keresztül.
Klaritromicin 500 mg naponta kétszer, napi kétszer 30 mg lanzoprazollal és napi kétszer 1000 mg amoxicillinnel kombinálva 10 napon keresztül.
Kettős terápia:
Klaritromicin 500 mg naponta háromszor, napi 40 mg omeprazollal kombinálva 14 napon keresztül, majd további 20 napig 20 mg vagy 40 mg omeprazol további 14 napon keresztül.
Klaritromicin 500 mg naponta háromszor, napi 60 mg lanzoprazollal kombinálva 14 napon keresztül. A fekély csökkentéséhez szükség lehet a savas szekréció további elnyomására.
A klaritromicint a következő terápiás módszerekben is alkalmazták:
- klaritromicin + tinidazol és omeprazol vagy lanzoprazol
- klaritromicin + metronidazol és omeprazol vagy lanzoprazol
- klaritromicin + tetraciklin, szubszalicilát -bizmut és ranitidin
- klaritromicin + amoxicillin és lanzoprazol
- klaritromicin + ranitidin -bizmut -citrát
A belsőleges szuszpenzió elkészítése tasakokban:
A szuszpenzió tasakokban való elkészítéséhez a tasak tartalmát a beadáskor öntsük egy pohár vízbe, majd rázzuk, amíg homogén szuszpenziót nem kapunk.
A Veclam bevont tabletták alkalmazását 12 év alatti gyermekeknél nem vizsgálták.
Veclam RM 500 mg módosított hatóanyag -leadású tabletta:
A Veclam RM 500 mg módosított hatóanyag -leadású tabletta ajánlott adagja felnőtteknél és 12 évesnél idősebb gyermekeknél naponta 1 tabletta, amelyet étkezés közben kell bevenni.
Súlyosabb fertőzések esetén az adag napi 2500 mg módosított hatóanyag-leadású tablettára emelhető, amelyet egyetlen adagként kell bevenni.
A tablettákat egészben kell lenyelni.
A kezelés szokásos időtartama 5-14 nap, kivéve a közösségben szerzett tüdőgyulladás és arcüreggyulladás kezelését, amely 6-14 napig tart.
Vesekárosodásban szenvedő betegek: veseelégtelenségben szenvedő betegeknél, akik kreatinin clearance értéke 30 ml / perc alatt van, a klaritromicin adagját felére kell csökkenteni, pl. 250 mg naponta egyszer, vagy 250 mg naponta kétszer súlyos fertőzések esetén. Ezeknél a betegeknél a kezelést nem szabad 14 napnál tovább folytatni. Mivel a tabletta nem osztható fel, és a napi 500 mg-os adag nem csökkenthető, a módosított hatóanyag-leadású tablettát nem szabad adni ennek a betegpopulációnak (lásd 4.3 pont).
A Veclam módosított hatóanyag -leadású tabletták alkalmazását 12 év alatti gyermekeknél nem vizsgálták.
Veclam 125 mg / 5 ml granulátum belsőleges szuszpenzióhoz és Veclam 250 mg / 5 ml granulátum belsőleges szuszpenzióhoz:
Klinikai vizsgálatokat végeztek a klaritromicin-alapú gyermek szuszpenzió 6 hónapos és 12 éves kor közötti gyermekeknek történő beadásával. Következésképpen a 12 év alatti gyermekeknek be kell venniük a gyermek szuszpenziót (granulátum belsőleges szuszpenzióhoz).
Az ajánlott napi adag gyermekeknél 7,5 mg / kg, naponta kétszer beadva nem mycobacterium fertőzések esetén.
A kezelés szokásos időtartama 5-10 nap, az érintett kórokozóktól és a helyzet súlyosságától függően.
A szuszpenziót étkezés közben és éhgyomorra is be lehet venni, és tejjel is le lehet nyelni.
Adagolási rend Veclam 125 mg / 5 ml granulátum belsőleges szuszpenzióhoz
A teáskanál használata
Adagolási rend Veclam 125 mg / 5 ml granulátum belsőleges szuszpenzióhoz
Az adagoló fecskendő használata egyszeri beadáshoz
(Szívja fel a szuszpenziót a megfelelő kg jelig)
Adagolási rend Veclam 250 mg / 5 ml granulátum belsőleges szuszpenzióhoz
A teáskanál használata
Adagolási rend Veclam 250 mg / 5 ml granulátum belsőleges szuszpenzióhoz
Az adagoló fecskendő használata egyszeri beadáshoz
(Szívja fel a szuszpenziót a megfelelő kg jelig)
A belsőleges szuszpenzió elkészítése palackban:
A Veclam szuszpenzió elkészítése:
- adjon hozzá vizet a palackban lévő granulátumhoz a palackon lévő piros vonalig.
- Jól rázza fel.
- Adjon hozzá több vizet, hogy visszajusson a vezetékbe.
Az így előállított szuszpenzió koncentrációja 5% Veclam 250 mg / 5 ml belsőleges szuszpenziós granulátum esetén és 2,5% Veclam 125 mg / 5 ml belsőleges szuszpenziós granulátum esetén, és szobahőmérsékleten (15 ° C - 30 ° C) tárolható ) 14 napig.
Minden használat előtt jól rázza fel.
Az adagoló fecskendő használata
Csavarja le a kupakot az üvegen. Helyezze be a fecskendőt a palack nyakába a speciális adapter segítségével. Szívja ki az adagoló skáláján feltüntetett kívánt adagot, és miután csak a fecskendőt kivette, végezze el az adagolást. Ezután az adapter behelyezése után csavarja vissza a kupakot az üveg nyakán.
Az adagot a fecskendő skálájával kell kiválasztani, a gyermek megfelelő testtömegéig.
Veclam 500 mg / 10 ml por és oldószer oldatos infúzióhoz:
Az ajánlott adag 18 év feletti felnőtt betegeknél 4-8 mg / kg / nap, két napi adagban. Az injekciózandó oldat elkészítése a por oldószerben való feloldásával, majd 5% -os glükóz vagy fiziológiás oldat hígításával történik, amíg el nem éri az 1-2 mg / ml végkoncentrációt.
Célszerű azonban nem túllépni a maximális napi 1 g -os adagot két napi beadáskor.
Az elkészített készítményt 24 órán belül fel kell használni.
Ne használjon sóoldatot oldószerként. Nagyon lassan adja be az injekciót.
Az adagolást a fertőzés súlyosságától függően legfeljebb 6-14 napig kell folytatni.
Vesekárosodásban szenvedő betegek: veseelégtelenségben szenvedő betegeknél, akiknél a kreatinin clearance kevesebb, mint 30 ml / perc, az adagot felére kell csökkenteni.
Ilyen betegeknél az adagolást nem szabad 14 napon túl folytatni.
Nincs elegendő adat ahhoz, hogy a klaritromicin IV adagolási rendjét 12 évesnél fiatalabb betegeknél alkalmazzák (lásd "Veclam 125 mg / 5 ml granulátum belsőleges szuszpenzióhoz" és "Veclam 250 mg / 5 ml granulátum belsőleges szuszpenzióhoz") ").
12 és 18 év közötti gyermekeknél az adagolás ugyanaz, mint a felnőtteknél.
04.3 Ellenjavallatok
Túlérzékenység a makrolid osztályú antibiotikumokkal vagy a 6.1 pontban felsorolt bármely segédanyaggal szemben.
- A klaritromicin egyidejű alkalmazása az alábbi gyógyszerek bármelyikével: asztemizol, ciszaprid, pimozid és terfenadin, mivel ezek QT -intervallum megnyúlást és szívritmuszavarokat okozhatnak, beleértve a kamrai tachycardiát, a kamrai fibrillációt és a torsades de pointes -t (lásd 4.5 pont).
- A klaritromicin egyidejű alkalmazása tikagrelorral vagy ranolazinnal.
- Klaritromicin és ergot alkaloidok (ergotamin vagy dihidroergotamin) egyidejű alkalmazása, mivel ez ergot -toxicitáshoz vezethet (lásd 4.5 pont).
- klaritromicin és midazolám egyidejű alkalmazása szájon át (lásd 4.5 pont).
A Veclam nem adható olyan betegeknek, akiknél a QT -intervallum megnyúlása vagy szívkamrai aritmiája volt, beleértve a torsades de pointes -t is (lásd 4.4 és 4.5 pont).
A Veclam nem adható együtt a HMG-CoA reduktáz inhibitorokkal (sztatinokkal), amelyeket a CYP3A4 (lovasztatin vagy szimvasztatin) nagymértékben metabolizál, a myopathia, beleértve a rabdomiolízist, fokozott kockázata miatt (lásd 4.5 pont).
A Veclam nem adható hypokalaemiás betegeknek (a QT -intervallum megnyúlásának veszélye).
A Veclam nem alkalmazható olyan betegeknél, akik vesekárosodással járó súlyos májelégtelenségben szenvednek.
A többi erős CYP3A4 enzim inhibitorhoz hasonlóan a klaritromicint sem szabad kolchicinnel együtt alkalmazni (lásd 4.4 és 4.5 pont).
Mivel az 500 mg-os napi adag nem csökkenthető, a Veclam módosított hatóanyag-leadású tabletta ellenjavallt azoknál a betegeknél, akiknél a kreatinin-clearance 30 ml / perc alatt van. Ehhez a betegcsoporthoz minden más gyógyszerforma alkalmazható.
04.4 Különleges figyelmeztetések és a használathoz szükséges óvintézkedések
Tabletták és tasakok
Bármilyen antibiotikum terápia, például klaritromicin alkalmazása fertőzés kezelésére H.pylori rezisztens baktériumok megjelenését okozhatja.
Minden készítmény
A klaritromicint nem szabad terhes nőknek felírni „gondos előny / kockázat értékelés” nélkül, különösen a terhesség első trimeszterében (lásd 4.6 pont).
A többi antibiotikumhoz hasonlóan a klaritromicin tartós alkalmazása is okozhat rezisztens baktériumokkal és gombákkal szembeni szuperfertőzést, ami a kezelés megszakítását és megfelelő terápiák alkalmazását igényli.
Óvatosan kell eljárni azoknál a betegeknél, akik súlyos veseelégtelenségben szenvednek (lásd 4.2 pont).
A klaritromicin alkalmazása során májműködési zavarról (lásd 4.8 pont) beszámoltak, beleértve a májenzimszint emelkedését, hepatocelluláris károsodást és / vagy kolesztatikus hepatitist sárgasággal vagy anélkül. Ez a májműködési zavar súlyos lehet, és általában visszafordítható. halálos kimenetelű májelégtelenség, és általában súlyos alapbetegséggel vagy egyidejű kezeléssel jártak együtt.
A beteget tanácsolni kell, hogy hagyja abba a kezelést, és forduljon orvosához, ha májbetegség jelei és tünetei, például étvágytalanság, sárgaság, sötét vizelet, viszketés vagy hasi fájdalom jelentkeznek.
Pseudomembranosus colitis eseteiről számoltak be szinte minden antibakteriális szer alkalmazásával, beleértve a makrolidokat is, amelyek súlyossága mérsékeltől életveszélyesig terjed. Clostridium difficile hasmenés (CDAD) eseteiről számoltak be. amely a mérsékelt hasmenéstől a végzetes vastagbélgyulladásig terjedhet. Az antibakteriális szerekkel végzett kezelés megváltoztatja a normális bélflórát, ami a túlzott burjánzáshoz vezethet C. nehéz. Minden olyan betegnél, aki hasmenésre panaszkodik az antibiotikumok bevétele után, értékelni kell a CDAD (Clostridium difficile diarrhoea) jelenlétét. Ezeknek a betegeknek gondos kórtörténeten kell részt venniük, mivel beszámoltak arról, hogy az antibakteriális szerek bevételét követő két hónapban CDAD előfordulhat. Ezért a klaritromicin -kezelést a terápiás indikációtól függetlenül meg kell szakítani, mikrobiális tesztet kell végezni, és meg kell kezdeni a megfelelő kezelést. Kerülni kell az antiperisztaltikus szerek alkalmazását.
Mivel a klaritromicin főként a májban metabolizálódik és választódik ki, különös óvatossággal kell eljárni, ha a gyógyszert károsodott májfunkciójú betegeknek, mérsékelt vagy súlyos vesekárosodásban szenvedő betegeknek és időseknek (65 év felett) adják.
Kolchicin:
A forgalomba hozatalt követően a kolchicin és a klaritromicin egyidejű alkalmazása során kolhicintoxicitást jelentettek, különösen idős betegeknél, amelyek közül néhány veseelégtelenségben szenvedő betegeknél fordult elő. Ezen betegek egy részéről halálesetekről számoltak be (lásd 4.5 pont). ellenjavallt (lásd 4.3 pont).
Óvatosság szükséges a klaritromicin és a triazolobenzodiazepinek, például a triazolam és az injekciós midazolám egyidejű alkalmazásakor (lásd 4.5 pont).
Óvatosság szükséges a klaritromicin és más ototoxikus gyógyszerek, különösen az aminoglikozidok egyidejű alkalmazásakor. Ezért tanácsos rendszeresen ellenőrizni a vestibularis és hallási funkciót a kezelés alatt és után.
A QT -intervallum megnyúlásának veszélye miatt a klaritromicint óvatosan kell alkalmazni koszorúér -betegségben, súlyos szívelégtelenségben, hipomagnesémiában, bradycardiában (korábbi kamrai aritmia) szenvedő betegeknél.
Tüdőgyulladás:
Várva a feltörekvő ellenállást a Streptococcus pneumoniae makrolidokkal szemben fontos, hogy érzékenységi tesztet végezzen, mielőtt klaritromicint írnak fel a közösségben szerzett tüdőgyulladás kezelésére. Kórházban szerzett tüdőgyulladásban a klaritromicint megfelelő további antibiotikumokkal együtt kell beadni.
Enyhe vagy közepes intenzitású bőr- és lágyrészfertőzések:
Ezeket a fertőzéseket leggyakrabban az okozza Staphylococcus aureus És Streptococcus pyogenesMindkettő ellenállhat a makrolidoknak. Ezután érzékenységi tesztet kell végezni. Azokban az esetekben, amikor a béta-laktám antibiotikumok nem alkalmazhatók (pl. Allergia), előnyösebb más antibiotikumokat, például klindamicint használni. A makrolidok jelenleg csak a bőr- és lágyrészfertőzésekben játszanak alapvető szerepet, például a Corynebacterium minutissimum, az acne vulgaris, az erysipelas által okozott fertőzésekben és azokban a helyzetekben, amikor a penicillin-alapú terápia nem hozható létre.
Súlyos akut túlérzékenységi reakciók, például anafilaxia, Stevens-Johnson-szindróma, toxikus epidermális nekrolízis és DRESS-szindróma esetén a klaritromicin-kezelést azonnal abba kell hagyni, és a megfelelő kezelést azonnal el kell kezdeni.
A Veclam -ot óvatosan kell alkalmazni, ha olyan gyógyszerekkel együtt adják, amelyek képesek a CYP3A4 enzim indukálására (lásd 4.5 pont).
Figyelmet kell fordítani a klaritromicin és más makrolidok, linkomicin és klindamicin közötti keresztrezisztencia lehetőségére.
HMG-CoA reduktáz inhibitorok (sztatinok): A klaritromicin és a lovasztatin vagy a szimvasztatin egyidejű alkalmazása ellenjavallt (lásd 4.3 pont). Óvatosan kell eljárni a klaritromicin más sztatinokkal történő felírásakor. A klaritromicint és sztatinokat szedő betegeknél rabdomiolízist jelentettek. A betegeket monitorozni kell a myopathia jelei és tünetei tekintetében.
Azokban a helyzetekben, amikor a klaritromicin és a sztatinok egyidejű alkalmazása nem kerülhető el, ajánlott a statinok legalacsonyabb regisztrált adagját előírni.
Megfontolható lehet egy olyan sztatin alkalmazása, amely nem függ a CYP3A enzim metabolizmusától (pl. Fluvasztatin) (lásd 4.5 pont).
Orális hipoglikémiás szerek / inzulin:
A klaritromicin és az orális hipoglikémiás szerek (például szulfonil -karbamidok) és / vagy az inzulin egyidejű alkalmazása súlyos hypoglykaemiához vezethet.
Orális antikoagulánsok:
C "a súlyos vérzés kockázata, valamint a nemzetközi normalizált arány (INR) és a protrombin idő jelentős növekedése, ha klaritromicint adnak együtt warfarinnal (lásd 4.5 pont). akiket klaritromicinnel és orális antikoagulánsokkal egyidejűleg kezelnek.
Ismert hatású segédanyagok:
A Veclam granulátum belsőleges szuszpenzióhoz szacharózt tartalmaz. A ritka örökletes fruktóz intoleranciában, glükóz-galaktóz felszívódási zavarban vagy szacharáz-izomaltáz elégtelenségben szenvedő betegek nem szedhetik ezt a gyógyszert.
Amikor cukorbetegeknek rendelnek Veclam granulátumot belsőleges szuszpenzióhoz, figyelembe kell venni a szacharóztartalmat.
A Veclam granulátum belsőleges szuszpenzióhoz ricinusolajat is tartalmaz, ami gyomorpanaszokat és hasmenést okozhat.
A Veclam RM 500 mg módosított hatóanyag -leadású tabletta laktózt tartalmaz. Ritka örökletes galaktóz intoleranciában, Lapp laktáz hiányban, glükóz-galaktóz felszívódási zavarban szenvedő betegek nem szedhetik ezt a gyógyszert.
04.5 Kölcsönhatások más gyógyszerekkel és egyéb interakciók
A következő gyógyszerek alkalmazása abszolút ellenjavallt a gyógyszerkölcsönhatásukból adódó lehetséges súlyos hatások miatt.
Ciszaprid, pimozid, asztemizol és terfenadin
A ciszaprid szintjének emelkedését figyelték meg olyan betegeknél, akik egyidejűleg szedtek ciszapridot és klaritromicint. Az egyidejű alkalmazás meghosszabbította a QT -intervallumot, szívritmuszavarokat, beleértve a kamrai tachycardiát, a kamrai fibrillációt és a torsades de pointes -t. Hasonló hatásokat figyeltek meg klaritromicint és pimozidot egyidejűleg szedő betegeknél is (lásd 4.3 pont).
A szakirodalomban arról számoltak be, hogy a makrolidok megváltoztatják a terfenadin metabolizmusát azáltal, hogy növelik annak szintjét, amely esetenként szívritmuszavarokkal jár, mint például a QT megnyúlása, a kamrai tachycardia, a kamrai fibrilláció és a torsades de pointes (lásd 4.3 pont). Egy 14 egészséges önkéntesen végzett vizsgálatban a klaritromicin és a terfenadin egyidejű alkalmazása a terfenadin savas metabolitjának szérumszintjének kétszeres-háromszoros növekedését és a QT-intervallum meghosszabbodását eredményezte, ami nem vezetett kimutatható klinikai hatáshoz Hasonló hatásokat észleltek az astemizol és más makrolidok egyidejű alkalmazásakor.
Ergot alkaloidjai
Néhány forgalomba hozatalt követő jelentés azt jelzi, hogy a klaritromicin és az ergotamin vagy a dihidroergotamin együttes alkalmazása akut ergottoxicitással (ergotizmussal) jár együtt, amelyet vasospasmus és a végtagok és más szövetek, köztük a központi idegrendszer ischaemiája jellemez. A klaritromicin és az ergot alkaloidok egyidejű alkalmazása ellenjavallt (lásd 4.3 pont).
HMG-CoA reduktáz inhibitorok (sztatinok)
A klaritromicin és a lovasztatin vagy a szimvasztatin egyidejű alkalmazása ellenjavallt (lásd 4.3 pont), mivel ezeket a sztatinokat nagymértékben metabolizálja a CYP3A4, és a klaritromicinnel történő egyidejű kezelés növeli plazmakoncentrációjukat, ami növeli a myopathia, beleértve a rabdomiolízist, kockázatát.
Beszámoltak rabdomiolízisről azoknál a betegeknél, akik klaritromicint szedtek egyidejűleg ezekkel a sztatinokkal. Ha a klaritromicin -kezelést nem lehet elkerülni, a lovasztatin- vagy szimvasztatin -kezelést a kezelés ideje alatt fel kell függeszteni.
Óvatosan kell eljárni, amikor a klaritromicint sztatinokkal együtt írják fel. Azokban a helyzetekben, amikor a klaritromicin és a sztatinok egyidejű alkalmazását nem lehet elkerülni, ajánlott a statinok legalacsonyabb regisztrált dózisát előírni A sztatin alkalmazásának lehetősége, amely nem függ a CYP3A metabolizmusától (pl. Fluvasztatin). A betegeket figyelni kell a myopathia jeleire és tüneteire.
Más gyógyszerek hatása a klaritromicinre
A CYP3A -t indukáló gyógyszerek (pl. Rifampicin, fenitoin, karbamazepin, fenobarbitál, orbáncfű) kiválthatják a klaritromicin metabolizmusát. Ez a klaritromicin szubterápiás szintjeihez vezet, csökkent terápiás hatékonysággal.
Ezenkívül szükségessé válhat a CYP3A -induktor plazmakoncentrációjának ellenőrzése, amely a klaritromicin CYP3A gátlása miatt növekedhet (lásd még a beadott CYP3A -inhibitor betegtájékoztatóját). A rifabutin és a klaritromicin egyidejű alkalmazása megnövekedett a rifabutin szérumszintjében a klaritromicin szérumszintjének csökkenése, ami az uveitis kockázatának növekedésével jár.
A következő gyógyszerekről ismert vagy gyaníthatóan befolyásolják a keringő klaritromicin -koncentrációt; Szükség lehet a klaritromicin adagjának módosítására, vagy mérlegelni kell az alternatív terápiák alkalmazásának lehetőségét.
Efavirenz, nevirapin, rifampin, rifabutin és rifapentin
Azok a gyógyszerek, amelyekről kimutatták, hogy erősen indukálják a citokróm P450 metabolizmusát, mint például az efavirenz, a nevirapin, a rifampicin, a rifabutin és a rifapentin, felgyorsíthatják a klaritromicin metabolizmusát, következésképpen csökkenthetik a klaritromicin plazmaszintjét, miközben növelhetik a 14-OH-klaritromicin plazmaszintjét. metabolit, amely mikrobiológiai szempontból is aktív.
Etravirin
Az etravirin csökkentette a klaritromicin -expozíciót; azonban az aktív metabolit, a 14-OH-klaritromicin koncentrációja megnőtt. Mivel a 14-OH-klaritromicin csökkentette az aktivitást a Mycobacterium Avium komplex (MAC), a kórokozóval szembeni általános aktivitás megváltozhat, ezért a MAC kezelésében fontolóra kell venni a klaritromicin alternatíváit.
Flukonazol
A napi 200 mg flukonazol és a napi kétszeri 500 mg klaritromicin 21 egészséges önkéntes egyidejű alkalmazása 33% -kal, illetve 18% -kal növelte a klaritromicin átlagos minimális koncentrációját (Cmin) és a görbe alatti területet (AUC). Az aktív metabolit, a 14-OH-klaritromicin nem befolyásolta szignifikánsan a flukonazol egyidejű alkalmazása.
Ritonavir
Egy farmakokinetikai vizsgálat kimutatta, hogy 200 mg ritonavir 8 óránként és 500 mg klaritromicin 12 óránként történő együttes alkalmazása a klaritromicin metabolizmusának jelentős gátlásához vezet. A ritonavir egyidejű alkalmazásakor a klaritromicin Cmax 31% -os, a Cmin 182% -os és az AUC 77% -os növekedését figyelték meg. A 14-OH-klaritromicin képződés teljes gátlását figyelték meg. A klaritromicin nagy terápiás ablaka miatt normál vesefunkciójú betegeknél nincs szükség dóziscsökkentésre. Veseelégtelenségben szenvedő és ritonavirrel egyidejűleg kezelt betegeknél azonban a következő dózismódosításra kell gondolni: ha a kreatinin clearance (CLCR) 30 és 60 ml / perc között van, a klaritromicin adagját 50%-kal kell csökkenteni; olyan betegeknél, akiknél a CLCR
Hasonló dózismódosításokat kell fontolóra venni azoknál a betegeknél, akiknek károsodott a veseműködése, és ritonavirt adnak más HIV proteáz inhibitorok, köztük az atazanavir és a sakvinavir farmakokinetikai fokozójának (lásd alább Kétirányú gyógyszerkölcsönhatások).
A klaritromicin hatása más gyógyszerekre
CYP3A -alapú kölcsönhatások
A klaritromicin, amelyről ismert, hogy gátolja a CYP3A -t, és egy elsősorban CYP3A által metabolizált gyógyszer egyidejű alkalmazása a gyógyszerkoncentráció növekedésével járhat, ami fokozhatja vagy meghosszabbíthatja az egyidejűleg alkalmazott gyógyszer terápiás és káros hatásait.
A klaritromicint óvatosan kell alkalmazni azoknál a betegeknél, akik olyan gyógyszereket kapnak, amelyekről úgy gondolják, hogy a CYP3A enzim szubsztrátjai, különösen akkor, ha a CYP3A szubsztrátnak szűk a biztonsági határa (pl. Karbamazepin), és / vagy ha ez a szubsztrát nagymértékben metabolizálódik enzim.
Az egyidejű klaritromicin -kezelésben részesülő betegeknél mérlegelni kell az adagolás módosítását, és lehetőség szerint gondosan ellenőrizni kell az elsősorban CYP3A által metabolizált gyógyszerek szérumkoncentrációját.
Azok a gyógyszerek vagy gyógyszerosztályok, amelyeket ismert vagy feltételezett módon ugyanaz a CYP3A izoenzim metabolizál: , omeprazol, pimozid, kinidin, rifabutin, szildenafil, szimvasztatin, szirolimusz, takrolimusz, terfenadin, triazolam és vinblasztin, de ez a lista nem teljes. A citokróm P450 rendszeren belül más izoenzimeken keresztül hasonló mechanizmussal kölcsönhatásba lépő egyéb gyógyszerek a fenitoin, a teofillin és a valproát.
Antiaritmiás szerek
A forgalomba hozatalt követően torsade de pointes eseteket jelentettek klaritromicin és kinidin vagy disopiramid egyidejű alkalmazása után. Ezen gyógyszerek klaritromicinnel történő egyidejű alkalmazása során ellenőrizni kell az elektrokardiográfiás nyomokat, hogy kimutassák a QT-intervallum megnyúlásának jelenlétét. a kinidin és a disopiramid koncentrációja a klaritromicin terápia során.
A forgalomba hozatalt követően hipoglikémiáról számoltak be klaritromicin és disopiramid egyidejű alkalmazása után. Ezért a klaritromicin és a disopiramid egyidejű alkalmazása során ellenőrizni kell a vércukorszintet.
Orális hipoglikémiás szerek / inzulin
Abban az esetben, ha a klaritromicint bizonyos hipoglikémiás gyógyszerekkel, például nategliniddel és repagliniddel egyidejűleg alkalmazzák, előfordulhat, hogy a CYP3A enzim klaritromicin gátolja, és hipoglikémiát okozhat. Javasolt a glükózszint szoros monitorozása.
Omeprazol
Egészséges felnőtt alanyok klaritromicint (500 mg 8 óránként) kaptak omeprazollal (napi 40 milligramm) kombinációban. Az omeprazol kiindulási plazmakoncentrációja megnőtt (Cmax, AUC0-24 és T½ 30%, 89%és 34%) a klaritromicin egyidejű alkalmazásához.
A gyomor átlagos pH -értéke 24 óra alatt 5,2 volt, ha az omeprazolt önmagában adták, és 5,7 volt, amikor az omeprazolt klaritromicinnel együtt adták.
Szildenafil, tadalafil és vardenafil
Ezen foszfodiészteráz inhibitorok mindegyike metabolizálódik, legalább részben, a CYP3A által, és a CYP3A gátolható a klaritromicin egyidejű alkalmazásával. A klaritromicin és a szildenafil, tadalafil vagy vardenafil egyidejű alkalmazása nagy valószínűséggel fokozza a foszfodiészteráz -gátló expozícióját. Ezért fontolóra kell venni a szildenafil, a tadalafil és a vardenafil adagjának csökkentését, ha ezeket a gyógyszereket klaritromicinnel együtt adják.
Teofillin, karbamazepin
A klinikai vizsgálatok eredményei azt mutatták, hogy a karbamazepin és a teofillin plazmaszintje szerény, de statisztikailag szignifikáns (p≤0,05) növekedést mutathat, ha ezeket klaritromicinnel együtt alkalmazzák. Szükség lehet az adag csökkentésére.
Tolterodina
A tolterodin fő metabolikus útja a citokróm P450 (CYP2D6) 2D6 izoformáján halad át. Azonban egy CYP2D6 nélküli populáció alcsoportban az azonosított metabolikus útvonal a CYP3A. Ebben a populáció alcsoportban a CYP3A gátlás. Szignifikánsan magasabb szérum tolterodin koncentrációt eredményez . CYP3A inhibitorok jelenlétében szükség lehet a tolterodin dózisának csökkentésére, valamint a klaritromicin dózisának csökkentésére azon betegek körében, akiknél a CYP2D6 gyengén metabolizálódik.
Triazolobenzodiazepinek (pl. Alprazolam, midazolám, triazolam)
Amikor a midazolámot klaritromicin tablettákkal (500 mg naponta kétszer) együtt adták, a midazolám AUC-értéke 2,7-szeresére emelkedett az intravénás midazolám beadását követően, és 7-szeresére az intravénás midazolám beadását követően. Orális midazolám beadása. Abban az esetben, ha intravénás midazolámra van szükség klaritromicinnel egyidejűleg, a beteget gondosan ellenőrizni kell az adag módosítására. Ugyanezeket az óvintézkedéseket kell tenni más, a CYP3A által metabolizálódó benzodiazepinek, köztük a triazolam és az alprazolam jelenlétében is. Azon benzodiazepinek esetében, amelyek eliminációja nem függ a CYP3A -tól (temazepám, nitrazepám, lorazepám), a klaritromicinnel való klinikailag fontos kölcsönhatás nem valószínű.
A klaritromicin és a triazolam együttes alkalmazása során a forgalomba hozatalt követően beszámoltak gyógyszerkölcsönhatásokról és központi idegrendszeri (CNS) hatásokról (pl. Aluszékonyság és zavartság). Célszerű monitorozni a beteget, hogy kordában tartsa az esetleges farmakológiai hatásokat, amelyeket ez meghatározhat a központi idegrendszerre.
Egyéb gyógyszerkölcsönhatások
Aminoglikozidok
Óvatosan kell eljárni a klaritromicin más ototoxikus gyógyszerekkel, különösen aminoglikozidokkal történő egyidejű alkalmazásakor (lásd 4.4 pont).
Kolchicin
A kolchicin mind a CYP3A, mind a kiáramló transzporter, a P-glikoprotein (Pgp) szubsztrátja. A klaritromicinről és más makrolidokról ismert, hogy gátolják a CYP3A-t és a Pgp-t. A klaritromicin és a kolhicin egyidejű alkalmazásakor a CYP3A és / vagy a Pgp gátlása klaritromicinnel fokozott kolhicin -expozícióhoz vezethet. Figyelje a betegeket a kolhicin toxicitás klinikai tünetei tekintetében (lásd 4.4 pont).
Digoxin
Úgy gondolják, hogy a digoxin a kiáramló transzporter, a P-glikoprotein (Pgp) szubsztrátja. A klaritromicinről ismert, hogy gátolja a Pgp-t. A digoxin és a klaritromicin egyidejű alkalmazásakor a Pgp gátlása A klaritromicin egy része fokozott digoxin-expozícióhoz vezethet. plazma digoxin-koncentrációról is beszámoltak a forgalomba hozatalt követő felügyelet során azoknál a betegeknél, akik egyidejűleg digoxint és klaritromicint kaptak. A digoxin plazmakoncentrációját gondosan ellenőrizni kell, amíg a betegek egyidejű digoxin- és klaritromicin -kezelést kapnak.
Zidovudin
A klaritromicin tabletták és a zidovudin egyidejű alkalmazása HIV -fertőzött felnőtt betegeknél a zidovudin egyensúlyi állapotának csökkenését eredményezheti. Mivel a klaritromicin látszólag zavarja az egyidejűleg szájon át adott zidovudin felszívódását, ez a kölcsönhatás erősen elkerülhető, ha a klaritromicin és a zidovudin adagjait legalább 4 órás időközönként eltorzítják. fertőzések, ha a klaritromicint granulált formában a zidovudinnal vagy didanozinnal egyidejűleg veszik be. Ez a kölcsönhatás nem valószínű, ha klaritromicint intravénásan adnak be.
Fenitoin és valproát:
Spontán vagy publikált jelentések érkeztek arról, hogy a CYP3A -gátlók, köztük a klaritromicin kölcsönhatásba lépnek olyan gyógyszerekkel, amelyeket nem tekintünk a CYP3A által metabolizálhatónak (pl. Fenitoin és valproát). Ezeknek a gyógyszereknek a szérumszint meghatározása javasolt, ha klaritromicinnel együtt alkalmazzák. A szérum emelkedett szintjeiről számoltak be.
Kétirányú gyógyszerkölcsönhatások
Atazanavir
A klaritromicin és az atazanavir mind a CYP3A szubsztrátjai, mind gátlói, és bizonyíték van a kétirányú gyógyszerkölcsönhatásra ezen gyógyszerek között. A klaritromicin (500 mg naponta kétszer) és az atazanavir (napi egyszer 400 mg) egyidejű alkalmazása kétszeresére növelte az expozíciót klaritromicinre, és a 14-OH-klaritromicin expozíciójának 70% -os csökkenése, az atazanavir AUC-jának 28% -os növekedésével. A klaritromicin nagy terápiás ablaka miatt normál vesefunkciójú betegeknél nincs szükség dóziscsökkentésre. Mérsékelt veseelégtelenségben (30-60 ml / perc kreatinin -clearance) szenvedő betegeknél a klaritromicin dózisát 50%-kal kell csökkenteni. A kreatinin kevesebb, mint 30 ml / perc, a klaritromicin adagját csökkenteni kell 75%, megfelelő klaritromicin készítmény alkalmazásával. A klaritromicin napi 1000 mg -nál nagyobb dózisának alkalmazása proteázgátlókkal együtt nem ajánlott.
Kalciumcsatorna -blokkolók
Óvatosság szükséges a klaritromicin és a CYP3A4 által metabolizált kalciumcsatorna -blokkolók (pl. Verapamil, amlodipin, diltiazem) egyidejű alkalmazásakor a hipotenzió veszélye miatt. A klaritromicin, valamint a kalciumcsatorna -blokkolók plazmakoncentrációja az interakció miatt megnőhet.Klaritromicint és verapamilt egyidejűleg szedő betegeknél hipotenziót, bradiaritmiát és tejsavas acidózist figyeltek meg.
Itrakonazol
A klaritromicin és az itrakonazol mind a CYP3A szubsztrátjai, mind gátlói, ami kétirányú gyógyszerkölcsönhatást eredményez ezen gyógyszerek között. A klaritromicin növelheti az itrakonazol plazmaszintjét, míg az itrakonazol növelheti a klaritromicin plazmaszintjét.A klaritromicint és az itrakonazolt egyidejűleg szedő betegeket gondosan ellenőrizni kell, hogy nincsenek -e jelek és tünetek, amelyek fokozzák és meghosszabbítják ezen gyógyszerek farmakológiai hatásait.
Saquinavir
A klaritromicin és a szakinavir mind a CYP3A szubsztrátjai, mind gátlói, ami "kétirányú gyógyszerkölcsönhatást eredményez ezen gyógyszerek között. Klaritromicin (500 mg naponta kétszer) és szakinavir (lágyzselatin kapszula, napi háromszor 1200 mg) egyidejű alkalmazása 12 egészséges önkéntesben A szakinavir AUC és Cmax értékei 177% -kal és 187% -kal magasabbak voltak, mint a szakinavir monoterápia esetén A klaritromicin AUC és Cmax értékei körülbelül 40% -kal voltak magasabbak, mint a klaritromicin monoterápia alkalmazásakor. Nincs szükség dózismódosításra, ha a két gyógyszert egyidejűleg, korlátozott ideig adják a vizsgált dózisokban / készítményekben. A lágy zselatin kapszula készítmény alkalmazásával végzett gyógyszerkölcsönhatási vizsgálatok megfigyelései nem reprezentatívak a szakinavir keményzselatin kapszula készítmény alkalmazásával tapasztalt hatásokra. A kizárólag szakvinavirral végzett gyógyszerkölcsönhatási vizsgálatokból származó megfigyelések nem reprezentálják a szakinavir / ritonavir kombinációs terápia hatását. Ha a szakinavirt ritonavirrel egyidejűleg adják, alaposan mérlegelni kell a ritonavir klaritromicinre gyakorolt lehetséges hatásait.
04.6 Terhesség és szoptatás
Terhesség
A klaritromicin terhes nőknél történő alkalmazásának biztonságosságát nem értékelték. Az egereken, patkányokon, nyulakon és majmokon végzett vizsgálatok eredményei alapján nem zárható ki az embrionális-magzati fejlődésre gyakorolt káros hatások lehetősége. Következésképpen a terhesség alatt történő alkalmazás nem ajánlott gondos kockázat / haszon értékelés nélkül.
Etetési idő
A klaritromicin szoptatás alatti alkalmazásának biztonságosságát nem értékelték. A klaritromicin kiválasztódik az anyatejbe.
04.7 Hatások a gépjárművezetéshez és gépek kezeléséhez szükséges képességekre
Nincsenek adatok a klaritromicin gépjárművezetéshez és gépek kezeléséhez szükséges képességekre gyakorolt hatásáról. Mielőtt a beteg gépjárművet vezetne vagy gépeket kezelne, mérlegelni kell a szédülés, szédülés, zavartság és zavartság kockázatát, amely az alkalmazás után előfordulhat.
04.8 Nemkívánatos hatások
nak nek. A biztonsági profil összefoglalása
A klaritromicin -terápiával kapcsolatos leggyakoribb és leggyakoribb mellékhatások mind felnőtt, mind gyermekgyógyászati betegeknél a hasi fájdalom, hasmenés, hányinger, hányás és ízérzés. Ezek a mellékhatások általában közepes intenzitásúak, és összhangban vannak a makrolid antibiotikumok ismert biztonsági profiljával (lásd a 4.8 pont b szakaszát).
A klinikai vizsgálatok során nincsenek szignifikáns különbségek ezen gasztrointesztinális mellékhatások előfordulási gyakoriságában a már meglévő mycobacterium fertőzésben szenvedő betegek vagy azok nélkül.
b. A mellékhatások összefoglaló táblázata
Az alábbi táblázat a klaritromicin azonnali hatóanyag-leadású tablettákkal, granulátumokkal, belsőleges szuszpenzióhoz, porral és oldószer oldatos infúzióval, valamint módosított hatóanyag-leadású tablettákkal kapcsolatos klinikai vizsgálatok során és forgalomba hozatalt követően jelentett mellékhatásokat foglalja össze.
A klaritromicinnel kapcsolatban állónak ítélt mellékhatásokat szervtípus és gyakoriság szerint jelentik a következő megállapodás szerint: nagyon gyakori (≥1 / 10), gyakori (≥1 / 100,
* Mivel ezeket a reakciókat önként jelentették egy határozatlan méretű populációból, nem mindig lehetséges a gyakoriság valódi becslése, vagy ok-okozati összefüggés megállapítása a gyógyszer expozíciójával. kezelés klaritromicinnel
** A bejelentett rabdomiolízis esetek egy részében a klaritromicint sztatinokkal, fibrátokkal, kolhicinnel vagy allopurinollal egyidejűleg alkalmazták.
1 Mellékhatás, amelyet csak az infúziós oldathoz készült por és oldószer készítmény esetében jelentettek
2 Mellékhatást csak az orális szuszpenzió granulátumánál jelentettek
3 A mellékhatásokról csak az azonnali hatóanyag -leadású tabletták esetében számoltak be
4, 6, 8,9 Lásd a) pont
5, 7, 10 Lásd c) pont
c. A kiválasztott mellékhatások leírása
Az injekció beadásának helyén fellépő phlebitis, az injekció beadásának helyén jelentkező fájdalom, tűszúrásos fájdalom és az injekció beadásának helyén fellépő gyulladás az intravénás készítményre jellemző.
A jelentett rabdomiolízis esetek egy részében a klaritromicint sztatinokkal, fibrátokkal, kolhicinnel vagy allopurinollal együtt adták (lásd 4.3 és 4.4 pont).
A forgalomba hozatalt követően beszámoltak a klaritromicin és a triazolam egyidejű alkalmazása során fellépő gyógyszerkölcsönhatásokról és központi idegrendszeri (CNS) hatásokról (pl. Aluszékonyság és zavartság). Javasolt, hogy a beteget fokozott farmakológiai hatásokra figyeljék központi idegrendszeri szinten (lásd 4.5. szakasz).
Ritka esetekben jelentettek klaritromicin módosított hatóanyagleadású tablettákat a széklettel, amelyek többsége anatómiai elváltozásokban (beleértve az ileosztómiát vagy kolosztómiát) vagy gyomor -bélrendszeri rendellenességekben szenvedő betegeknél fordult elő, akiknek csökkent a gasztrointesztinális áthaladási ideje. Számos esetben tablettamaradványok fordultak elő hasmenés kapcsán. Azoknál a betegeknél, akik tapasztalták, hogy tabletták maradványai vannak a székletben, és állapotuk nem javul, javasoljuk a klaritromicin (pl. Belsőleges szuszpenzió) vagy más antibiotikum más összetételének megváltoztatását.
Különleges populáció: Mellékhatások immunhiányos betegeknél (lásd e pont).
d. Gyermekpopulációk
Klinikai vizsgálatokat végeztek a klaritromicin-alapú gyermek szuszpenzió 6 hónapos és 12 éves kor közötti gyermekeknek történő beadásával. Következésképpen a 12 év alatti gyermekeknek fel kell venniük a gyermek szuszpenziót. Nem áll rendelkezésre elegendő adat ahhoz, hogy a klaritromicin IV adagolási rendjét 12 évesnél fiatalabb betegeknél alkalmazzák.
A mellékhatások gyakorisága, típusa és súlyossága várhatóan hasonló lesz a felnőtteknél tapasztaltakhoz.
És. Egyéb speciális populációk
Immunhiányos betegek
AIDS vagy immunhiányos betegeknél, akiket mycobacterium fertőzések miatt hosszú ideig nagy dózisú klaritromicinnel kezeltek, gyakran nehéz volt megkülönböztetni a klaritromicin alkalmazásával esetlegesen összefüggő mellékhatásokat a humán immunhiányos vírustól (HIV) vagy az egyidejű betegségekhez kapcsolódó megnyilvánulásoktól.
Felnőtt betegeknél a leggyakrabban jelentett mellékhatások az 1000 mg és 2000 mg klaritromicin napi dózisokkal kezelt betegeknél a következők voltak: hányinger, hányás, ízérzékenység, hasi fájdalom, hasmenés, kiütés, puffadás, fejfájás, székrekedés, halláskárosodás, fokozott szérum Glutamic-Oxaloacetic Transaminase (SGOT) és szérum Glutamic-Pyruvic Transaminase (SGPT). További ritkább reakciók közé tartozik a dyspnoe, az álmatlanság és a szájszárazság. Az incidencia összehasonlítható volt azoknál a betegeknél, akik 1000 mg-os és 2000 mg-os kezelésben részesültek, de általában 3 4 -szer gyakoribb azoknál a betegeknél, akik 4000 mg klaritromicin napi teljes adagot kapnak.
Ezeknél az immunhiányos betegeknél a laboratóriumi értékeket úgy értékelték ki, hogy elemezték azokat az értékeket, amelyek kívül estek az adott vizsgálat szempontjából komolynak ítélt kóros szinteken (pl. Felső és alsó határértékek). Ezen kritériumok alapján a napi 1000 mg vagy 2000 mg klaritromicint szedő betegek körülbelül 2% -ának vagy 3% -ának rendkívül magas volt az abnormális SGOT- és SGPT -értéke, valamint rendkívül alacsony a fehérvérsejtek és a vérlemezkék száma. A két dóziscsoportba tartozó betegek alacsonyabb százaléka is emelkedett BUN értékeket mutatott. A rendellenes értékek valamivel gyakoribb előfordulását figyelték meg azoknál a betegeknél, akiket napi 4000 mg klaritromicinnel kezeltek minden paraméter esetében, kivéve a leukocita képletet.
A feltételezett mellékhatások bejelentése.
A gyógyszer engedélyezése után jelentkező feltételezett mellékhatások bejelentése fontos, mivel lehetővé teszi a gyógyszer előny / kockázat arányának folyamatos nyomon követését. Az egészségügyi szakembereket kérjük, hogy jelentsék be a feltételezett mellékhatásokat a nemzeti jelentési rendszeren keresztül. "Address https: //www.aifa.gov.it/content/segnalazioni-reazioni-avverse.
04.9 Túladagolás
Nagy klaritromicin dózisok esetén gyomor -bélrendszeri zavarok léphetnek fel. Egy bipoláris zavarban szenvedő beteg nyolc gramm klaritromicint fogyasztott, ami megváltozott mentális állapotot, paranoiás viselkedést, hypokalaemiát és hypoxémiát mutat. A túladagolás esetén fellépő mellékhatásokat a felszívódott gyógyszer azonnali megszüntetésével és megfelelő támogató terápiákkal kell kezelni.A többi makrolidhoz hasonlóan a klaritromicin szérumszintje sem szűnik meg hemodialízissel vagy peritoneális dialízissel.
Túladagolás esetén a klaritromicin IV (por és oldószer oldatos infúzióhoz) kezelést abba kell hagyni, és minden megfelelő támogató intézkedést meg kell kezdeni.
05.0 FARMAKOLÓGIAI TULAJDONSÁGOK
05.1 Farmakodinámiás tulajdonságok
Farmakoterápiás csoport: általános antibakteriális szerek szisztémás használatra - makrolidok.
ATC kód: J01FA09.
A klaritromicin egy új, Abbott által kifejlesztett makrolid, amely a hidroxilcsoport eritromicin laktongyűrűjének 6. pozíciójában a CH3O csoporttal történő helyettesítésből származik.
Az új makrolidról kimutatták, hogy in vitro antibakteriális spektrummal rendelkezik, amely a legismertebb és klinikailag legfontosabb Gram -pozitív és Gram -negatív baktériumok ellen is aktív, beleértve az aerobokat és az anaerobokat.
A klaritromicin in vitro antibakteriális spektrumát a következőképpen állapították meg: Streptococcus agalactiae, Streptococcus pyogenes, Streptococcus viridans, Streptococcus pneumoniae, Haemophilus influenzae, Haemophilus parainfluenzae, Neisseria gonorrheaopleae, Listeria monogaraluseriae Staphilococco aureus, Propionibacterium acnes, Mycobacterium avium, Mycobacterium leprae, Mycobacterium intracellulare, Mycobacterium chelonae, Mycobacterium fortuitum és Mycobacterium kansasii.
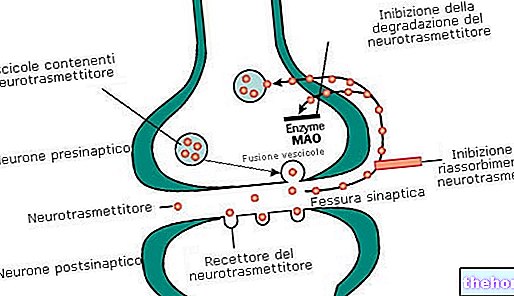
Hatása az 50S riboszómális alegységhez való kötődéssel történik, gátolja a baktériumsejt fehérjeszintézisét.
TÖRVÉNYEK
Az Európai Antimikrobiális Érzékenységi Tesztek Bizottsága (EUCAST) a következő határértékeket állapította meg a klaritromicinre vonatkozóan, elkülönítve a fogékony organizmusokat.
A klaritromicint a "felszámolására" használják.H. pylori: minimális gátló koncentráció (MIC) ≤ 0,25 mcg / ml, amelyet a Clinical and Laboratory Standards Institute (C.I.S.I) érzékenységi töréspontként állapított meg.
05.2 Farmakokinetikai tulajdonságok
Kutyákon végzett vizsgálatok kimutatták, hogy 10 mg / kg intravénás vagy orális adagolás után a plazma gyógyszerkoncentrációja 3, 2 vagy 1 mg / ml volt 1, 4 és 12 óra múlva.
A (14C) jelzésű klaritromicin orális vagy intravénás beadását követő 5 napon belül a 14C dózis körülbelül 35-36% -a nyerhető ki a vizeletben és körülbelül 52% -a a székletben.
A klaritromicin a májban metabolizálódik, és a legfontosabb metabolitja a 14-hidroxi-N-demetil-klaritromicin, amely 250 és 1200 mg beadása után 2-4 óra múlva éri el a plazma csúcskoncentrációját (0,5 mcg / ml és 1,2 mcg / ml). Csak 1200 mg szájon át történő bevétele után a deszladinosil-klaritromicin alacsony szintjét is azonosították a plazmában; az anyagcsere folyamat nagy dózisokban telítődésre hajlamos.
Az embereken végzett farmakokinetikai vizsgálatok 250 mg klaritromicin szájon át történő beadása után 2,08 μg / ml plazmakoncentrációt mutattak ki.
500 mg klaritromicin intravénás beadását követően az átlagos plazmacsúcsok 5,52 ± 0,98 mcg / ml értéket érnek el.
A vegyület felezési ideje 6,3 óra.
Ugyanazokat a metabolitokat azonosítják, amelyek szájon át történő beadás után keletkeznek, de alacsonyabb koncentrációban, feltehetően az első lépcsős máj metabolizmus hiánya miatt.
Módosított felszabadulású készítmény:
A szájon át alkalmazott módosított hatóanyag -leadású klaritromicin farmakokinetikáját felnőtt betegeknél vizsgálták, és összehasonlították a 250 mg és 500 mg azonnali hatóanyag -leadású klaritromicinnel. Ha egyenlő teljes napi dózist adtak be, a felszívódás mértéke egyenértékű volt. Az abszolút biohasznosulás körülbelül 50%.
Többszöri adagolást követően enyhe felhalmozódást észleltek, és az anyagcsere nem változott egyik fajnál sem.
Az egyenértékű felszívódási eredmények alapján a módosított hatóanyag -leadású készítmény alábbi adatai alkalmazhatók in vitro és in vivo.
In vitro
In vitro vizsgálatok kimutatták, hogy a klaritromicin fehérjéhez való kötődése átlagosan körülbelül 70%. 0,45 - 4,5 mcg / ml koncentrációban. A kötődés 41% -ra történő csökkenése 45 mcg / ml koncentrációban azt sugallja, hogy a kötődési helyek telítődhetnek, azonban ez csak a terápiás szintekhez képest magas gyógyszerkoncentrációk esetén következett be.
In vivo
A klaritromicin koncentrációja minden szövetben - a központi idegrendszert leszámítva - jóval magasabb volt, mint a keringő gyógyszer koncentrációja.
A legnagyobb koncentrációt a májban és a tüdőszövetben találták, ahol a szövet / plazma arány 10-20 volt.
A klaritromicin farmakokinetikai viselkedése nem lineáris. Azoknál a betegeknél, akik 500 mg / nap módosított hatóanyag-leadású klaritromicint ettek és kaptak, a klaritromicin és a 14-OH klaritromicin egyensúlyi plazma csúcskoncentrációja 1,3 mcg / ml, illetve 0,48 mcg / ml volt.Amikor az adagot napi 1000 mg-ra emelték, az egyensúlyi állapot koncentrációja 2,4 mcg / ml, illetve 0,67 mcg / ml volt.
A klaritromicint a májban citokróm P450 metabolizálja. Három metabolitot írtak le: N-demetil-klaritromicin; dekladinosil-klaritromicin és 14-hidroxi-klaritromicin.
A klaritromicin és aktív metabolitjának eliminációs felezési ideje 5,3, illetve 7,7 óra volt.
Magasabb koncentrációk esetén a klaritromicin és metabolitja látszólagos felezési ideje általában hosszabb.
A klaritromicin a vizelettel (kb. 40%) és a széklettel (kb. 30%) ürül.
05.3 A preklinikai biztonságossági adatok
Az LD50 egerekben és patkányokban szájon át nagyobb volt, mint 5 g / kg, kutyáknál és majmoknál pedig nagyobb, mint 300 mg / kg. A rövid távú toxicitás (1 hónap) nem mutatott toxikus hatást sem patkányokra (150 mg / kg / nap), sem kutyákra (10 mg / kg / nap). Továbbá a krónikus toxicitás (3 hónap) patkányokban 15 mg / kg / nap, kutyákban 10 mg / kg / nap volt.
A mutagén vizsgálatok azt mutatták, hogy a gyógyszernek nincs mutagén hatása vagy mikroszomális aktivációja. A klaritromicin nem volt hatással az egér motoros aktivitására 100 mg / kg orális adagolás után.
06.0 GYÓGYSZERÉSZETI INFORMÁCIÓK
06.1 Segédanyagok
Veclam 250 mg bevont tabletta:
Nátrium-kroszkarmellóz, zselatinizált keményítő, mikrokristályos cellulóz, E-104, szilikagél, povidon, sztearinsav, magnézium-sztearát, talkum, hipromellóz, propilénglikol, szorbitán-monoleát, vanillin, E-171, hidroxipropil-cellulóz, szorbinsav.
- Veclam 500 mg bevont tabletta:
Kroszkarmellóz -nátrium, mikrokristályos cellulóz, szilikagél, povidon, sztearinsav, magnézium -sztearát, talkum; bevonó oldat: hipromellóz, hidroxi-propil-cellulóz, propilénglikol, szorbitán-monoleát, E-171, szorbinsav, vanillin, E-104.
- Veclam 125 mg / 5 ml granulátum belsőleges szuszpenzióhoz és Veclam 250 mg / 5 ml granulátum belsőleges szuszpenzióhoz:
Carbopol 974, povidon, hipromellóz -ftalát, ricinusolaj, szilikagél, szacharóz, xantángumi, vegyes gyümölcsíz, kálium -szorbát, citromsav, titán -dioxid, maltodextrin, víz.
- Veclam 500 mg / 10 ml por és oldószer oldatos infúzióhoz:
Laktobionsav, nátrium -hidroxid, mint pH -beállító.
Minden oldószeres injekciós üveg tartalmaz:
Víz p.p.i.
- Veclam 250 mg granulátum belsőleges szuszpenzióhoz és Veclam 500 mg granulátum belsőleges szuszpenzióhoz:
Carbopol 974P, povidon K90, hidroxi -propil -metil -cellulóz -ftalát, ricinusolaj, szilícium -dioxid, maltodextrin, szacharóz, titán -dioxid, módosított keményítő, narancs aroma, glicirizált ammónium, aceszulfám K.
- Veclam RM 500 mg módosított hatóanyag -leadású tabletta:
Vízmentes citromsav, nátrium -alginát, nátrium- és kalcium -alginát, laktóz, povidon K30, talkum, sztearinsav, magnézium -sztearát, hipromellóz 6 cps, makrogol 400, makrogol 8000, titán -dioxid (E -171), szorbinsav, kinolinsárga (E - 104).
06.2 Inkompatibilitás
Jelenleg nincs specifikus összeférhetetlenség az ismert gyógyszerekkel.
06.3 Érvényességi idő
Veclam 250 mg bevont tabletta 3 év.
Veclam 500 mg bevont tabletta 3 év.
Veclam 125 mg / 5 ml granulátum belsőleges szuszpenzióhoz 2 év.
Veclam 250 mg / 5 ml granulátum belsőleges szuszpenzióhoz 2 év.
Veclam 250 mg granulátum belsőleges szuszpenzióhoz 3 év.
Veclam 500 mg granulátum belsőleges szuszpenzióhoz 3 év.
Veclam 500 mg / 5 ml por és oldószer oldatos infúzióhoz 3 év.
Veclam RM 500 mg módosított hatóanyag -leadású tabletta 3 év.
06.4 Különleges tárolási előírások
A csomagolás 500 mg granulátum belsőleges szuszpenzióhoz: Legfeljebb 25 ° C -on tárolandó.
Kiszerelés 250 mg bevont tabletta, 500 mg bevont tabletta, RM 500 módosított hatóanyagleadású tabletta, 250 mg granulátum belsőleges szuszpenzióhoz, 125 mg / 5 ml granulátum belsőleges szuszpenzióhoz és 250 mg / 5 ml granulátum belsőleges szuszpenzióhoz: Ez a gyógyszer nem igényel különleges tárolási körülményeket.
A csomagoláshoz 500 mg / 10 ml por és oldószer oldatos infúzióhoz: Nincs különleges tárolási előírás. Az elkészített készítményt 24 órán belül fel kell használni.
06.5 A közvetlen csomagolás jellege és a csomagolás tartalma
- Veclam 250 mg bevont tabletta:
Kartondoboz, 12 buborékcsomagot tartalmaz
- Veclam 500 mg bevont tabletta:
Kartondoboz, 14 cellás, átlátszatlan buborékfóliával
- Veclam RM 500 mg módosított hatóanyag -leadású tabletta:
Kartondoboz, 7 cellás buborékcsomagolással
- Veclam 125 mg / 5 ml granulátum belsőleges szuszpenzióhoz:
100 ml -es műanyag palack adagolóval
- Veclam 250 mg / 5 ml granulátum belsőleges szuszpenzióhoz:
100 ml -es műanyag palack adagolóval
- Veclam 500 mg / 10 ml por és oldószer oldatos infúzióhoz:
Kartondoboz, amely 1 ampulla 500 mg klaritromicint és 1 ampulla oldószert tartalmaz
- Veclam 250 mg granulátum belsőleges szuszpenzióhoz:
Kartondoboz 14 db 250 mg -os tasakot tartalmaz
- Veclam 500 mg granulátum belsőleges szuszpenzióhoz:
Kartondoboz, amely 14 db 500 mg -os tasakot tartalmaz
06.6 Használati utasítás
Lásd a 4.2 pontot
07.0 FORGALOMBA HOZATALI ENGEDÉLY
MALESCI Farmakobiológiai Intézet S.p.A. Via Lungo l "Ema, 7 - Bagno a Ripoli (FI)
Az ABBOTT S.r.l. licence alapján - Campoverde di Aprilia (LT)
08.0 A FORGALOMBA HOZATALI ENGEDÉLY SZÁMA
Veclam 250 mg bevont tabletta:
12 buborékcsomagolás - AIC 027529054
Veclam 500 mg bevont tabletta:
Blister 14 tabletta - AIC 027529116
Veclam 125 mg / 5 ml granulátum belsőleges szuszpenzióhoz:
100 ml -es palack - AIC 027529041
Veclam 250 mg / 5 ml granulátum belsőleges szuszpenzióhoz:
100 ml -es palack - AIC 027529104
Veclam 250 mg granulátum belsőleges szuszpenzióhoz:
14 tasak - AIC 027529080
Veclam 500 mg granulátum belsőleges szuszpenzióhoz:
14 tasak - AIC 027529092
Veclam 500 mg / 10 ml por és oldószer oldatos infúzióhoz:
Palack + oldószeres injekciós üveg - AIC 027529039
Veclam RM 500 mg módosított hatóanyag -leadású tabletta:
7 db módosított hatóanyag -leadású tablettát tartalmazó buborékcsomagolás - AIC n. 027529130
09.0 Az első forgalomba hozatali engedély kiadásának időpontja
Veclam 250 mg bevont tabletta 1997.02.19
Veclam 500 mg bevont tabletta 1999.03.03
Veclam 125 mg/5 ml granulátum belsőleges szuszpenzióhoz 1997.02.19
Veclam 500 mg/10 ml por és oldószer oldatos infúzióhoz 1992.04.01
Veclam 250 mg/5 ml granulátum belsőleges szuszpenzióhoz 1999.08.17
Veclam 250 mg granulátum belsőleges szuszpenzióhoz 1999.03.17
Veclam 500 mg granulátum belsőleges szuszpenzióhoz 1999.03.17
Veclam RM 500 mg módosított hatóanyag -leadású tabletta 2001.05.30
Az engedély megújítása: 2010.05.31
10.0 A SZÖVEG FELÜLVIZSGÁLÁSÁNAK DÁTUMA
Az AIFA 2015. áprilisi meghatározása