Hatóanyagok: Lamotrigin
Lamictal 2 mg diszpergálódó / rágótabletta
Lamictal 5 mg diszpergálódó / rágótabletta
Lamictal 25 mg diszpergálódó / rágótabletta
Lamictal 50 mg diszpergálódó / rágótabletta
Lamictal 100 mg diszpergálódó / rágótabletta
Lamictal 200 mg diszpergálódó / rágótabletta
Miért alkalmazzák a Lamictalt? Mire való?
A Lamictal az epilepszia elleni gyógyszerek csoportjába tartozik. Két állapot - epilepszia és bipoláris zavar - kezelésére alkalmazzák.
A Lamictal az epilepsziát úgy kezeli, hogy blokkolja az agyban a görcsöket (görcsöket) kiváltó jeleket.
- Felnőtteknél és 13 éves vagy idősebb gyermekeknél a Lamictal önmagában vagy más gyógyszerekkel együtt alkalmazható epilepszia kezelésére, míg a Lamictal más gyógyszerekkel együtt is alkalmazható a Lennox-Gastaut-szindróma nevű állapotban fellépő görcsök kezelésére.
- 2 és 12 év közötti gyermekeknél a Lamictal más gyógyszerekkel együtt alkalmazható ezen állapotok kezelésére. Önmagában is alkalmazható az epilepszia egyik típusának, az úgynevezett tipikus távollétrohamok kezelésére.
A Lamictal a bipoláris zavarokat is kezeli.
A bipoláris zavarban (más néven mániás depresszióban) szenvedő betegeknél hirtelen szélsőséges hangulatváltozások tapasztalhatók, mániás időszakok (izgalom vagy eufória) váltakoznak depressziós időszakokkal (mély szomorúság vagy kétségbeesés). 18 éves vagy annál idősebb felnőtteknél önmagában vagy más gyógyszerekkel együtt a bipoláris zavarban előforduló depressziós rohamok megelőzésére. Egyelőre nem ismert, hogy a Lamictal hogyan fejti ki hatását az agyban.
Ellenjavallatok Amikor a Lamictal -t nem szabad alkalmazni
Ne szedje a Lamictal -t:
- ha allergiás (túlérzékeny) a lamotriginre vagy a gyógyszer (6. pontban felsorolt) egyéb összetevőjére.
Ha ez vonatkozik Önre:
- tájékoztassa kezelőorvosát, és ne szedje a Lamictal -t.
Az alkalmazással kapcsolatos óvintézkedések Mit kell tudnia a Lamictal szedése előtt
A Lamictal fokozott elővigyázatossággal alkalmazható
A Lamictal szedése előtt beszéljen kezelőorvosával vagy gyógyszerészével:
- ha bármilyen veseproblémája van
- ha valaha kiütései voltak a lamotrigin vagy más bipoláris zavar vagy epilepszia kezelésére szolgáló gyógyszerek bevétele után
- ha valaha is agyhártyagyulladása volt a lamotrigin szedése után (kérjük, olvassa el e tünetek leírását a betegtájékoztató 4. pontjában: Egyéb mellékhatások).
- ha már lamotrigint tartalmazó gyógyszereket szed.
Ha ezek közül bármelyik vonatkozik Önre:
- tájékoztassa kezelőorvosát, aki dönthet az adag csökkentéséről, vagy arról, hogy a Lamictal nem megfelelő az Ön számára.
Fontos információk a potenciálisan életveszélyes reakciókkal kapcsolatban
A Lamictal-t szedő betegek kis számának allergiás reakciója vagy potenciálisan életveszélyes bőrreakciója van, amely kezelés nélkül súlyosabb problémákat okozhat. Tudnia kell, hogy a Lamictal szedése során mire kell figyelni.
Olvassa el ezeknek a tüneteknek a leírását a betegtájékoztató 4. szakaszában „Potenciálisan életveszélyes reakciók: azonnal forduljon orvoshoz”.
Öngyilkosság vagy öngyilkosság gondolatai
Az epilepszia elleni gyógyszereket különböző állapotok, köztük az epilepszia és a bipoláris zavar kezelésére használják. A bipoláris zavarban szenvedő embereknek néha eszükbe juthat, hogy ártanak maguknak vagy öngyilkosságot követnek el.
- amikor először elkezdi a kezelést
- ha korábban gondolatai merültek fel önmagának ártása vagy öngyilkosság miatt
- ha 25 év alatti.
Ha gondolatai vagy tapasztalatai vannak, amelyek zavarják Önt, vagy ha észreveszi, hogy rosszabbul érzi magát, vagy új tünetek jelentkeznek a Lamictal szedése alatt:
- a lehető leghamarabb forduljon orvosához, vagy menjen a legközelebbi kórházba segítségért.
Az epilepsziaellenes szerekkel, például a Lamictal -lal kezelt betegek egy kis hányada gondolt arra is, hogy ártson vagy öngyilkos legyen. Ha bármikor ilyen gondolatai támadnak, azonnal forduljon orvosához.
Ha a Lamictal -t epilepszia kezelésére szedi
Az epilepszia egyes típusaiban a görcsrohamok időnként súlyosbodhatnak vagy gyakrabban fordulhatnak elő a Lamictal -kezelés alatt.
Néhány beteg súlyos rohamokat kaphat, amelyek súlyos egészségügyi problémákat okozhatnak.
Ha a görcsök gyakoribbá válnak, vagy ha súlyos rohamai vannak a Lamictal szedése alatt:
- forduljon orvosához a lehető leghamarabb.
A Lamictal nem adható 18 év alatti személyeknek bipoláris zavar kezelésére. A depressziót és más mentális egészségi problémákat kezelő gyógyszerek növelik az öngyilkossági gondolatok és viselkedés kockázatát gyermekeknél és 18 év alatti serdülőknél.
Kölcsönhatások Mely gyógyszerek vagy élelmiszerek módosíthatják a Lamictal hatását
Feltétlenül tájékoztassa kezelőorvosát vagy gyógyszerészét a jelenleg vagy nemrégiben szedett, valamint szedni tervezett egyéb gyógyszereiről, beleértve a növényi készítményeket vagy más vény nélkül kapható gyógyszereket.
Orvosának tudnia kell, hogy más gyógyszereket szed -e epilepszia vagy mentális egészségi problémák kezelésére, hogy megbizonyosodjon arról, hogy a Lamictal megfelelő adagját alkalmazza. Ezek a gyógyszerek a következők:
- oxkarbazepin, felbamát, gabapentin, levetiracetám, pregabalin, topiramát vagy zonisamid, epilepszia kezelésére
- lítium, olanzapin vagy aripiprazol mentális egészségügyi problémák kezelésére
- bupropion, amelyet mentális egészségügyi problémák kezelésére vagy a dohányzás abbahagyására használnak
Tájékoztassa kezelőorvosát, ha ezen gyógyszerek bármelyikét szedi.
Egyes gyógyszerek kölcsönhatásba lépnek a Lamictal -lal, vagy valószínűbbé teszik a mellékhatásokat.
Ezek tartalmazzák:
- valproát, epilepszia és mentális egészségügyi problémák kezelésére használják
- karbamazepin, epilepszia és mentális egészségügyi problémák kezelésére használják
- fenitoin, primidon vagy fenobarbitál, epilepszia kezelésére használt riszperidon, mentális egészségügyi problémák kezelésére
- rifampicin, antibiotikum
- a humán immunhiányos vírus (HIV) fertőzés kezelésére használt gyógyszerek (lopinavir és ritonavir vagy atazanavir és ritonavir kombinációja)
- hormonális fogamzásgátlók, például tabletta (lásd alább)
Tájékoztassa kezelőorvosát, ha ezen gyógyszerek bármelyikét szedi, elkezdi vagy abbahagyja.
A hormonális fogamzásgátlók (például a tabletták) megváltoztathatják a Lamictal hatását
Orvosa javasolhatja bizonyos típusú hormonális fogamzásgátlók vagy más fogamzásgátló módszerek, például óvszer, rekeszizom vagy tekercs használatát. Ha hormonális fogamzásgátlót, például tablettát használ, orvosa vérmintát vehet a Lamictal szintjének ellenőrzésére. Ha hormonális fogamzásgátlót használ vagy tervezi, hogy elkezdi használni:
tájékoztassa kezelőorvosát, aki megbeszéli Önnel a megfelelő fogamzásgátló módszereket.
A Lamictal megváltoztathatja a hormonális fogamzásgátlók működését is, bár nem valószínű, hogy csökkenti a hatékonyságukat. Ha hormonális fogamzásgátlót használ, és bármilyen változást észlel a menstruációjában, például hirtelen vérzést vagy menstruáció közötti vérzést:
mondja el orvosának. Ezek arra utalhatnak, hogy a Lamictal megváltoztatja a fogamzásgátló hatását.
Figyelmeztetések Fontos tudni, hogy:
Terhesség és szoptatás
Fokozottan fennáll a születési rendellenességek kockázata azoknál a csecsemőknél, akiknek anyja terhesség alatt szedte a Lamictal -t. Ezek a hibák közé tartozik az ajakhasadék (ajakhasadék) vagy a szájpadlás (szájpadhasadék). Orvosa azt tanácsolhatja Önnek, hogy vegyen be „kiegészítő folsavat”, ha terhességet tervez, vagy ha már terhes.
A terhesség szintén befolyásolhatja a Lamictal hatékonyságát, ezért vérvizsgálatra és a Lamictal adagjának módosítására lehet szükség.
- Ha Ön terhes, vagy ha fennáll Önnél a terhesség lehetősége vagy gyermeket szeretne, a gyógyszer alkalmazása előtt beszéljen kezelőorvosával vagy gyógyszerészével. Ne hagyja abba a kezelést anélkül, hogy megbeszélné orvosával. Ez különösen akkor fontos, ha epilepsziás.
- Ha Ön szoptat vagy szoptatni tervez, a gyógyszer szedése előtt kérje ki kezelőorvosa vagy gyógyszerésze tanácsát. A Lamictal hatóanyaga behatol az anya mellébe, és hatással lehet a babára. Kezelőorvosa beszélni fog Önnel a szoptatás kockázatairól és előnyeiről a Lamictal szedése alatt, és időnként ellenőrizni fogja gyermekét, ha úgy dönt, hogy szoptat.
A készítmény hatásai a gépjárművezetéshez és gépek kezeléséhez szükséges képességekre
A Lamictal szédülést és kettős látást okozhat.
- Ne vezessen gépjárművet vagy ne kezeljen gépeket, ha nem biztos abban, hogy nincsenek ilyen tünetei.
Ha epilepsziában szenved, beszéljen kezelőorvosával a gépjárművezetésről és a gépek kezeléséről.
Adagolás, az alkalmazás módja és ideje A Lamictal alkalmazása: Adagolás
Ezt a gyógyszert mindig az orvos vagy a gyógyszerész által elmondottaknak megfelelően szedje. Ha kétségei vannak, forduljon orvosához vagy gyógyszerészéhez.
Mennyi Lamictal -t kell bevennie
Eltarthat egy ideig, amíg megtalálja az Ön számára optimális Lamictal adagot. A szükséges adag az alábbiaktól függ:
- korától
- ha a Lamictal -t más gyógyszerekkel együtt szedi
- ha bármilyen vese- vagy májbetegsége van.
Kezdetben orvosa alacsony adagot ír elő, és néhány hét alatt fokozatosan növeli az adagot, amíg el nem éri az Önnek megfelelő dózist (az úgynevezett hatékony dózist). Ne vegyen be több Lamictal -t, mint amennyit orvosa előírt.
A Lamictal szokásos hatékony adagja felnőtteknél és 13 éves vagy idősebb gyermekeknél naponta 100 mg és 400 mg között van.
2-12 éves gyermekeknél a hatékony dózis a testtömegtől függ - általában 1 mg és 15 mg között van a gyermek súlyának minden kilogrammjánál, de legfeljebb napi 200 mg fenntartó adag.
A Lamictal nem ajánlott 2 év alatti gyermekek számára.
Hogyan kell bevenni a Lamictal adagját?
Vegye be a Lamictal adagját naponta egyszer vagy kétszer, ahogy orvosa mondta. Étkezés közben vagy attól függetlenül is bevehető.
- Mindig vegye be az orvos által előírt teljes adagot. Soha ne vegye be a tabletta csak egy részét.
Kezelőorvosa azt is tanácsolhatja, hogy kezdje el vagy hagyja abba más gyógyszerek szedését, attól függően, hogy milyen körülmények között szedik őket, és hogyan reagál a kezelésre.
A Lamictal diszpergálódó / rágótablettákat egészben, kevés vízzel le lehet nyelni, rágni vagy vízzel keverni folyékony gyógyszer előállításához.
A tabletta rágásához:
Előfordulhat, hogy egyidejűleg vizet kell innia, hogy a tabletta feloldódjon a szájában. Ezután igyon még egy kis vizet, hogy megbizonyosodjon arról, hogy az összes gyógyszert lenyelte.
A gyógyszer folyékonyvá tétele:
- Tegye a tablettát egy pohárba, annyi vízzel, hogy legalább ellepje az egész tablettát.
- A tabletta feloldásához keverje meg vagy várjon, amíg a tabletta teljesen fel nem oldódik.
- Igyon meg minden folyadékot.
- Öntsön egy kis vizet a pohárba, és igya meg, hogy ne maradjon gyógyszer a pohárban.
Túladagolás Mi a teendő, ha túl sok Lamictalt vett be?
Ha az előírtnál több Lamictal -t vett be
- Azonnal forduljon orvosához vagy a legközelebbi kórház sürgősségi osztályához. Ha lehetséges, mutasd meg nekik a Lamictal csomagot.
Ha túl sok Lamictal -t vett be, nagyobb valószínűséggel jelentkeznek súlyos mellékhatások, amelyek halálosak lehetnek.
Bárki, aki túl sok Lamictal -t vett be, az alábbi tünetek bármelyikét tapasztalhatja:
- gyors, ellenőrizhetetlen szemmozgások (nystagmus)
- ügyetlenség és koordináció hiánya, ami megváltoztatja az egyensúlyt (ataxia)
- szívritmus változás (általában az EKG -n látható)
- eszméletvesztés, görcsök vagy kóma.
Ha elfelejtette bevenni a Lamictal -t
Ne vegyen be további tablettákat a kihagyott adag pótlására. A következő adagot a szokásos időben vegye be.
Kérje orvosa tanácsát, hogyan kezdje el újra szedni. Ne hagyja abba a Lamictal szedését orvosa tanácsa nélkül
A Lamictal -t addig kell szedni, amíg orvosa javasolja. Ne hagyja abba, hacsak orvosa nem mondja.
Ha a Lamictal -t epilepszia kezelésére szedi
A Lamictal szedésének abbahagyásához fontos, hogy az adagot fokozatosan, körülbelül 2 hét alatt csökkentse Ha hirtelen abbahagyja a Lamictal szedését, epilepsziája visszatérhet vagy rosszabbodhat.
Ha a Lamictal -t bipoláris zavar kezelésére szedi
A Lamictal eltarthat egy ideig, amíg hatni fog, így nem valószínű, hogy azonnal jobban érzi magát. Ha abbahagyja a Lamictal szedését, nem kell fokozatosan csökkentenie az adagot. De ha abba akarja hagyni a Lamictal szedését, először mindig beszéljen orvosával.
Mellékhatások Melyek a Lamictal mellékhatásai?
Mint minden gyógyszer, így ez a gyógyszer is okozhat mellékhatásokat, amelyek azonban nem mindenkinél jelentkeznek.
Potenciálisan életveszélyes reakciók: Azonnal orvosi segítséget kell kérni
A Lamictal-t szedő betegek kis számának allergiás reakciója vagy potenciálisan életveszélyes bőrreakciója van, amely kezelés nélkül súlyosabb problémákat okozhat.
Ezek a tünetek nagyobb valószínűséggel jelentkeznek a Lamictal -kezelés első néhány hónapjában, különösen akkor, ha a kezdő adag túl magas, vagy ha az adagot túl gyorsan emelik, vagy ha a Lamictal -t egy másik, valproát nevű gyógyszerrel együtt alkalmazzák. Ezen tünetek némelyike gyakoribb a gyermekeknél, ezért a szülőknek különös figyelmet kell fordítaniuk előfordulására.
Az ilyen reakciók tünetei a következők:
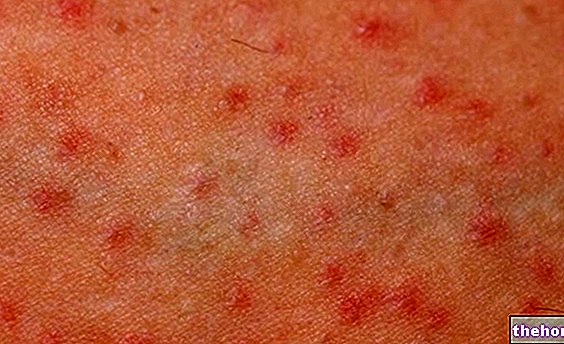
- kiütés vagy bőrpír, amely életveszélyes bőrreakciókká alakulhat, beleértve a széles körű kiütéseket hólyagosodással és bőrhámlással, különösen a száj, az orr, a szem és a nemi szervek környékén (Stevens-Johnson-szindróma), a bőr széles körű hámlása (a testfelület több mint 30% -a - toxikus epidermális nekrolízis)
- fekélyek a szájban, a torokban, az orrban vagy a nemi szervekben
- fájdalom a szájban vagy vörös, duzzadt szem (kötőhártya -gyulladás)
- magas hőmérséklet (láz), influenzaszerű tünetek vagy álmosság
- az arc duzzanata vagy a nyak, hónalj vagy ágyék duzzadt mirigyei
- váratlan vérzés vagy véraláfutás, vagy az ujjak kékre váltása
- torokfájás, vagy a szokásosnál több fertőzés (például megfázás).
Sok esetben ezek a tünetek kevésbé súlyos mellékhatások jelei. De tisztában kell lennie azzal, hogy potenciálisan életveszélyesek, és ha nem kezelik őket, súlyosabb problémákká, például szervi elégtelenséggé alakulhatnak ki. Ha az alábbi tünetek bármelyikét észleli:
- azonnal forduljon orvosához. Orvosa dönthet úgy, hogy máj-, vese- vagy vérvizsgálatot végez, és utasíthatja a Lamictal szedésének abbahagyását.
Nagyon gyakori mellékhatások
10 beteg közül több mint 1 beteget érinthetnek:
- fejfájás
- kiütés
Gyakori mellékhatások
10 beteg közül legfeljebb 1 beteget érinthetnek:
- agresszivitás vagy ingerlékenység
- álmosság
- szédülés
- rázkódások vagy remegések
- alvászavar (álmatlanság)
- agitáció
- hasmenés
- száraz száj
- hányinger vagy hányás
- fáradtság
- fájdalom a hátban, az ízületekben vagy máshol.
Nem gyakori mellékhatások
100 beteg közül legfeljebb 1 beteget érinthetnek:
- ügyetlenség és a koordináció hiánya (ataxia)
- kettős látás vagy homályos látás
Ritka mellékhatások
Ezek 1000 beteg közül legfeljebb 1 beteget érinthetnek:
- életveszélyes bőrreakció (Stevens-Johnson szindróma): lásd még a 4. pont elején található információkat.
- a kapcsolódó tünetek csoportja, amelyek közé tartozik: láz, hányinger, hányás, fejfájás, nyakmerevség és erős fényérzékenység. Ennek oka lehet az agyat és a gerincvelőt körülvevő membránok gyulladása (meningitis). Ezek a tünetek általában elmúlnak a kezelés abbahagyása után, de ha a tünetek továbbra is fennállnak vagy súlyosbodnak, forduljon orvosához.
- gyors, ellenőrizhetetlen szemmozgások (nystagmus)
- viszkető szemek, folyással és a szemhéjak kérgesedésével (kötőhártya -gyulladás)
Nagyon ritka mellékhatások
Ezek 10 000 -ből legfeljebb 1 beteget érinthetnek:
- életveszélyes bőrreakció (toxikus epidermális nekrolízis): lásd még a 4. pont elején található információkat.
- magas hőmérséklet (láz): lásd még a 4. pont elején található információkat.
- az arc duzzanata (ödéma) vagy a nyak, a hónalj vagy az ágyék mirigyeinek duzzanata (limfadenopátia): lásd még a 4. pont elején található információkat.
- a májfunkció változásai, amelyeket vérvizsgálatok mutatnak ki, vagy májelégtelenség: lásd még a 4. pont elején található információkat.
- súlyos véralvadási rendellenesség, amely váratlan vérzést vagy véraláfutást okozhat (disszeminált intravaszkuláris koaguláció): lásd még a 4. pont elején található információkat.
- a vérvizsgálatokkal kimutatható változások - beleértve a vörösvértestek számának csökkenését (vérszegénység), a fehérvérsejtek számának csökkenését (leukopenia, neutropenia, agranulocitózis), a vérlemezkék számának csökkenését (trombocitopénia) ), ezen sejttípusok számának csökkenése (pancytopenia) és az aplasztikus anaemia nevű csontvelő -rendellenesség.
- hallucinációk (valójában nem létező dolgok "látása" vagy "hallása")
- zavar
- „ingatagnak” vagy instabilnak érzi magát a mozgásban
- ellenőrizhetetlen testmozgások (tics), ellenőrizhetetlen izomgörcsök, amelyek a szemet, a fejet és a törzset érintik (koreoatetózis), vagy más szokatlan testmozgások, például remegés, remegés vagy merevség
- görcsrohamok gyakrabban fordulnak elő olyan embereknél, akik már epilepsziában szenvednek
- a Parkinson -kórban már szenvedő betegeknél a tünetek súlyosbodása.
- lupus-szerű reakciók (tünetek lehetnek: hát- vagy ízületi fájdalom, amelyet néha láz és / vagy általános rossz közérzet kísérhet).
Egyéb mellékhatások
Más mellékhatások is előfordultak néhány embernél, de gyakoriságuk nem ismert:
- Csontbetegségekről, köztük csontritkulásról és csontritkulásról (csontritkulás) és törésekről számoltak be. Kérdezze meg kezelőorvosát vagy gyógyszerészét, ha hosszú távú epilepsziaellenes kezelésben részesül, csontritkulásban szenved, vagy szteroidokat szed.
Ha Önnél mellékhatások jelentkeznek
- Ha Önnél bármilyen mellékhatás jelentkezik, tájékoztassa erről kezelőorvosát vagy gyógyszerészét. Ez a betegtájékoztatóban fel nem sorolt bármilyen lehetséges mellékhatásra is vonatkozik.
Lejárat és megőrzés
A gyógyszer gyermekektől elzárva tartandó!
A buborékcsomagoláson, a dobozon vagy a palackon feltüntetett lejárati idő után ne alkalmazza ezt a gyógyszert. A lejárati idő az adott hónap utolsó napjára vonatkozik.
A Lamictal nem igényel különleges tárolási körülményeket.
Semmilyen gyógyszert ne dobjon a szennyvízbe vagy a háztartási hulladékba. Kérdezze meg gyógyszerészét, hogy mit tegyen a már nem használt gyógyszereivel. Ez elősegíti a környezet védelmét.
Összetétel és gyógyszerforma
Mit tartalmaz a Lamictal diszpergálódó / rágótabletta
A készítmény hatóanyaga a lamotrigin. Minden diszpergálódó / rágótabletta 2 mg, 5 mg, 25 mg, 50 mg, 100 mg vagy 200 mg lamotrigint tartalmaz.
Egyéb összetevők: kalcium-karbonát, alacsony szubsztituált hidroxi-propil-cellulóz, magnézium-alumínium-szilikát, nátrium-keményítő-glikolát (A típus), povidon K30, nátrium-szacharin, magnézium-sztearát, feketeribizli aroma.
Milyen a Lamictal diszpergálódó / rágótabletta külleme és mit tartalmaz a csomagolás?
A Lamictal diszpergálódó / rágótabletta (minden erősség) fehér vagy törtfehér, és enyhén tompa lehet. Fekete ribizli illatúak.
Előfordulhat, hogy nem minden kiszerelés kerül kereskedelmi forgalomba az Ön országában.
A 2 mg -os diszpergálódó / rágótabletta kerek. Az egyik oldalon a "2" szám fölött "LTG" jelzés található; a másik oldalon két derékszögben átfedő ovális, minden egyes palack 30 tablettát tartalmaz.
Az 5 mg -os diszpergálható / rágótabletta hosszúkás, ívelt oldalú. Az egyik oldalon "GSCL2" jelzéssel vannak ellátva; Minden csomagolás 10, 14, 28, 30, 50 vagy 56 tablettát tartalmazó buborékcsomagolást tartalmaz.
A 25 mg -os diszpergálható / rágótabletta négyzet alakú, lekerekített sarkokkal. Az egyik oldalon "GSCL5" jelöléssel vannak ellátva; és "25" a másik oldalon. Minden csomag 10, 14, 21, 28, 30, 42, 50, 56 vagy 60 tablettát tartalmazó buborékcsomagolást tartalmaz. A 21 vagy 42 tablettát tartalmazó kezdőcsomagok az első néhány hétben használhatók. kezelés, amikor az adagot lassan kell emelni.
Az 50 mg -os diszpergálható / rágótabletta négyzet alakú, lekerekített sarkokkal. Az egyik oldalon "GSCX7" jelzéssel vannak ellátva; és "50" a másik oldalon. Minden csomag 10, 14, 28, 30, 42, 50, 56, 60, 90, 98, 100, 196 vagy 200 tablettát tartalmazó buborékcsomagolást tartalmaz. 42 tablettát tartalmazó kezdőcsomagolás használható a kezelés első heteiben, amikor az adagot lassan kell emelni.
A 100 mg -os diszpergálható / rágótabletta négyzet alakú, lekerekített sarkokkal. Az egyik oldalon "GSCL7" jelöléssel vannak ellátva; A csomagolás 10, 14, 28, 30, 42, 50, 56, 60, 90, 98, 100, 196 vagy 200 tablettát tartalmazó buborékcsomagolást tartalmaz.
A 200 mg -os diszpergálható / rágótabletta négyzet alakú, lekerekített sarkokkal. Az egyik oldalon "GSEC5" jelzéssel vannak ellátva; A csomagolás 10, 14, 28, 30, 42, 50, 56, 60, 90, 98, 100, 196 vagy 200 tablettát tartalmazó buborékcsomagolást tartalmaz.
Forrás betegtájékoztató: AIFA (Olasz Gyógyszerügynökség). A tartalom 2016 januárjában jelent meg. A jelenlévő információk nem feltétlenül naprakészek.
A legfrissebb verzióhoz való hozzáféréshez ajánlatos az AIFA (Olasz Gyógyszerügynökség) webhelyét elérni. Jogi nyilatkozat és hasznos információk.
01.0 A GYÓGYSZER MEGNEVEZÉSE
LAMICTAL diszpergálható / rágható tabletták
02.0 MINŐSÉGI ÉS MENNYISÉGI ÖSSZETÉTEL
Minden Lamictal 5 mg diszpergálódó / rágótabletta 5 mg lamotrigint tartalmaz
Minden Lamictal 25 mg diszpergálódó / rágótabletta 25 mg lamotrigint tartalmaz
Minden Lamictal 50 mg diszpergálódó / rágótabletta 50 mg lamotrigint tartalmaz
Minden Lamictal 100 mg diszpergálódó / rágótabletta 100 mg lamotrigint tartalmaz
Minden Lamictal 200 mg diszpergálódó / rágótabletta 200 mg lamotrigint tartalmaz
A segédanyagok teljes listáját lásd a 6.1 pontban.
03.0 GYÓGYSZERFORMA
Diszpergálható / rágható tabletta.
5 mg diszpergálódó / rágótabletta:
Fehér vagy törtfehér, hosszúkás, mindkét oldalán domború, fekete ribizli szagú tabletta, egyik oldalán "GS CL2", másik oldalán "5" mélynyomással.
25 mg diszpergálódó / rágótabletta:
Fehér vagy törtfehér, többoldalas, elliptikus tabletta, fekete ribizli szaggal, egyik oldalán "GSCL5", másik oldalán "25" mélynyomással.
50 mg diszpergálódó / rágótabletta:
Fehér vagy törtfehér, többoldalas elliptikus tabletta, fekete ribizli szaggal, egyik oldalán "GSCX7", másik oldalán "50" mélynyomással.
100 mg diszpergálódó / rágótabletta:
Fehér vagy törtfehér, többoldalas, elliptikus tabletta, fekete ribizli szaggal, egyik oldalán "GSCL7", másik oldalán "100" mélynyomással.
200 mg diszpergálódó / rágótabletta:
Fehér vagy törtfehér, többoldalas elliptikus tabletta, fekete ribizli szaggal, egyik oldalán "GSEC5", másik oldalán "200" mélynyomással.
04.0 KLINIKAI INFORMÁCIÓK
04.1 Terápiás javallatok
Epilepszia
Felnőttek és 13 éves és idősebb serdülők
- Kiegészítő vagy monoterápiás kezelés részleges görcsök és generalizált rohamok, beleértve a tónusos-klónikus rohamokat.
- Lennox-Gastaut-szindrómával kapcsolatos válságok. A Lamictal-t kiegészítő terápiaként alkalmazzák, de Lennox-Gastaut szindróma esetén kezdetben az epilepszia elleni gyógyszer lehet.
Gyermekek és serdülők 2-12 éves korig
-Részleges rohamok és generalizált rohamok kiegészítő kezelése, beleértve a tónusos-klónikus rohamokat és a Lennox-Gastaut-szindrómával kapcsolatos rohamokat.
- A tipikus hiányrohamok monoterápiája.
Bipoláris zavar
18 éves és idősebb felnőttek
- A depressziós epizódok megelőzése I -es típusú bipoláris zavarban szenvedő betegeknél, akik túlnyomórészt depressziós epizódokkal rendelkeznek (lásd 5.1 pont).
A Lamictal nem javallott mániás vagy depressziós epizódok akut kezelésére.
04.2 Adagolás és alkalmazás
A diszpergálható / rágható tablettákat rághatja, feloldhatja kis mennyiségű vízben (legalább annyira, hogy az egész tablettát ellepje), vagy egészben, kevés vízzel lenyelheti.
Ha a lamotrigin kiszámított dózisa (pl. Epilepsziás gyermekek vagy májelégtelenségben szenvedő gyermekek kezelésében) nem egyezik meg a teljes tablettákkal, akkor a beadandó adag megegyezik a legalacsonyabb egész tablettával.
A terápia folytatása a felfüggesztés után
Amikor a Lamictal-kezelést újrakezdi azoknál a betegeknél, akik bármilyen okból abbahagyták, az orvosnak mérlegelnie kell, hogy a fenntartó dózis elérése érdekében fokozatosan kell titrálni, mivel a súlyos kiütések kockázata összefügg a nagy kezdeti dózisok alkalmazásával és az ajánlott titrálás által előírt adag túllépése (lásd 4.4 pont). Minél hosszabb az előző adagtól eltelt idő, annál jobban meg kell fontolni a titrálás alkalmazását egymást követő lépésekben a fenntartás elérése érdekében. öt felezési idő (lásd 5.2 pont), a Lamictal dózis titrálása a fenntartó dózis eléréséhez általában a megfelelő adagolási sémát követi.
Javasolt, hogy a Lamictal adagolását ne folytassák azoknál a betegeknél, akik abbahagyták az adagolást a korábbi lamotrigin -kezeléssel járó kiütések miatt, kivéve, ha a lehetséges előny egyértelműen meghaladja a kockázatot.
Epilepszia
Az alábbiakban ismertetjük az ajánlott adagolást a dózis titrálásához és a fenntartó dózishoz felnőtteknél és 13 éves vagy idősebb serdülőknél (1. táblázat), valamint gyermekeknél és serdülőknél 2–12 éves korban (2. táblázat). A kiütés kockázata miatt a kezdeti és a következő adagokat nem szabad túllépni a titráláshoz (lásd 4.4 pont).
Ha az egyidejűleg alkalmazott epilepsziaellenes gyógyszereket abbahagyják, vagy ha más, epilepszia elleni vagy egyéb gyógyszereket adnak a lamotrigint tartalmazó kezelési rendhez, akkor figyelembe kell venni ennek a lamotrigin farmakokinetikájára gyakorolt hatását (lásd 4.5 pont).
1. táblázat: Felnőttek és 13 éves vagy idősebb serdülők - ajánlott adagolási rend epilepsziában
2. táblázat: 2-12 éves gyermekek és serdülők - ajánlott adagolási rend epilepsziában (teljes napi adag mg / testtömeg -kilogramm / nap)
A terápiás adag fenntartásának biztosítása érdekében ellenőrizni kell a gyermek testtömegét, és testtömegváltozás esetén felül kell vizsgálni az adagot. A két -hat éves betegek valószínűleg fenntartják az ajánlott adagolás felső határait.
Ha az epilepszia kezelését kiegészítő kezeléssel érik el, az egyidejűleg alkalmazott epilepszia elleni gyógyszereket abba kell hagyni, és a betegek folytathatják a Lamictal monoterápiás kezelést.
5 mg diszpergálódó / rágótabletta: ha a 2 mg -os diszpergálódó / rágótabletta nincs forgalomban, és a Lamictal 5 mg diszpergálódó / rágótabletta a legalacsonyabb adag a piacon:
Figyelembe kell venni, hogy a jelenleg rendelkezésre álló 5 mg -os Lamictal diszpergálható / rágótablettával a 17 kg -nál kisebb testtömegű gyermekeknél nem lehet pontosan elkezdeni a lamotrigin -kezelést az ajánlott adagolási irányelvek alapján.
2 év alatti gyermekek
Kevés adat áll rendelkezésre a lamotrigin hatékonyságáról és biztonságosságáról részleges rohamok kiegészítő terápiájaként 1 hónapos és 2 év közötti gyermekeknél (lásd 4.4 pont). 1 hónaposnál fiatalabb gyermekeknél nincsenek adatok. Ezért a Lamictal alkalmazása nem javasolt két évesnél fiatalabb gyermekeknél ajánlott. Ha a klinikai szükségletek alapján mégis dönt a kezelésről, lásd 4.4, 5.1 és 5.2 pont.
Bipoláris zavar
Az alábbi táblázatok az ajánlott adagolást mutatják a dózis titrálásához és a fenntartó dózishoz 18 éves és idősebb felnőtteknél. Az átmeneti adagolási rend magában foglalja a lamotrigin adagjának növelését a fenntartó dózisig, amelyet hat hetes időszak alatt kell elérni (lásd a 3. táblázatot), ekkor, ha klinikailag indokolt, más pszichotróp és / vagy epilepszia elleni gyógyszereket felfüggeszthetnek (lásd. Táblázat). Az adagolás módosítása más pszichotróp és / vagy epilepszia elleni gyógyszerek hozzáadását követően szintén az alábbiakban látható (5. táblázat). A kiütés veszélye miatt a kezdeti és a későbbi adagokat nem szabad túllépni a titráláshoz (lásd 4.4 pont).
3. táblázat: 18 éves és idősebb felnőttek - ajánlott adagolási rend a stabilizáló fenntartó teljes napi dózis eléréséhez a bipoláris zavar kezelésében
(*) Az elérni kívánt stabilizáló dózis a klinikai választól függően változik.
4. táblázat: 18 éves és idősebb felnőttek - teljes napi adagolási rend a stabilizáció fenntartása érdekében, ha abbahagyják a bipoláris zavar kezelésére szolgáló egyéb egyidejű gyógyszerek szedését.
Miután elérte a stabilizáló fenntartó napi adagot, a többi gyógyszer az alábbiakban leírtak szerint abbahagyható.
(*) Az adag szükség esetén napi 400 mg -ra emelhető
5. táblázat: 18 éves és idősebb felnőttek - ütemterv a lamotrigin napi adagjának módosítására a bipoláris zavar kezelésére szolgáló egyéb gyógyszerek hozzáadását követően.
Nincs klinikai tapasztalat a lamotrigin dózisának más gyógyszerek hozzáadását követő módosításával kapcsolatban. A más gyógyszerekkel való interakciós vizsgálatok alapján azonban a következő ajánlásokat lehet tenni:
A Lamictal abbahagyása bipoláris zavarban szenvedő betegeknél.
A klinikai vizsgálatokban a lamotrigin -kezelés hirtelen abbahagyását követően nem nőtt a mellékhatások gyakorisága, súlyossága vagy típusa a placebóhoz képest. Ezért a betegek abbahagyhatják a lamotrigin szedését az adag csökkentése nélkül.
Gyermekek és 18 év alatti serdülők.
A lamotrigin alkalmazása 18 év alatti gyermekeknél nem javallt a biztonságosságra és a hatásosságra vonatkozó adatok hiánya miatt (lásd 4.4 pont).
Általános ajánlások a Lamictal adagolására speciális betegpopulációkban
Hormonális fogamzásgátlót szedő nők
Az etinil -ösztradiol / levonorgesztrel (30 mcg / 150 mcg) kombináció alkalmazása növeli tisztítás megközelítőleg kétszeresére csökkenti a lamotrigin szintjét, ami a plazma lamotriginszintjének csökkenését eredményezi. A dózistitrálási fázis után az optimális terápiás válasz eléréséhez magasabb (legfeljebb kétszeres) lamotrigin fenntartó adagokra lehet szükség. A tabletták nélküli hét során a lamotrigin szint kétszeres növekedését figyelték meg. Az adaggal kapcsolatos nemkívánatos események nem zárhatók ki. Ezért a pirula nélküli fogamzásgátlás alkalmazását első vonalbeli kezelésnek kell tekinteni (pl. Folyamatos hormonális fogamzásgátlók vagy nem hormonális módszerek; lásd 4.4 és 4.5 pont).
Hormonális fogamzásgátló kezelés megkezdése azoknál a betegeknél, akik már fenntartó lamotrigin adagokat szednek, és NEM szednek lamotrigin glükuronidációt indukáló szereket
A lamotrigin fenntartó adagjait sok esetben kétszeresére kell emelni (lásd 4.4 és 4.5 pont). Javasoljuk, hogy a hormonális fogamzásgátló kezelés kezdetétől kezdve a lamotrigin adagját hetente 50 mg -ról 100 mg -ra emeljék, az egyéni klinikai válasz alapján. Annak megerősítésére, hogy a kiindulási lamotrigin -koncentráció megmarad, mérlegelhető a szérum lamotrigin -koncentráció mérése a hormonális fogamzásgátló kezelés megkezdése előtt és után. Szükség esetén az adagot módosítani kell. Fogamzásgátlót szedő nőknél. -szabad hét "), a szérum lamotriginszintet monitorozni kell az aktív kezelés 3. hetében, azaz a tabletta ciklus 15. napjától 21. napjáig. terápia (pl. folyamatos hormonális fogamzásgátlók vagy nem hormonális módszerek; lásd 4.4 és 4.5 pont).
A hormonális fogamzásgátlók visszavonása azoknál a betegeknél, akik már lamotrigin fenntartó adagokat szednek, és NEM szednek lamotrigin -glükuronidációt indukáló szereket
A lamotrigin fenntartó adagjait a legtöbb esetben legfeljebb 50% -kal kell csökkenteni (lásd 4.4 és 4.5 pont). Javasoljuk, hogy fokozatosan csökkentse a lamotrigin napi adagját 50-100 mg-mal hetente (százalékban, amely nem haladja meg a heti teljes adag 25% -át), 3 hét alatt, hacsak a klinikai válasz másképp nem jelzi. Annak megerősítésére, hogy a kiindulási lamotrigin -koncentráció megmarad, mérlegelhető a szérum lamotrigin -koncentráció mérése a hormonális fogamzásgátló kezelés előtt és után. Azoknál a nőknél, akik abba akarják hagyni a hormonális fogamzásgátló szedését, amely egy hét inaktív kezelést ("tabletta nélküli hét") tartalmaz, a szérum lamotrigin szintjét ellenőrizni kell az aktív kezelés 3. hetében, azaz a 15. naptól a pirulázási ciklus 21. napjáig. A fogamzásgátló tabletta végleges abbahagyása után a lamotriginszint meghatározásához szükséges mintákat nem szabad a tabletta abbahagyását követő első héten gyűjteni.
A lamotrigin -kezelés megkezdése olyan betegeknél, akik már hormonális fogamzásgátlót szednek
A dózistitrálásnak a táblázatokban leírt szokásos adagolási ajánlásokat kell követnie.
A hormonális fogamzásgátló kezelés megkezdése és abbahagyása azoknál a betegeknél, akik már fenntartó dózisú lamotrigint szednek, és szedik a lamotrigin -glükuronidációt előidézőket
Előfordulhat, hogy a lamotrigin ajánlott karbantartási adagolásának módosítására nincs szükség.
Alkalmazza atazanavir / ritonavirrel
Ha a meglévő atazanavir / ritonavir terápiához lamotrigint adnak, nem szükséges módosítani a lamotrigin ajánlott csökkentő adagját.
Azoknál a betegeknél, akik már fenntartó lamotrigin adagokat szednek, és nem szednek glükuronidáció -induktorokat, előfordulhat, hogy növelni kell a lamotrigin adagját, ha atazanavirt / ritonavirt adnak hozzá, vagy csökkenteni kell az atazanavir / ritonavir abbahagyását. A lamotrigin plazmában történő monitorozását az atazanavir / ritonavir megkezdése vagy abbahagyása előtt, majd ezt követően 2 hétig kell ellenőrizni, hogy szükséges -e a lamotrigin adagjának módosítása (lásd 4.5 pont).
Lopinavir / ritonavirrel együtt kell alkalmazni
Ha a meglévő lopinavir / ritonavir terápiához lamotrigint adnak, nem szükséges módosítani a lamotrigin ajánlott csökkentő adagját.
Azoknál a betegeknél, akik már fenntartó lamotrigin adagokat szednek, és nem szednek glükuronidáció -induktorokat, előfordulhat, hogy a lamotrigin dózisát növelni kell, ha lopinavirt / ritonavirt adnak hozzá, vagy csökkenteni kell, ha a lopinavir / ritonavir felfüggesztését abbahagyják. A lamotrigin plazmában történő monitorozását el kell végezni a lopinavir / ritonavir megkezdése vagy abbahagyása előtt, majd ezt követően 2 hétig, hogy kiderüljön, szükséges -e a lamotrigin adagjának módosítása (lásd 4.5 pont).
Idősek (65 év felett)
Az ajánlott adagolási rendben nincs szükség az adag módosítására. A lamotrigin farmakokinetikája ebben a korcsoportban nem tér el jelentősen a nem idős felnőtt populációtól (lásd 5.2 pont).
Vesekárosodás
Óvatosan kell eljárni, ha a Lamictal -t veseelégtelenségben szenvedő betegeknek adják. Végstádiumú veseelégtelenségben szenvedő betegeknél a lamotrigin kezdő adagját a beteg egyidejű gyógyszerein kell alapulnia; csökkent fenntartó dózisok hatékonyak lehetnek jelentős vesekárosodásban szenvedő betegeknél (lásd 4.4 és 5.2 pont).
Májkárosodás
A kezdeti, titrálási és fenntartó adagokat általában körülbelül 50% -kal kell csökkenteni közepesen súlyos májkárosodásban (Child-Pugh B fokozat) és 75% -ban súlyos májkárosodásban szenvedő betegeknél (Child-Pugh C fokozat). A titrálási és fenntartó adagokat a klinikai válasznak megfelelően kell beállítani (lásd 5.2 pont).
04.3 Ellenjavallatok
A készítmény hatóanyagával vagy bármely segédanyagával szembeni túlérzékenység.
04.4 Különleges figyelmeztetések és a használathoz szükséges óvintézkedések
Kiütés
Bőrrel kapcsolatos mellékhatásokról számoltak be, amelyek általában a lamotrigin-kezelés megkezdését követő első nyolc hétben jelentkeztek. A kiütések többsége enyhe és magától megszűnik, azonban súlyos bőrreakciókat is jelentettek, amelyek miatt kórházi kezelésre és a lamotrigin-kezelés abbahagyására volt szükség. potenciálisan életveszélyes kiütéseket, például Stevens-Johnson-szindrómát és toxikus epidermális nekrolízist tartalmazott (lásd 4.8 pont).
A jelenleg ajánlott lamotrigin -adagolási rendet alkalmazó klinikai vizsgálatokba bevont felnőtt betegeknél a súlyos kiütések előfordulási gyakorisága körülbelül minden 500 epilepsziás beteg. Az esetek körülbelül felét Stevens -szindrómának jelentették. Johnson (1000 -ből 1).
A bipoláris zavarban szenvedő betegek klinikai vizsgálatai során a súlyos kiütések előfordulási gyakorisága körülbelül 1: 1000.
A súlyos kiütések kockázata gyermekeknél nagyobb, mint felnőtteknél.Egyes tanulmányok rendelkezésre álló adatai azt mutatják, hogy a kórházi kezeléssel járó kiütések gyakorisága epilepsziás gyermekeknél 1: 300 és 1: 100 között van.
Gyermekeknél a "kiütés kezdeti megnyilvánulása fertőzéssel összetéveszthető", az orvosnak mérlegelnie kell a lamotrigin -kezelésre adott reakció lehetőségét azoknál a gyermekeknél, akiknél a kezelés első nyolc hetében kiütések és láz tünetei alakulnak ki.
Ezenkívül a bőrkiütés általános kockázata erősen összefügg a következőkkel:
- a lamotrigin kezdeti nagy dózisa, amely meghaladja a lamotrigin terápia dózisának titrálásához javasolt dózist (lásd 4.2 pont)
- valproát egyidejű alkalmazása (lásd 4.2 pont).
Óvatosság ajánlott azoknál a betegeknél is, akik más epilepsziaellenes gyógyszereket követően allergiásak vagy kiütések voltak, mivel a lamotrigin-kezelést követő nem súlyos kiütések gyakorisága ezeknél a betegeknél megközelítőleg háromszor nagyobb volt, mint azoknál, akiknél nem volt ez az anamnézis. .
Minden kiütést észlelő beteget (felnőttet és gyermeket) azonnal ki kell értékelni, és a Lamictal -kezelést azonnal abba kell hagyni, kivéve, ha a kiütés nyilvánvalóan nem kapcsolódik a lamotrigin -kezeléshez. Javasoljuk, hogy ne folytassa újra a Lamictal -t azoknál a betegeknél, akik a "korábbi" bőrkiütés miatt abbahagyták. lamotrigin -kezelés, kivéve, ha a lehetséges előny egyértelműen meghaladja a kockázatot.
Kiütéseket jelentettek olyan túlérzékenységi szindróma összefüggésében is, amely szisztémás tünetek, mint például láz, limfadenopátia, arcödéma, kóros hematológiai és májparaméterek és aszeptikus meningitis változó mintázatával jár együtt (lásd 4.8 pont). A szindróma klinikai súlyossága széles spektrumú, és ritkán disszeminált intravaszkuláris koagulációhoz és többszervi elégtelenséghez vezethet. Fontos megjegyezni, hogy a túlérzékenység korai megnyilvánulásai (pl. Láz, limfadenopátia) továbbra is előfordulhatnak kiütés nélkül. Ha ilyen jelek és tünetek jelentkeznek, a beteget azonnal ki kell vizsgálni, és a Lamictal -kezelést fel kell függeszteni mindaddig, amíg meg nem állapítható az alternatív etiológia.
Az aszeptikus agyhártyagyulladás sok esetben reverzibilis volt a gyógyszer megvonásával, de számos esetben kiújult a lamotrigin újbóli expozíciója esetén. Az ismételt expozíció a gyakran súlyosabb tünetek gyors visszatérését eredményezte. A lamotrigint nem szabad újrakezdeni olyan betegeknél, akik a korábbi lamotrigin -kezeléssel összefüggő aszeptikus meningitis miatt abbahagyták a kezelést.
Klinikai súlyosbodás és öngyilkossági kockázat
Öngyilkossági gondolatokat és viselkedést jelentettek epilepsziaellenes gyógyszerekkel különböző indikációk miatt kezelt betegeknél. Az epilepsziaellenes szerekkel végzett randomizált, placebo-kontrollos vizsgálatok metaanalízise szintén kismértékben növelte az öngyilkossági gondolatok és magatartás kockázatát. Ennek a kockázatnak a mechanizmusa nem ismert, és a rendelkezésre álló adatok nem zárják ki a lamotrigin fokozott kockázatának lehetőségét.
Ezért a betegeket ellenőrizni kell az öngyilkossági gondolatok és magatartás jelei tekintetében, és meg kell fontolni a megfelelő kezelést. A betegeket (és gondozóikat) tanácsolni kell, hogy forduljanak orvoshoz, ha öngyilkossági gondolatok és magatartások jelei jelentkeznek.
A depressziós tünetek és / vagy az öngyilkossági hajlam súlyosbodhatnak bipoláris zavarban szenvedő betegeknél, függetlenül attól, hogy bipoláris zavar kezelésére szolgáló gyógyszereket szednek -e, beleértve a Lamictalt.
Ezért a Lamictal -t bipoláris rendellenességben kapó betegeket gondosan figyelemmel kell kísérni a klinikai rosszabbodás (beleértve az új tünetek kialakulását) és az öngyilkossági hajlam tekintetében, különösen a kezelés kezdetén vagy az adag módosítása idején. Néhány beteg, például öngyilkossági magatartás vagy gondolatok története, fiatal felnőttek és azok a betegek, akik a kezelés megkezdése előtt jelentős szintű öngyilkossági gondolatokat tapasztalnak, fokozottan veszélyeztethetik az öngyilkossági gondolatokat vagy öngyilkossági kísérleteket, és gondosan ellenőrizni kell őket a kezelés során.
A kezelési rend módosítását, beleértve a gyógyszer abbahagyásának lehetőségét, meg kell fontolni azoknál a betegeknél, akiknél a klinikai állapot súlyosbodása (beleértve az új tünetek kialakulását) és / vagy öngyilkossági gondolatok / viselkedés alakul ki, különösen, ha ezek a tünetek súlyosak, hirtelen. kezdetben, vagy nem voltak jelen a beteg kezdeti tünetei között.
Hormonális fogamzásgátlók
A hormonális fogamzásgátlók hatása a lamotrigin hatékonyságára
Az etinil -ösztradiol / levonorgesztrel (30 mcg / 150 mcg) kombináció alkalmazása növeli tisztítás kb. kétszeresére, ami a plazma lamotriginszintjének csökkenését eredményezi (lásd 4.5 pont). A lamotriginszint csökkenését a rohamok kontrolljának elvesztésével hozták összefüggésbe. A dózis -titrálási fázis után sok esetben magasabb (legfeljebb kétszeres) lamotrigin fenntartó dózisra lehet szükség az optimális terápiás válasz eléréséhez. A hormonális fogamzásgátlók leállításakor a tisztítás a lamotrigin felére csökkenthető. A lamotrigin koncentrációjának növekedése az adagtól függő mellékhatásokkal járhat. E tekintetben a betegeket figyelemmel kell kísérni.
Azoknál a nőknél, akik még nem szednek lamotrigin-glükuronidációt kiváltó gyógyszereket, és hormonális fogamzásgátlót szednek, amely egy hetes inaktív kezelést foglal magában (pl. „Tabletta nélküli hét”), a kezelés hetében a lamotrigin plazmaszintjének átmeneti fokozatos növekedése fordulhat elő. a kezelés abbahagyása (lásd 4.2 pont). A lamotrigin ilyen mértékű változása káros hatásokkal járhat. Ezért a tablettamentes héttől eltérő fogamzásgátlás (pl. Folyamatos hormonális fogamzásgátlók vagy nem hormonális módszerek) alkalmazását első vonalbeli kezelésnek kell tekinteni.
Más orális fogamzásgátlók vagy hormonpótló kezelések lamotriginnel való kölcsönhatását nem vizsgálták, bár hasonló módon befolyásolhatják a lamotrigin farmakokinetikai paramétereit.
A lamotrigin hatása a hormonális fogamzásgátlók hatékonyságára
Egy interakciós vizsgálat 16 egészséges önkéntes részvételével kimutatta, hogy ha lamotrigint és hormonális fogamzásgátlót (etinilösztradiol / levonorgesztrel kombináció) adnak együtt, akkor kismértékben megnő az tisztítás levonorgesztrel és a szérum FSH- és LH -szint változásai (lásd 4.5 pont). Ezen változások hatása a petefészek ovulációs aktivitására nem ismert. Mindazonáltal nem zárható ki annak lehetősége, hogy ezek a változások a fogamzásgátlás hatékonyságának csökkenéséhez vezethetnek egyes betegeknél, akik hormonkészítményeket szednek lamotriginnel. Ezért a betegeket tanácsolni kell, hogy haladéktalanul jelentsék a menstruációs ciklusukban bekövetkezett változásokat, például hirtelen vérzést.
Dihidrofolát -reduktáz
Mivel a lamotrigin a dihidrofolát-reduktáz gyenge inhibitora, a folsav-anyagcsere zavarhat a hosszú távú kezelés során (lásd 4.6 pont).
Azonban a lamotrigin -kezelés hosszú ideig nem mutatott szignifikáns változásokat a hemoglobin -koncentrációban, az átlagos corpuscularis térfogatban és a szérum- és intra -eritrocita -folsav -koncentrációkban legfeljebb egy évig, vagy az eritrocita -folát -koncentrációban legfeljebb 5 évig.
Veseelégtelenség
Végső stádiumú veseelégtelenségben szenvedő alanyokkal végzett egyszeri dózisú vizsgálatokban a lamotrigin plazmakoncentrációja nem változott jelentősen. Mivel azonban a glükuronid -metabolit felhalmozódására kell számítani, óvatosság ajánlott veseelégtelenségben szenvedő betegek kezelésekor.
A lamotrigint tartalmazó egyéb készítményeket szedő betegek
A Lamictal nem adható olyan betegeknek, akik más, lamotrigint tartalmazó készítménnyel kezelik anélkül, hogy előzetesen konzultálnának orvosukkal.
Fejlődés gyermekeknél
Nincs adat a lamotrigin növekedésre, szexuális érésre, valamint kognitív, érzelmi és viselkedési fejlődésre gyakorolt hatásáról gyermekeknél.
Az epilepsziával kapcsolatos óvintézkedések
A többi epilepszia elleni gyógyszerhez hasonlóan a Lamictal hirtelen abbahagyása is visszapattanó rohamokat okozhat.
A szakirodalomban olyan esetekről számoltak be, amelyekben súlyos rohamok, köztük a status epilepticus, rabdomiolízishez, többszervi diszfunkcióhoz és disszeminált intravaszkuláris koagulációhoz vezethetnek, néha halálos kimenetelűek. Hasonló esetek fordultak elő a lamotrigin alkalmazásával kapcsolatban.
A rohamok gyakoriságának klinikailag jelentős romlása figyelhető meg, nem pedig javulás. Azoknál a betegeknél, akiknél egynél több rohamtípus van, az egyik rohamtípus ellenőrzésében megfigyelt előnyöket mérlegelni kell egy másik rohamtípusban észlelt rosszabbodással szemben.
A mioklonikus rohamokat súlyosbíthatja a lamotrigin.
Az adatok arra utalnak, hogy az enziminduktorokat tartalmazó kombinációra adott válasz alacsonyabb, mint a nem enzimet indukáló epilepsziaellenes szereket tartalmazó kombinációra adott válasz. Az ok nem világos.
A tipikus távollétű epilepszia kezelésére lamotrigint szedő gyermekeknél a hatásosság nem biztos, hogy minden betegnél fennmarad.
A bipoláris zavarhoz kapcsolódó óvintézkedések
Gyermekek és 18 év alatti serdülők
Az antidepresszánsokkal történő kezelés az öngyilkossági gondolatok és magatartás fokozott kockázatával jár a súlyos depressziós és más pszichiátriai rendellenességekben szenvedő gyermekek és serdülők körében.
04.5 Kölcsönhatások más gyógyszerekkel és más interakciók
Interakciós vizsgálatokat csak felnőtteknél végeztek.
Az UDP-glükuroniltranszferázt azonosították a lamotrigin metabolizmusáért felelős enzimként. Nincs bizonyíték arra, hogy a lamotrigin klinikailag jelentős indukciót vagy gátlást okozna az oxidatív májgyógyszert metabolizáló enzimekben, és nem valószínű, hogy kölcsönhatás lenne a lamotrigin és a citokróm P450 metabolizált gyógyszerek között. A lamotrigin saját anyagcseréjét indukálhatja, de a hatás szerény, és nem valószínű, hogy klinikailag jelentős következményekkel járna.
6. táblázat: Más gyógyszerek hatása a lamotrigin -glükuronidációra
* Az adagolásra vonatkozó útmutatás (lásd 4.2 pont)
** Más hormonális fogamzásgátlókat és hormonpótló kezeléseket nem vizsgáltak, de valószínűleg hasonlóan befolyásolják a lamotrigin farmakokinetikai paramétereit (lásd 4.2 és 4.4 pont).
Kölcsönhatások epilepszia elleni szerekkel
A valproát a lamotrigin glükuronidációjának gátlásával lelassítja annak anyagcseréjét, és körülbelül kétszeresére növeli az átlagos felezési idejét.A valproáttal egyidejűleg kezelt betegeknél a megfelelő terápiás sémát kell alkalmazni (lásd 4.2 pont).
Néhány epilepszia elleni gyógyszer (például fenitoin, karbamazepin, fenobarbitál és primidon) a gyógyszereket metabolizáló májenzimek indukálásával indukálja a lamotrigin glükuronidációját és felgyorsítja annak anyagcseréjét. Azoknál a betegeknél, akik fenitoint, karbamazepint, fenobarbitált vagy primidont kapnak egyidejűleg, a megfelelő terápiás sémát kell alkalmazni (lásd 4.2 pont).
Jelentést kaptak a központi idegrendszerre gyakorolt hatásokról, beleértve a szédülést, ataxiát, diplopiát, homályos látást és hányingert azoknál a betegeknél, akik karbamazepint szedtek a lamotrigin -kezelés megkezdése után. Ezek az események rendszerint csökkenéssel megszűnnek. Hasonló hatást figyeltek meg egy lamotriginnel végzett vizsgálatban és oxkarbazepint egészséges felnőtt önkéntesekben, bár az adagcsökkentést nem vizsgálták.
A szakirodalomban vannak jelentések a lamotrigin szintjének csökkenéséről, amikor a lamotrigint oxcabazepinnel kombinálták. Azonban egy egészséges felnőtt önkénteseken végzett vizsgálatban, amelyet 200 mg lamotriginnel és 1200 mg oxkarbazepinnel kezeltek, az oxkarbazepin nem változtatta meg a lamotrigin metabolizmusát, és a lamotrigin nem változtatta meg az oxkarbazepin metabolizmusát. Ezért a kezelésben részesülő betegeknél. valproát és lamotrigin -glükuronidáció induktorok nélküli terápiát kell alkalmazni (lásd 4.2 pont).
Egy egészséges önkénteseken végzett vizsgálatban a felbamát (1200 mg naponta kétszer) és a lamotrigin (100 mg naponta kétszer 10 napon keresztül) együttes alkalmazása nem bizonyította klinikailag releváns hatást a lamotrigin farmakokinetikájára.
A lamotrigint gabapentinnel vagy anélkül kapó betegek plazmaszintjének retrospektív elemzése alapján a gabapentin nem bizonyította, hogy megváltoztatja a tisztítás nyilvánvaló a lamotrigin.
A levetiracetám és a lamotrigin közötti lehetséges gyógyszerkölcsönhatásokat a két gyógyszer szérumkoncentrációjának értékelésével határozták meg a placebo-kontrollos klinikai vizsgálatokban. Ezek az adatok azt mutatják, hogy a lamotrigin nem befolyásolja a levetiracetám farmakokinetikáját, és a levetiracetám nem befolyásolja a lamotrigin farmakokinetikáját.
Az egyensúlyi állapotú, minimális lamotrigin plazmakoncentrációt nem befolyásolta a pregabalin (napi 3-szor 200 mg) egyidejű alkalmazása. A lamotrigin és a pregabalin között nincs farmakokinetikai kölcsönhatás.
A topiramát nem okozott változást a lamotrigin plazmakoncentrációjában. A lamotrigin beadása a topiramát koncentrációjának 15% -os növekedését eredményezte.
Egy epilepsziás betegeken végzett vizsgálatban a zonisamid (napi 200–400 mg) és a lamotrigin (napi 150–500 mg) együttes alkalmazása 35 napon keresztül nem volt jelentős hatással a lamotrigin farmakokinetikájára.
Bár más AED -k plazmakoncentrációjának változásáról is beszámoltak, az ellenőrzött vizsgálatok nem mutattak bizonyítékot arra, hogy a lamotrigin befolyásolja az egyidejűleg alkalmazott AED plazmakoncentrációját. Oktatás in vitro azt jelzik, hogy a lamotrigin nem szorítja ki más epilepszia elleni gyógyszereket a fehérjekötő helyekről.
Más pszichoaktív szerekkel kapcsolatos kölcsönhatások
A lítium farmakokinetikája, amelyet 2 egészséges vízmentes lítium-glükonát napi kétszeri, hat napon át 20 egészséges alanynak történő beadása után értékeltek, nem változott a napi 100 mg lamotrigin együttes alkalmazásával.
A bupropion többszörös orális adagja nem volt statisztikailag szignifikáns hatással a lamotrigin egyetlen adagjának farmakokinetikájára 12 alanyban, a bupropion csak kismértékben emelte a lamotrigin -glükuronid AUC -jét.
Egy egészséges felnőtt önkénteseken végzett vizsgálatban 15 mg olanzapin 24% -kal, illetve 20% -kal csökkentette a lamotrigin átlagos AUC -értékét és Cmax -értékét. Egy ilyen nagyságú hatás nem tekinthető általában klinikailag relevánsnak. A lamotrigin 200 mg -os dózisban nem változtatja meg az olanzapin farmakokinetikáját.
A lamotrigin napi 400 mg -os többszörös orális adagja nem gyakorolt klinikailag jelentős hatást egyetlen, 2 mg -os risperidon adag farmakokinetikájára 14 egészséges felnőtt önkéntesben. 2 mg riszperidon és lamotrigin egyidejű beadását követően 14 önkéntes közül 12 jelentett álmosságot, míg a riszperidont önmagában adva 20 -ból 1 -et, és egyetlen lamotriginnel sem.
Egy 18 bipoláris zavarban szenvedő felnőtt betegen végzett vizsgálatban, akik stabil lamotrigin-kezelést kaptak (napi 100-400 mg), az aripiprazol adagját a napi 10 mg-ról a tervezett napi 30 mg-ra emelték. napi időszakban, és további 7 napig naponta egyszer folytatják. Megfigyelték, hogy a lamotrigin Cmax és AUC értéke körülbelül 10% -kal csökken. Egy ekkora hatás várhatóan nem jár klinikai következményekkel.
Oktatás in vitro azt jelzik, hogy az elsődleges lamotrigin metabolit, a 2-N-glükuronid képződését korlátozott mértékben befolyásolta az amitriptilinnel, bupropionnal, klonazepámmal, haloperidollal vagy lorazepámmal történő együttes inkubáció. Ezek a vizsgálatok azt is sugallják, hogy a klozapin, a fluoxetin, a fenelzin, a riszperidon, a szertralin vagy a trazodon valószínűleg nem befolyásolja a lamotrigin metabolizmusát. Továbbá, a bufuralol metabolizmusának tanulmányozása humán májmikroszóma -készítmények felhasználásával azt sugallja, hogy a lamotrigin nem csökkenti tisztítás túlnyomórészt a CYP2D6 által metabolizált gyógyszerek.
A hormonális fogamzásgátlókat érintő kölcsönhatások
A hormonális fogamzásgátlók hatása a lamotrigin farmakokinetikájára
Egy 16 önkéntes nőt vizsgáló vizsgálatban 30 mcg etinil-ösztradiolt / 150 mcg levonorgesztrelt tartalmazó kombinált orális fogamzásgátló alkalmazása körülbelül kétszeres növekedést okozott tisztítás szájon át adott lamotrigin, ami a lamotrigin AUC és Cmax értékeinek átlagosan 52% -os, illetve 39% -os csökkenését eredményezi. A szérum lamotrigin koncentrációja fokozatosan emelkedett az inaktív kezelési hét során (beleértve a "tabletta nélküli hetet"), az inaktív kezelési hét végén az adag előtti koncentrációk átlagosan körülbelül kétszer magasabbak voltak, mint az inaktív kezelésnél héten a fogamzásgátlóval történő egyidejű alkalmazás (lásd 4.4 pont). A hormonális fogamzásgátlók önmagukban történő alkalmazása nem teszi szükségessé az ajánlott adag módosítását a titrálás során, de a hormonális fogamzásgátló kezelés megkezdésekor vagy abbahagyásakor sok esetben növelni vagy csökkenteni kell a lamotrigin fenntartó adagját (lásd 4.2 pont).
A lamotrigin hatása a hormonális fogamzásgátlók farmakokinetikájára
Egy 16 önkéntes nőt vizsgáló vizsgálatban a 300 mg lamotrigin egyensúlyi dózisa nem volt hatással a kombinált orális fogamzásgátló összetevőjének, az etinilösztradiolnak a farmakokinetikájára. tisztítás a másik komponens, a levonorgesztrel, ami a levonorgesztrel AUC és Cmax átlagértékeinek 19% -os, illetve 12% -os csökkenését eredményezi. Az FSH, az LH és az ösztradiol szérumszintjének mérése a vizsgálat során azt mutatta, hogy petefészek hormonális aktivitás néhány nőnél, bár a szérum progeszteron mérése nem mutatott hormonális bizonyítékot az ovulációra a 16 alany egyikében sem. A szerény növekedés hatása tisztítás levonorgesztrel és a szérum FSH- és LH -értékek változása a petefészek ovulációs aktivitására nem ismert (lásd 4.4 pont). A napi 300 mg -os lamotrigin dózisok hatásait nem vizsgálták, és más női hormonkészítményekkel nem végeztek vizsgálatokat.
Más gyógyszerekkel kapcsolatos kölcsönhatások
Egy 10 önkéntes férfi vizsgálatban a rifampicin növelte a tisztítás a glükuronidációért felelős májenzimek indukciója miatt csökkentette a lamotrigin hatását és felezési idejét.
Egy egészséges önkénteseken végzett vizsgálatban a lopinavir / ritonavir megközelítőleg a felére csökkentette a lamotrigin plazmakoncentrációját, valószínűleg a glükuronidáció indukciójával. Azoknál a betegeknél, akik egyidejűleg lopinavir / ritonavir terápiát kapnak, a megfelelő terápiás sémát kell alkalmazni (lásd 4.2 pont).
Egy egészséges felnőtt önkénteseken végzett vizsgálatban az atazanavir / ritonavir (300 mg / 100 mg) 9 napon át történő alkalmazása átlagosan 32% -kal, illetve 6% -kal csökkentette a lamotrigin (egyszeri 100 mg -os adag) plazma AUC -értékét és Cmax -értékét. Azoknál a betegeknél, akik egyidejűleg atazanavir / ritonavir terápiát kapnak, a megfelelő terápiás sémát kell alkalmazni (lásd 4.2 pont).
Értékelésből származó adatok in vitro azt mutatják, hogy a lamotrigin, de nem az N-glükuronid metabolit, gátolja a "Szerves transzporter 2 (OCT 2) potenciálisan klinikailag releváns koncentrációban. Ezek az adatok azt mutatják, hogy a lamotrigin inhibitor in vitro erősebb OCT 2, mint a cimetidin, IC50 értékei 53,8 mcM és 186 mcM. A lamotrigin és az OCT 2 szubsztrátjai, a vesén keresztül kiválasztott gyógyszerek (például metformin, gabapentin és vareniklin) egyidejű alkalmazása ezen gyógyszerek plazmaszintjének emelkedését eredményezheti.
Ennek klinikai jelentősége nincs egyértelműen meghatározva, azonban óvatosan kell eljárni azoknál a betegeknél, akik ezeket a gyógyszereket egyidejűleg kapják.
04.6 Terhesség és szoptatás
Az epilepszia elleni szerekkel kapcsolatos kockázatok általában
Szakértői tanácsot kell kérni azoknak a nőknek, akik potenciálisan terhesek. Ha a nő terhességet tervez, újra kell gondolni az epilepszia elleni kezelés szükségességét. Mindenesetre kerülni kell az epilepszia elleni kezelés hirtelen megszakítását az epilepsziás kezelés alatt álló nőknél, mivel ez hirtelen rohamokhoz vezethet, amelyek súlyos következményekkel járhatnak az anyára és a születendő gyermekre nézve.
A veleszületett fejlődési rendellenességek kockázata 2-3 -szorosára nő az antiepileptikumokkal kezelt anyák születésekor, szemben az általános populációban előforduló várható gyakorisággal, ami körülbelül 3%. A leggyakrabban jelentett hibák az ajakhasadék, a szív- és érrendszeri rendellenességek és hibák. A politerapia a veleszületett rendellenességek nagyobb kockázatával jár, mint a monoterápia, ezért lehetőség szerint monoterápiát kell alkalmazni.
A lamotriginnel kapcsolatos kockázatok
Terhesség
Számos leendő terhességi nyilvántartás forgalomba hozatal utáni adatai dokumentálták az eredményeket több mint 2000 nőnél, akik a terhesség első trimeszterében lamotrigin monoterápiának voltak kitéve. Összességében ezek az adatok nem utalnak a súlyos veleszületett rendellenességek kockázatának jelentős növekedésére, bár az adatok még mindig túl korlátozottak ahhoz, hogy kizárják a szájüregi kockázat mérsékelt növekedését. Az állatokon végzett vizsgálatok fejlődési toxikus hatásokat mutattak (lásd 5.3 pont).
Ha a Lamictal -kezelést terhesség alatt szükségesnek ítélik, ajánlott a lehető legalacsonyabb terápiás dózist alkalmazni.
A lamotrigin enyhe gátló hatást fejt ki a dihidrofolát -reduktázra, ezért elméletileg a folsavszint csökkentése révén az embrionális / magzati károsodás fokozott kockázatához vezethet (lásd 4.4 pont). A folsav adagolása megfontolható a terhesség tervezésekor és a terhesség korai szakaszában.
A terhesség alatti élettani változások befolyásolhatják a lamotrigin szintjét és / vagy terápiás hatását. Előfordultak olyan esetek, amikor a lamotrigin plazmaszintje csökkent a terhesség alatt, és fennáll a rohamok kontrolljának elvesztésének kockázata. Szülés után a lamotrigin szintje gyorsan emelkedhet, és fennáll a dózisfüggő mellékhatások kockázata. Ezért a szérum lamotrigin koncentrációját ellenőrizni kell a terhesség előtt, alatt és után, valamint közvetlenül a születés után. Szükség esetén az adagot úgy kell módosítani, hogy a szérum lamotrigin -koncentráció a terhesség előtti szinten maradjon, vagy a klinikai válasznak megfelelően. Ezenkívül a dózistól függő nemkívánatos hatásokat a születés után ellenőrizni kell.
Etetési idő
Jelentések szerint a lamotrigin nagymértékben változó koncentrációban jut be az anyatejbe, ami a teljes lamotriginszintet a csecsemőben az anyaihoz viszonyítva körülbelül 50% -ig eredményezi. Ezért néhány szoptatott csecsemőnél a lamotrigin szérumkoncentrációja elérheti azt a szintet, amelynél a farmakológiai hatások jelentkeznek. A kitett gyermekek korlátozott csoportjában nem figyeltek meg káros hatásokat.
A szoptatás lehetséges előnyeit mérlegelni kell a csecsemőre gyakorolt káros hatások lehetséges kockázatával szemben.Ha egy nő úgy dönt, hogy szoptat a lamotrigin -kezelés alatt, a babát figyelni kell a káros hatásokra.
Termékenység
Az állatokon végzett vizsgálatok nem mutatták ki a lamotrigin által okozott termékenységi károsodást (lásd 5.3 pont).
04.7 Hatások a gépjárművezetéshez és gépek kezeléséhez szükséges képességekre
Mivel az epilepszia elleni terápiában alkalmazott összes gyógyszerre adott válasz változhat, a Lamictal -t epilepszia kezelésére szedő betegeknek konzultálniuk kell orvosukkal a vezetés és az epilepszia következményeiről.
Nem végeztek vizsgálatokat a gépjárművezetéshez és gépek kezeléséhez szükséges képességekre gyakorolt hatásokról. Két, önkénteseken végzett vizsgálat kimutatta, hogy a lamotrigin hatása a finom látási motoros koordinációra, a szemmozgásokra, a testmozgásokra és a nyugtató hatásokra. Szubjektív hatások nem különböznek a placebótól. A lamotriginnel végzett klinikai vizsgálatok során neurológiai nemkívánatos hatásokról, például szédülésről és diplopiáról számoltak be, ezért a betegeknek figyelniük kell a Lamictal -kezelés hatásait.
04.8 Nemkívánatos hatások
A nemkívánatos hatásokat a jelenleg rendelkezésre álló adatok alapján epilepsziára és bipoláris zavarra osztották, azonban a lamotrigin általános biztonságossági profiljának mérlegelésekor mindkettővel konzultálni kell.
A monoterápiás klinikai vizsgálatokban († szimbólummal azonosított) és más klinikai tapasztalatok során azonosított mellékhatásokat az alábbi táblázat tartalmazza, a klinikai vizsgálatokban előforduló gyakoriságuk szerint.
A nemkívánatos hatások osztályozására a következő egyezményt használták: nagyon gyakori (≥1 / 10); gyakori (≥1 / 100 -
Epilepszia
A kiválasztott mellékhatások leírása
1 A hematológiai rendellenességek és a limfadenopátia társulhat vagy nem társulhat túlérzékenységi szindrómához (lásd Immunrendszeri betegségek2).
2 Kiütésekről számoltak be olyan túlérzékenységi szindrómával összefüggésben, amely különböző szisztémás tünetekkel, például láz, limfadenopátia, arcödéma, hematológiai és májparaméterek változásával jár. Ez a szindróma a klinikai súlyosság széles spektrumát mutatja, és ritkán disszeminált intravaszkuláris koagulációhoz és többszervi elégtelenséghez vezethet. Fontos megjegyezni, hogy a túlérzékenység korai megnyilvánulásai (pl. Láz, limfadenopátia) a kiütés minden jele nélkül is előfordulhatnak. Ha ilyen jelek / tünetek jelentkeznek, a beteget azonnal ki kell értékelni, és a Lamictal -kezelést fel kell függeszteni mindaddig, amíg meg nem állapítható az alternatív etiológia.
3 Ezeket a hatásokat más klinikai tapasztalatok során jelentették. Beszámoltak arról, hogy a lamotrigin rontja a Parkinson-kór tüneteit a már meglévő Parkinson-kórban szenvedő betegeknél, és az extrapiramidális hatások és a koreoatetózis elszigetelt eseteiről számoltak be az alapbetegségben nem szenvedő betegeknél.
4 A májműködési zavar általában túlérzékenységi reakciókkal együtt jelentkezik, de egyedi esetekről, amelyekben nincsenek nyilvánvaló túlérzékenységi jelek, beszámoltak.
További felnőtteken végzett kettős vak klinikai vizsgálatokban bőrkiütések fordultak elő a lamotrigint szedő betegek körülbelül 10% -ánál és a placebót szedő betegek 5% -ánál. A bőrkiütések a betegek 2% -ánál a lamotrigin -kezelés abbahagyásához vezettek. A kiütés, amely rendszerint makulopapulárisan jelenik meg, általában a kezelés megkezdését követő nyolc héten belül jelentkezik, és a Lamictal -kezelés abbahagyása után megszűnik (lásd 4.4 pont).
Súlyos, potenciálisan életveszélyes bőrkiütésekről számoltak be, beleértve a Stevens-Johnson-szindrómát és a toxikus epidermális nekrolízist (Lyell-szindróma). Bár a betegek többségénél ezek a reakciók a lamotrigin -kezelés abbahagyásakor megszűnnek, egyes esetekben maradandó hegesedés maradhat, és ritkán halálos kimenetelű esetek is előfordultak (lásd 4.4 pont).
A bőrkiütés általános kockázata erősen összefügg a következőkkel:
- a lamotrigin kezdeti nagy dózisa, amely meghaladja a lamotrigin -terápiában javasolt dózisnövelést (lásd 4.2 pont);
- valproát egyidejű alkalmazása (lásd 4.2 pont).
Kiütésekről is beszámoltak a szisztémás tünetek változó klinikai képével összefüggő túlérzékenységi szindróma részeként (lásd Immunrendszeri betegségek2).
Bipoláris zavar
A lamotrigin általános biztonsági profiljának elérése érdekében az alább felsorolt nemkívánatos hatásokat az epilepsziás betegeknél jelentett mellékhatásokkal együtt kell figyelembe venni. A táblázatban szereplő mellékhatásokat a bipoláris zavar klinikai vizsgálatai során azonosították.
1 A bipoláris rendellenességben a lamotriginnel végzett összes (kontrollált és nem kontrollált) vizsgálatot figyelembe véve bőrkiütések jelentkeztek a lamotriginnel kezelt betegek 12% -ánál. Míg a bipoláris zavarban szenvedő betegek kontrollált klinikai vizsgálatai során bőrkiütések jelentkeztek a lamotrigint kapó betegek 8% -ánál és a placebót kapó betegek 6% -ánál.
04.9 Túladagolás
Tünetek és jelek
A maximális terápiás dózisnál 10-20-szor nagyobb dózisok akut lenyeléséről számoltak be. A túladagolás olyan tüneteket eredményezett, mint a nystagmus, ataxia, eszméletvesztés és kóma.
Kezelés
Túladagolás esetén a beteget kórházba kell helyezni, és megfelelő támogató terápiát kell alkalmazni. Ha indokolt, el kell végezni a felszívódást csökkentő terápiát (aktív szén). A további kezeléseket klinikailag indokoltnak kell tekinteni. Nincs tapasztalat a hemodialízis túladagolás kezeléséről. Hat önkéntes veseelégtelenségben a lamotrigin 20% -a távozott a szervezetből egy 4 órás hemodialízis során (lásd 5.2 pont).
05.0 FARMAKOLÓGIAI TULAJDONSÁGOK
05.1 Farmakodinámiás tulajdonságok
Farmakoterápiás csoport: egyéb antiepileptikumok, ATC -kód: N03AX09.
A cselekvés mechanizmusa
A farmakológiai vizsgálatok eredményei azt sugallják, hogy a lamotrigin a feszültségfüggő nátriumcsatornák frekvencia- és feszültségfüggő blokkolója. Blokkolja az idegsejtek hosszan ismétlődő kisülését, és gátolja a glutamát (neurotranszmitter, amely kulcsszerepet játszik az epilepsziás rohamok kialakulásában) felszabadulását. Ezek a hatások valószínűleg hozzájárulnak a lamotrigin görcsoldó tulajdonságaihoz.
Ezzel szemben azt a mechanizmust, amellyel a lamotrigin kifejti terápiás hatását bipoláris zavarban, nem állapították meg, bár a kölcsönhatások a feszültségfüggő nátriumcsatornákkal valószínűleg fontosak.
Farmakodinámiás hatások
Az egészséges önkénteseken végzett, a gyógyszer központi idegrendszerre gyakorolt hatásának értékelésére végzett vizsgálatokban a 240 mg lamotrigin adaggal egészséges önkénteseknél kapott eredmények nem különböztek a placebóval kapott eredményektől, míg 1000 mg fenitoin és 10 mg mg diazepám csökkentette mindegyiket, szignifikánsan, a finom látás -motoros koordináció és a szemmozgások növelték a test lengését és szubjektív nyugtató hatásokat váltottak ki.
Egy másik vizsgálatban a 600 mg -os karbamazepin egyszeri szájon át adott dózisa jelentősen csökkentette a finom látás -motoros koordinációt és a szemmozgásokat, fokozta a test lengését és a pulzusszámot, míg a 150 mg -os és 300 mg -os lamotrigin -kezelés eredményei nem különböztek a placebótól.
Klinikai hatásosság és biztonságosság 1–24 hónapos gyermekeknél
A részleges rohamok kiegészítő terápiájának hatékonyságát és biztonságosságát 1–24 hónapos betegeknél egy kis, kettős-vak, placebo-kontrollos elvonási vizsgálatban értékelték. A kezelést 177 alanynál kezdték, akiknek a dózisa hasonló volt a gyermekek adagolásához. 2-12. A 2 mg lamotrigin tabletta a rendelkezésre álló legalacsonyabb dózis, következésképpen a szokásos adagolási rendet bizonyos esetekben a titrálási fázis során módosították (pl. Egy tabletta beadása). 2 mg minden második napon, ha a számított adag 2 mg -nál kisebb volt ) A szérumszintet a titrálás 2. hetének végén mérték, és a következő adagot csökkentették vagy nem növelték, ha a koncentráció egyidejűleg meghaladta a felnőtteknél várt 0,41 μg / ml koncentrációt. Egyes betegeknél az adagot csökkenteni kellett a második hét végén 90% -ig. válaszadók (a rohamok gyakoriságának csökkenése> 40%) randomizáltak placebóra vagy folytatott lamotriginre. A kezelésben sikertelen alanyok aránya a placebo csoportban 84% (16/19 alany), a lamotrigin karon 58% (11/19 alany) volt. A különbség nem volt statisztikailag szignifikáns: 26,3%, CI 95% - 2,6% 50,2%, p = 0,07.
Összesen 256 1-24 hónapos alany volt kitéve lamotrigin 1-15 mg / kg / nap dózisban legfeljebb 72 hétig. A lamotrigin biztonságossági profilja 1 hónap és 2 év közötti gyermekeknél hasonló volt az idősebb gyermekekéhez, kivéve a rohamok klinikailag jelentős súlyosbodását (> = 50%), amelyeket gyakrabban jelentettek 2 évesnél fiatalabb gyermekeknél. %) az idősebb gyermekekhez képest (14%).
Klinikai hatékonyság és biztonság Lennox-Gastaut szindrómában
Nincsenek adatok a Lennox-Gastaut-szindrómával összefüggő rohamok monoterápiájáról.
Klinikai hatékonyság a hangulat epizódok megelőzésében bipoláris zavarban szenvedő betegeknél.
A lamotrigin hatékonyságát a hangulat epizódok megelőzésében I bipoláris zavarban szenvedő betegeknél két vizsgálatban értékelték.
Az SCAB2003 vizsgálat egy randomizált, kettős vak, kettős próbabábu, placebo és lítium, randomizált, többközpontú vizsgálat, amely a lamotrigin fix dózisát értékelte a depresszió és / vagy mánia relapszusainak és kiújulásának hosszú távú megelőzésében. Olyan rendellenesség, akinek nemrégiben volt vagy jelenleg súlyos depressziós epizódja van. A lamotrigin monoterápiával vagy kombinációs terápiával stabilizálódott betegeket az alábbi öt kezelési csoport egyikébe randomizálták: lamotrigin (50, 200, 400 mg / nap), lítium (szérumszint 0,8-1, 1 mmol / l) vagy placebo legfeljebb 76 hét (18 hónap).
L "végpont elsődleges volt a "hangulatzavar beavatkozásáig" eltelt időIdeje az intervencióhoz egy hangulatos epizódhoz": TIME), azaz a beavatkozás kiegészítő farmakoterápiát vagy elektrokonvulzív terápiát jelent. Az SCAB2006 vizsgálat hasonló felépítésű, mint az SCAB2003 vizsgálaté, de eltért az utóbbitól" a rugalmas dózisú (100-400 mg / nap) lamotrigin értékeléséhez ), valamint azoknak a bipoláris I. rendellenességben szenvedő betegeknek a bevonására, akiknek a közelmúltban vagy jelenleg mániás epizódja volt. Az eredményeket a 7. táblázat tartalmazza.
7. táblázat: A lamotrigin hatékonyságát a hangulat epizódok megelőzésében értékelő vizsgálatok eredményeinek összefoglalása I bipoláris zavarban szenvedő betegeknél
Az első depressziós epizódig és az első mániás / hipomániás vagy vegyes epizódig eltelt idő alátámasztó elemzéseiben a lamotriginnel kezelt betegeknél az első depressziós epizódig eltelt idő szignifikánsan hosszabb volt, mint a placebóval kezelt betegeknél, és a kezelések közötti különbségek a mániás / a hipomán vagy vegyes epizódok nem voltak statisztikailag szignifikánsak.
A lamotrigin és a hangulat -stabilizátorok kombinációjának hatékonyságát nem vizsgálták megfelelően.
A lamotrigin szívvezetésre gyakorolt hatásának vizsgálata
Egy egészséges, felnőtt önkénteseken végzett vizsgálat értékelte a lamotrigin (legfeljebb 400 mg / nap) ismételt adagjának a szívvezetésre gyakorolt hatását, 12 elvezetéses EKG-val mérve. A lamotrigin klinikailag jelentős hatása nem volt a QT intervallumra. .
05.2 Farmakokinetikai tulajdonságok
Abszorpció
A lamotrigin gyorsan és teljes mértékben felszívódik a bélből, jelentéktelen first pass metabolizmussal. A plazma csúcskoncentrációja körülbelül 2,5 órával a lamotrigin szájon át történő beadása után jelentkezik. A csúcskoncentráció eléréséhez szükséges idő kissé késik az étkezés után, de a felszívódott mennyiség nincs hatással jelentős egyének közötti eltérések a csúcskoncentrációkban egyensúlyi állapotban, de az egyedi koncentrációk ritkán változnak.
terjesztés
A plazmafehérjékhez való kötődés körülbelül 55%; a plazmafehérjékből való kiszorulás nagyon valószínűtlen, hogy toxikus hatásokat okozna.
Az eloszlási térfogat 0,92-1,22 l / kg.
Anyagcsere
A lamotrigin metabolizmusáért felelős enzimeket azonosították az UDP-glükuronil-transzferázokban.
A lamotrigin szerény mértékben, dózisfüggő mértékben indukálja saját metabolizmusát. Nincs azonban bizonyíték arra, hogy a lamotrigin módosítaná más epilepszia elleni gyógyszerek farmakokinetikáját, és a rendelkezésre álló adatok arra utalnak, hogy a lamotrigin és a citokróm P450 enzimek által metabolizált gyógyszerek közötti kölcsönhatások nem valószínűek.
Kiküszöbölés
Ott tisztítás A látszólagos plazmakoncentráció egészséges egyénekben körülbelül 30 ml / perc. Ott tisztítás A lamotrigin metabolizmusa elsősorban metabolikus, ezt követően a glükurononnal konjugált metabolit kiválasztódik a vizelettel. Kevesebb mint 10% -a ürül változatlan formában a vizelettel. A lamotrigin és metabolitjai csak körülbelül 2% -a ürül a széklettel. Ott tisztítás és a felezési idő független a dózistól. A plazma látszólagos felezési ideje egészséges személyeknél körülbelül 33 óra (hatótávolság 14-103 óra). Egy Gilbert -szindrómás alanyokkal végzett vizsgálatban a tisztítás a látszólagos átlag 32% -kal csökkent a normál kontrollokhoz képest, de az értékek a hatótávolság az általános népességhez képest.
A lamotrigin felezési idejét jelentősen befolyásolja az egyidejű kezelés.
Ha glükuronidációt kiváltó gyógyszerekkel, például karbamazepinnel és fenitoinnal együtt adják, az átlagos felezési idő körülbelül 14 órára csökken, míg önmagában valproáttal kombinálva a felezési idő átlagosan körülbelül 70 órára nő (lásd 4.2 pont).
Linearitás
A lamotrigin farmakokinetikája lineáris 450 mg -ig, a legnagyobb vizsgált egyszeri adagig.
Speciális betegpopulációk
Gyermekek
Ott tisztítás, testtömeghez igazítva magasabb a gyermekeknél, mint a felnőtteknél, a legmagasabb értékeket az öt év alatti gyermekeknél találják. A lamotrigin felezési ideje gyermekeknél általában rövidebb, mint felnőtteknél, átlagos értéke körülbelül 7 óra, ha metabolizáló enzimet indukáló gyógyszerekkel, például karbamazepinnel és fenitoinnal együtt adják, és 45-50 csak valproáttal együtt (lásd 4.2 pont).
2-26 hónapos gyermekek
143 2-26 hónapos, 3-16 kg súlyú gyermekbetegen a tisztítás csökkent az azonos testtömegű idősebb gyermekekhez képest, akik a 2 évesnél idősebb gyermekekéhez hasonló orális adagokat kaptak testtömegkilogrammonként. Az átlagos felezési időt 23 órára becsülték enziminduktor-terápiát kapó, 26 hónaposnál fiatalabb gyermekeknél, 136 órát valproáttal együtt adva és 38 órát azoknál az alanyoknál, akiket enzimgátlók / induktorok nélkül kezeltek. tisztítás magas volt a 2-26 hónapos gyermekcsoportban (47%). A 2-26 hónapos csecsemők várható szérumkoncentrációs szintje általában ugyanabban a tartományban volt, mint az idősebb csecsemőké, bár magasabb Cmax -szintek valószínűleg megfigyelhetők egyes 10 kg alatti testtömegű csecsemőknél.
Idős államporgárok
Az azonos klinikai vizsgálatokba bevont, epilepsziás fiatal és idős betegek bevonásával végzett populációs farmakokinetikai elemzés eredményei azt mutatták, hogy a tisztítás a lamotrigin szintje nem változott klinikailag releváns szinten. A lamotrigin egyszeri adagja után a tisztítás 12%-kal, 20 éves korban 35 ml / percről 70 évre 31 ml / percre csökkent. 48 hetes kezelés után a csökkenés 10%volt, 41 -ről 37 ml / percre. Ezen kívül a A lamotrigint 12 egészséges idős alanyon vizsgálták, egyszeri 150 mg -os lamotrigin adag beadását követően. tisztítás átlag időseknél (0,39 ml / perc / kg) az hatótávolság átlagos értékeinek tisztítás (0,31–0,65 ml / perc / kg), kilenc vizsgálatban, nem idős felnőtteken, 30–450 mg egyszeri dózisokat követően.
Vesekárosodás
Egyetlen 100 mg -os lamotrigin adagot adtak be tizenkét krónikus veseelégtelenségben szenvedő önkéntesnek és hat másik hemodialízis alatt álló alanynak. Ott tisztítás átlagosan 0,42 ml / perc / kg (krónikus veseelégtelenségben), 0,33 ml / perc / kg (a hemodialízis között) és 1,57 ml / perc / kg (hemodialízis során) volt, összehasonlítva 0,58 ml / perc / kg értékkel egészséges önkénteseknél. Az átlagos plazma felezési idő 42,9 óra (krónikus veseelégtelenségben), 57,4 óra (hemodialízis között) és 13,0 óra (hemodialízis során) volt, szemben az egészséges önkéntesek 26,2 órájával. Átlagosan körülbelül 20% (hatótávolság = 5,6-35,1) a szervezetben lévő lamotrigin mennyisége 4 órás hemodialízis során eliminálódott. Ebben a betegpopulációban a lamotrigin kezdő adagját a betegnek egyidejűleg adott gyógyszerekre kell alapozni; csökkentett fenntartó dózisok hatékonyak lehetnek szignifikánsan csökkent veseműködésű betegek (lásd 4.2 és 4.4 pont).
Májkárosodás
Egyetlen dózisú farmakokinetikai vizsgálatot végeztek 24, különböző fokú májkárosodásban szenvedő alanyon és 12 egészséges alanyon kontrollként. A mediánja a tisztítás a látszólagos lamotrigin 0,31; 0,24 vagy 0,10 ml / perc / kg az A, B vagy C fokozatú (Child-Pugh besorolás) májkárosodásban szenvedő betegeknél, míg az egészséges kontrollokban 0,34 ml / perc / kg. A közepes vagy súlyos májkárosodásban szenvedő betegeknél a kezdeti, növekvő és fenntartó adagokat általában csökkenteni kell (lásd 4.2 pont).
05.3 A preklinikai biztonságossági adatok
A farmakológiai biztonságossági vizsgálatok, az ismételt dózisú toxicitás, a genotoxicitás és a karcinogén potenciál alapján a nem klinikai adatok nem mutatnak különösebb kockázatot az emberekre.
A rágcsálókon és nyulakon végzett reprodukciós és fejlődési toxicitási vizsgálatokban nem észleltek teratogén hatásokat, de csökkent magzati súly és késleltetett csontcsontosodás volt megfigyelhető a klinikai expozíciótól elvártnál alacsonyabb vagy ahhoz hasonló expozíciós szinteknél. Mivel az anyai toxicitás súlyossága miatt magasabb expozíciós szinteket állatokon nem lehet vizsgálni, a lamotrigin teratogén potenciálját nem igazolták a klinikai expozíciót meghaladó szinteken.
Patkányokban megnövekedett magzati és posztnatális mortalitást figyeltek meg, amikor lamotrigint adtak a terhesség végén és a korai posztnatális időszakban, és ezeket a hatásokat a várt klinikai expozíciós szinteken figyelték meg.
Fiatalkorú patkányoknál a Biel labirintus tesztben a tanulásra gyakorolt hatást, a balano-preputális elválasztás és a hüvelyi átjárhatóság enyhe késését, az F1-es állatok szülés utáni testsúlyának csökkenését figyelték meg a terápiás érték kétszeresénél nagyobb expozíciós szinteknél a felnőtt férfiban.
Az állatkísérletek nem mutatták ki a lamotrigin miatti termékenységi károsodást. A lamotrigin csökkentette a magzati folsavszintet patkányokban.
A lamotrigin a humán embrionális vesesejtek dózisfüggő gátlását okozta a hERG csatornákban. Az IC50 körülbelül kilencszerese volt a maximális terápiás szabad koncentrációnak. A lamotrigin nem okoz QT -megnyúlást állatokban a maximális szabad terápiás koncentráció körülbelül kétszeresének megfelelő expozíciós szinteken.
06.0 GYÓGYSZERÉSZETI INFORMÁCIÓK
06.1 Segédanyagok
Kálcium-karbonát
Alacsony szubsztitúciójú hidroxi-propil-cellulóz
Magnézium és alumínium -szilikát
Nátrium -keményítő -glikolát (A típus)
Povidone K30
Nátrium -szacharin
Magnézium-sztearát
Fekete ribizli illata.
06.2 Inkompatibilitás
Nem releváns.
06.3 Érvényességi idő
Három év.
06.4 Különleges tárolási előírások
Ez a gyógyszer nem igényel különleges tárolási körülményeket.
06.5 A közvetlen csomagolás jellege és a csomag tartalma
5 mg diszpergálódó / rágótabletta:
PVC / PVdC / alumínium buborékcsomagolás.
10, 14, 28, 30, 50 vagy 56 db diszpergálható / rágótablettát tartalmazó csomagolás
25 mg diszpergálódó / rágótabletta:
PVC / PVdC / alumínium buborékcsomagolás.
10, 14, 21, 28, 30, 42, 50, 56 vagy 60 db diszpergálható / rágótablettát tartalmazó csomagolás.
21 vagy 42 diszpergálható / rágótablettát tartalmazó kezdőcsomag.
50 mg diszpergálódó / rágótabletta:
PVC / PVdC / alumínium buborékcsomagolás.
10, 14, 30, 42, 50, 56, 60, 90, 100 vagy 200 db diszpergálható / rágótablettát tartalmazó csomagolás.
Kezdőcsomag 42 diszpergálható / rágótablettával.
100 mg diszpergálódó / rágótabletta:
PVC / PVdC / alumínium buborékcsomagolás.
Kiszerelés: 10, 30, 50, 56, 60, 90, 100 vagy 200 diszpergálható / rágótabletta.
200 mg diszpergálódó / rágótabletta:
PVC / PVdC / alumínium buborékcsomagolás.
Kiszerelés: 10, 30, 50, 56, 60, 90, 100 vagy 200 diszpergálható / rágótabletta.
Nem feltétlenül mindegyik kiszerelés kerül kereskedelmi forgalomba.
06.6 Használati utasítás
Nincsenek speciális utasítások.
07.0 FORGALOMBA HOZATALI ENGEDÉLY
GlaxoSmithKline S.p.A. - Via A. Fleming, 2 - Verona
08.0 A FORGALOMBA HOZATALI ENGEDÉLY SZÁMA
Lamictal 5 mg diszpergálódó / rágótabletta - 28 A.I.C. 027807066
Lamictal 25 mg diszpergálódó / rágótabletta - 28 A.I.C. 027807054
Lamictal 50 mg diszpergálódó / rágótabletta - 56 A.I.C. 027807080
Lamictal 100 mg diszpergálódó / rágótabletta - 56 A.I.C. 027807078
Lamictal 200 mg diszpergálódó / rágótabletta - 56 A.I.C. 027807092
Lamictal 25 mg diszpergálódó / rágótabletta - kezdőcsomagolás 21 tabletta
diszpergálható kezdőcsomagok kiegészítő kezeléshez valproáttal A.I.C. 027807142
Lamictal 25 mg diszpergálódó / rágótabletta - kezdőcsomag 42 diszpergálódó tabletta kezdőcsomag monoterápiához A.I.C. 027807130
Lamictal 50 mg diszpergálódó / rágótabletta - kezdőcsomag 42 diszpergálódó tabletta kezdőcsomag kiegészítő kezeléshez valproát nélkül A.I.C. 027807155
09.0 Az első forgalomba hozatali engedély engedélyezésének vagy megújításának dátuma
LAMICTAL diszpergálódó / rágótabletta 5 mg, 25 mg, 50 mg, 100 mg, 200 mg: 1998. március 31. / 2011. április 21.
LAMICTAL diszpergálódó / rágótabletta 25 mg, 50 mg kezdőcsomagolás: 2000. január 17. és 2011. április 21.
10.0 A SZÖVEG FELÜLVIZSGÁLÁSÁNAK DÁTUMA
2012. január 25