Hatóanyagok: Brimonidina (Brimonidina tartrato), Timolol
COMBIGAN® 2 mg / ml + 5 mg / ml szemcsepp, oldat
Indikációk Miért használják a Combigan -t? Mire való?
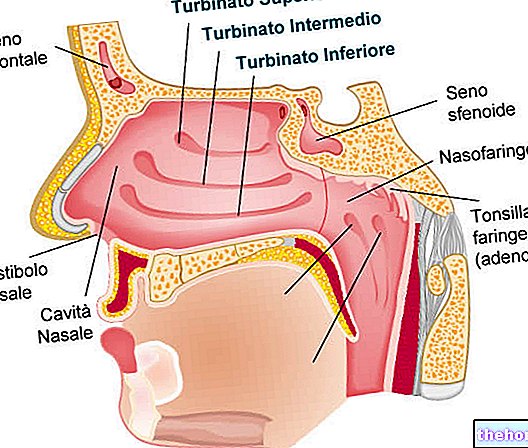
A COMBIGAN egy szemcsepp a glaukóma kezelésére. Két különböző hatóanyagot tartalmaz, brimonidint és timololt: mindkettő csökkenti a szem belsejében lévő magas nyomást. A brimonidin az alfa-2-adrenerg receptor agonistáknak nevezett gyógyszerek csoportjába tartozik. A timolol a béta-blokkolóknak nevezett gyógyszerek csoportjába tartozik. A COMBIGAN-t a szem magas nyomásának csökkentésére írják fel, amikor a béta-blokkoló szemcsepp önmagában nem elegendő.
A szem tiszta vizes folyadékot tartalmaz, amely elősegíti a szem tápanyagainak szállítását. Ezt a folyadékot folyamatosan eltávolítják a szemből, és új folyadékot állítanak elő az eltávolított szem helyett. A COMBIGAN úgy működik, hogy csökkenti a folyadékképződést és növeli az eltávolított folyadék mennyiségét. Ez csökkenti a szem belsejében lévő nyomást, miközben fenntartja a szem tápanyagszállító funkcióját.
Ellenjavallatok Amikor a Combigan -t nem szabad használni
Ne alkalmazza a COMBIGAN szemcseppet, oldatot:
- ha allergiás (túlérzékeny) a brimonidin -tartarátra, a timolra, a béta -blokkolókra vagy a gyógyszer egyéb összetevőjére. Az allergiás reakció tünetei lehetnek az arc, az ajkak és a torok duzzanata, zihálás, ájulásérzés, légszomj, viszketés vagy bőrpír a szem körül.
- - ha légzési problémái vannak, vagy szenvedtek, például asztma, vagy ha súlyos krónikus obstruktív tüdőbetegsége van (súlyos tüdőbetegség, amely légszomjat, légzési nehézséget és / vagy tartós köhögést okozhat)
- ha szívproblémái vannak, például lassú szívverés, szívelégtelenség vagy zavart szívverés (kivéve, ha pacemaker szabályozza)
- ha monoamin -oxidáz (MAO) inhibitorokat vagy más antidepresszáns gyógyszereket szed.
A COMBIGAN nem alkalmazható 2 év alatti gyermekeknél, és általában 2 és 17 év közötti gyermekeknél.
Ha úgy gondolja, hogy a fenti pontok bármelyike vonatkozik Önre, ne használja a COMBIGAN -t, amíg újra nem konzultált orvosával.
Azok számára, akik sporttevékenységet folytatnak: a gyógyszer terápiás szükségtelen használata doppingnak minősül, és mindenesetre pozitív doppingellenes tesztet eredményezhet.
Az alkalmazással kapcsolatos óvintézkedések Mit kell tudnia a Combigan szedése előtt
A COMBIGAN alkalmazása előtt beszéljen kezelőorvosával
- ha van vagy volt:
- szívkoszorúér -problémák által okozott szívbetegség (a tünetek közé tartozhat a mellkasi fájdalom vagy feszültség, légszomj vagy fulladás), szívelégtelenség, alacsony vérnyomás
- szívritmuszavarok, például lassú szívverés
- légzési problémák, asztma vagy krónikus obstruktív tüdőbetegség
- károsodott vérkeringés miatti állapotok (például Raynaud -kór vagy Raynaud -szindróma)
- cukorbetegség, mivel a timolol elfedheti az alacsony vércukorszint jeleit és tüneteit
- a pajzsmirigy túlzott aktivitása, mivel a timolol elfedheti a pajzsmirigy -betegség jeleit és tüneteit
- máj- vagy veseproblémák
- mellékvese daganat
- a szem operatív beavatkozásai a szemnyomás csökkentése érdekében
- ha allergiája (például szénanátha, ekcéma) vagy súlyos allergiás reakciója van vagy volt, tudnia kell, hogy a súlyos reakciók kezelésére használt szokásos adrenalin -adagot növelni kell.
- A műtét előtt tájékoztassa kezelőorvosát arról, hogy COMBIGAN -t használ, mivel a timolol megváltoztathatja néhány érzéstelenítés során alkalmazott gyógyszer hatását.
Kölcsönhatások Mely gyógyszerek vagy élelmiszerek módosíthatják a Combigan hatását
A COMBIGAN befolyásolhatja vagy befolyásolhatja más gyógyszerek szedése, beleértve a glaukóma kezelésére szolgáló egyéb szemcseppeket is. Feltétlenül tájékoztassa kezelőorvosát vagy gyógyszerészét a jelenleg vagy nemrégiben szedett, valamint szedni tervezett egyéb gyógyszereiről, beleértve a bármilyen betegség gyógyszereit is, még akkor is, ha nem kapcsolódnak a szem rendellenességéhez, beleértve a vény nélkül kapható gyógyszereket is. Vannak olyan gyógyszerek, amelyek befolyásolhatják a COMBIGAN hatását, ezért különösen fontos, hogy tájékoztassa kezelőorvosát, ha szedi:
- fájdalomcsillapítók
- álmatlanság vagy szorongás elleni gyógyszerek
- magas vérnyomás (magas vérnyomás) kezelésére szolgáló gyógyszerek
- szívproblémák (pl. szabálytalan szívverés) kezelésére szolgáló gyógyszerek, például béta -blokkolók, digoxin vagy kinidin (szívbetegségek és bizonyos típusú malária kezelésére használják)
- a cukorbetegség kezelésére vagy a vércukorszint szabályozására szolgáló gyógyszerek
- depresszió elleni gyógyszerek, például fluoxetin és paroxetin
- egyéb szemcseppek a szem magas nyomásának (glaukóma) csökkentésére
- súlyos allergiás reakciók kezelésére szolgáló gyógyszerek
- a hormonokat befolyásoló gyógyszerek, például az adrenalin és a dopamin
- az érizmokat befolyásoló gyógyszerek
- gyomorégés vagy gyomorfekély kezelésére szolgáló gyógyszerek.
Ha megváltoztatta bármelyik jelenleg alkalmazott gyógyszer adagját, vagy rendszeresen fogyaszt alkoholt, kérjük, tájékoztassa kezelőorvosát.
Ha érzéstelenítőre van szüksége, mondja el orvosának vagy fogorvosának, hogy COMBIGAN -t használ.
Figyelmeztetések Fontos tudni, hogy:
Terhesség és szoptatás
Ha Ön terhes vagy szoptat, illetve ha fennáll Önnél a terhesség lehetősége vagy gyermeket szeretne, a gyógyszer alkalmazása előtt beszéljen kezelőorvosával vagy gyógyszerészével.
Ne használja a COMBIGAN -t, ha terhes, kivéve, ha orvosa szükségesnek tartja.
Ne használja a COMBIGAN -t, ha szoptat. A timolol bejuthat a tejbe. Kérjen tanácsot orvosától, mielőtt bármilyen gyógyszert szoptatás alatt szed.
A készítmény hatásai a gépjárművezetéshez és gépek kezeléséhez szükséges képességekre
Néhány betegnél a COMBIGAN álmosságot, fáradtságot vagy homályos látást okozhat. Ne vezessen gépjárművet és ne kezeljen gépeket, amíg a tünetek nem szűnnek meg. Ha bármilyen egyéb problémája van, kérjük, jelezze orvosának.
Fontos információk a COMBIGAN kontaktlencsék egyes összetevőiről
- Ne használja a COMBIGAN -t kontaktlencsék viselése közben. Várjon legalább 15 percet a COMBIGAN bevétele után, mielőtt visszahelyezi lencséit.
- A COMBIGAN -ban található tartósítószer (benzalkonium -klorid) szemirritációt okozhat, és ismert, hogy elszínezi a lágy kontaktlencséket.
Adagolás és alkalmazás A Combigan alkalmazásának módja: Adagolás
Ezt a gyógyszert mindig pontosan az orvos által elmondottaknak megfelelően alkalmazza. Ha kétségei vannak, forduljon orvosához vagy gyógyszerészéhez. A COMBIGAN nem adható 2 év alatti gyermekeknek. A COMBIGAN alkalmazása gyermekeknél és serdülőknél (2-17 éves) nem ajánlott.
Az ajánlott adag egy csepp COMBIGAN naponta kétszer, körülbelül 12 órás különbséggel. Ne változtassa meg az adagot, és ne hagyja abba a készítmény alkalmazását anélkül, hogy orvosával konzultálna.
Ha a COMBIGAN -t más szemcseppekkel együtt használja, tartson legalább 5 percet a COMBIGAN bevétele és a többi szemcsepp bevétele között.
Használati útmutató
Ne használja a palackot, ha használat előtt nem sérült a kupakon lévő garanciapecsét.
Mosson kezet a palack kinyitása előtt. Hátrahajtod a fejed, és felnézsz.
- Lassan az alsó szemhéjat úgy, hogy kis zsebet képezzen.
- Fordítsa fejjel lefelé az üveget, és enyhe nyomással engedje el a csepp szemcseppeket minden kezelendő szemhez.
- Engedje el az alsó szemét, és tartsa csukva a szemét.
- Tartsa csukva a szemét, és nyomja a mutatóujját a szem sarkához (ahhoz az oldalhoz, ahol a szem találkozik az orrával) két percig. Ez segít megelőzni, hogy a COMBIGAN a test többi részébe kerüljön.
Ha a csepp nem kerül a szembe, ismételje meg a műveletet.
A szennyeződés elkerülése érdekében a palack hegye ne érjen a szeméhez, és ne érintkezzen más felülettel.A gyógyszer használata után zárja le szorosan az üveget a kupak visszacsavarásával.
Ha elfelejtette alkalmazni a COMBIGAN -t
Ha elfelejtette alkalmazni a COMBIGAN -t, amint eszébe jut, tegyen egy cseppet a kezelendő szembe, majd térjen vissza a szokásos adagolási időhöz.Ne használjon kétszeres adagot a kihagyott adag pótlására.
Ha idő előtt abbahagyja a COMBIGAN szedését
A megfelelő működés érdekében a COMBIGAN -t minden nap használni kell.
Ha bármilyen további kérdése van a COMBIGAN alkalmazásával kapcsolatban, kérdezze meg kezelőorvosát vagy gyógyszerészét.
Túladagolás Mi a teendő, ha túl sok Combigan -t vett be?
Felnőttek
Ha az előírtnál több COMBIGAN -t csepegtetett be, ez valószínűleg nem okoz súlyos következményeket. A következő adagot a szokásos időben adja be. Ha ez aggasztja, forduljon orvosához vagy gyógyszerészéhez.
Csecsemők és gyermekek
Számos túladagolásról számoltak be csecsemőknél és gyermekeknél, akik a glaukóma gyógyszeres kezelésének részeként szedtek brimonidint (a COMBIGAN egyik hatóanyaga). A túladagolás tünetei: álmosság, lassúság, alacsony testhőmérséklet, sápadtság és légzés nehézségek Ha ezen mellékhatások bármelyike jelentkezik, azonnal forduljon orvosához.
Felnőttek és gyermekek
Ha a COMBIGAN -t véletlenül lenyelte, azonnal forduljon orvosához.
Mellékhatások Melyek a Combigan mellékhatásai?
Mint minden gyógyszer, így ez a gyógyszer is okozhat mellékhatásokat, amelyek azonban nem mindenkinél jelentkeznek.
Ha az alábbi mellékhatások bármelyikét észleli, azonnal forduljon orvosához:
- Szívelégtelenség (például mellkasi fájdalom) vagy szabálytalan szívverés
- A pulzusszám növekedése vagy csökkenése vagy a vérnyomás csökkenése
Szembetegségek
Nagyon gyakori (10 beteg közül több mint 1 beteget érinthet):
- A szem vörössége vagy égő
Gyakori (10 beteg közül legfeljebb 1 beteget érinthet):
- Csípő érzés vagy fájdalom a szemben
- Allergiás reakció a szemben vagy a szem körüli bőrön
- Kis repedések a szem felszínén (gyulladással vagy anélkül)
- A szemhéj duzzanata, vörössége és gyulladása
- Irritáció vagy idegen test érzése a szemben
- A szem és a szemhéj viszketése
- Tüszők vagy fehér pontok a szemréteget borító vizuális rétegen
- Látási zavarok
- Tépés
- Száraz szem
- Ragadós szemek
Nem gyakori (100 beteg közül legfeljebb 1 beteget érinthet):
- Nehézség tisztán látni
- A szem felszínét borító vizuális réteg duzzanata vagy gyulladása
- Fáradt szemek
- Fényérzékenység
- Fájdalom a szemhéjban
- A szem felületét borító vizuális réteg fehérítése
- Duzzanat vagy gyulladásos területek a szem felszíne alatt
- Lebegő formák a szem előtt
Nem ismert (a gyakoriság a rendelkezésre álló adatokból nem állapítható meg):
- homályos látás
Rendellenességek a testben:
Gyakori (10 beteg közül legfeljebb 1 beteget érinthet):
- Magas vérnyomás
- Depresszió
- Álmosság
- Fejfájás
- Száraz száj
- Általános gyengeség
Nem gyakori (100 beteg közül legfeljebb 1 beteget érinthet):
- Szív elégtelenség
- Szabálytalan szívverés
- Könnyelmű érzés
- Halvány érzés
- Az orr kiszáradása
- Az íz megváltoztatása
- Hányinger
- Hasmenés
Nem ismert (a gyakoriság a rendelkezésre álló adatokból nem állapítható meg):
- Fokozott vagy lelassult pulzusszám
- Alacsony vérnyomás
- Az arc vörössége
Ezen hatások némelyike az összetevők bármelyikének allergiájából adódhat.
További mellékhatásokat észleltek olyan betegeknél, akik brimonidint vagy timololt tartalmazó szemcseppeket használtak, és ezért valószínűleg a COMBIGAN -nal együtt is előfordulnak.
A brimonidin alkalmazása során a következő további mellékhatásokat figyelték meg:
- gyulladás a szem belsejében, a pupillák beszűkülése, álmatlanság, hideg érzés, légszomj, a gyomorral és az emésztéssel kapcsolatos tünetek, általános allergiás reakciók, bőrreakciók, beleértve a bőrpírt, az arc duzzanatát, viszkető kiütéseket és az erek kiszélesedését.
Más szemre alkalmazott gyógyszerekhez hasonlóan a COMBIGAN (brimonidin / timolol) felszívódik a vérbe. A COMBIGAN béta-blokkolójának, a timololnak a felszívódása hasonló mellékhatásokat okozhat, mint az "intravénás" és / vagy "orális" béta-blokkolóknál. A nemkívánatos hatások gyakorisága a helyi szemészeti alkalmazás után alacsonyabb, mint az alkalmazásból adódóan gyógyszerek, például szájon át vagy injekció formájában.
A felsorolt mellékhatások közé tartoznak a szembetegségek kezelésére használt béta-blokkolók osztályával kapcsolatban észlelt reakciók:
- Általános allergiás reakciók, beleértve a bőr alatti duzzanatot (amely olyan területeken fordulhat elő, mint az arc és a végtagok, és elzárhatja a légutakat, ami nyelési vagy légzési nehézséget okozhat), csalánkiütés (vagy viszkető kiütés), lokalizált és általános kiütés, viszketés, hirtelen fellépő súlyos allergiás reakció, amely életveszélyes
- Alacsony vércukorszint
- Alvászavarok (álmatlanság), rémálmok, memóriavesztés
- Stroke, csökkent agyi véráramlás, fokozott myasthenia gravis (izomzavarok) jelei és tünetei, szokatlan érzések (például bizsergés vagy zsibbadás)
- A szaruhártya gyulladása, a retina alatti réteg leválása, amely vérereket tartalmaz szűrőműtét után, ami látászavarokat okozhat, csökkent szaruhártya -érzékenység, szaruhártya -erózió (a szemgolyó homlokrétegének károsodása), a felső szemhéj leesése (ami a szem felének lezárása), kettős látás
- Mellkasi fájdalom, ödéma (folyadékgyülem), a szívverés ritmusának vagy sebességének megváltozása, egyfajta szívritmuszavar, szívroham, szívelégtelenség
- Raynaud -jelenség, hideg kezek és lábak
- A tüdő légútjainak összehúzódása (különösen a már meglévő betegségben szenvedő betegeknél), légzési nehézség, köhögés
- Emésztési zavarok, hasi fájdalom, hányás
- Hajhullás, ezüstfehér bőrkiütés (pikkelysömör alakú kiütés) vagy a pikkelysömör súlyosbodása, bőrkiütés
- Izomfájdalom, amelyet nem a testmozgás okoz
- Szexuális diszfunkció, csökkent szexuális vágy
- Izomgyengeség / fáradtság.
A foszfátokat tartalmazó szemcseppek alkalmazásakor jelentett egyéb mellékhatások:
Nagyon ritkán azoknál a betegeknél, akik súlyos sérülést szenvedtek a szem elülső részén (szaruhártya) lévő tiszta membránon, a kezelés során a kalcium felhalmozódása miatt átlátszatlan foltok alakultak ki a szaruhártyán.
Mellékhatások bejelentése
Ha Önnél bármilyen mellékhatás jelentkezik, tájékoztassa erről kezelőorvosát vagy gyógyszerészét. Ez a betegtájékoztatóban fel nem sorolt bármilyen lehetséges mellékhatásra is vonatkozik. A mellékhatásokat közvetlenül a hatóság részére is bejelentheti az V. függelékben található elérhetőségeken keresztül. A mellékhatások bejelentésével Ön is hozzájárulhat ahhoz, hogy minél több információ álljon rendelkezésre a gyógyszer biztonságosságáról.
Lejárat és megőrzés
A gyógyszer gyermekektől elzárva tartandó!
Tartsa a palackot a külső dobozban, hogy megvédje a fénytől.
Egyszerre csak egy üveget használjon.
A palack címkéjén és a dobozon feltüntetett lejárati idő (EXP) után ne alkalmazza ezt a gyógyszert. A lejárati idő a hónap utolsó napjára vonatkozik.
Még ha nem is használta fel az összes oldatot, négy héttel az első felbontás után dobja ki az üveget. Ez segít megelőzni a fertőzéseket. Annak érdekében, hogy ne felejtsük el, a dobozon lévő helyre írja be a kinyitás dátumát.
Semmilyen gyógyszert ne dobjon a szennyvízbe vagy a háztartási hulladékba. Kérdezze meg gyógyszerészét, hogy mit tegyen a már nem használt gyógyszereivel. Ez elősegíti a környezet védelmét.
Egyéb információk
Mit tartalmaz a COMBIGAN?
- A hatóanyagok a brimonidin -tartarát és a timolol.
- Egy milliliter oldat 2 mg brimonidin -tartarátot és 5 mg timololnak megfelelő timolol -maleátot tartalmaz.
- Egyéb összetevők: benzalkónium -klorid (tartósítószer), egybázisú nátrium -foszfát -monohidrát, dinátrium -foszfát -heptahidrát és tisztított víz.
Kis mennyiségű sósavat vagy nátrium -hidroxidot adhatunk hozzá, hogy az oldat a megfelelő pH -értékre jusson (az oldat savasságának vagy lúgosságának mértéke).
A COMBIGAN megjelenésének leírása és a csomagolás
A COMBIGAN tiszta, sárga -zöld szemcsepp oldat csavaros kupakkal ellátott műanyag palackban. Minden palack körülbelül félig tele van, és 5 ml oldatot tartalmaz. 1 vagy 3 palackot tartalmazó csomagolás kapható. Nem feltétlenül mindegyik kiszerelés kerül kereskedelmi forgalomba.
Forrás betegtájékoztató: AIFA (Olasz Gyógyszerügynökség). A tartalom 2016 januárjában jelent meg. A jelenlévő információk nem feltétlenül naprakészek.
A legfrissebb verzióhoz való hozzáféréshez ajánlatos az AIFA (Olasz Gyógyszerügynökség) webhelyét elérni. Jogi nyilatkozat és hasznos információk.
01.0 A GYÓGYSZER MEGNEVEZÉSE
COMBIGAN 2 MG / ML + 5 MG / ML SZEMCSEPPEK, MEGOLDÁS
02.0 MINŐSÉGI ÉS MENNYISÉGI ÖSSZETÉTEL
Egy ml oldat tartalmaz:
2,0 mg brimonidin -tartarát, ami 1,3 mg brimonidinnek felel meg, 5,0 mg timolol, 6,8 mg timolol -maleát formájában
0,05 mg / ml benzalkonium -kloridot tartalmaz.
A segédanyagok teljes listáját lásd a 6.1 pontban.
03.0 GYÓGYSZERFORMA
Szemcseppek, oldat.
Sárga -zöld színű tiszta oldat.
04.0 KLINIKAI INFORMÁCIÓK
04.1 Terápiás javallatok
Az intraokuláris nyomás (IOP) csökkentése krónikus nyitott zugú glaukómában vagy okuláris hipertóniában szenvedő betegeknél, akik nem reagálnak megfelelően a helyi béta-blokkolókra.
04.2 Adagolás és alkalmazás
A szem vagy a szemcsepp szennyeződésének elkerülése érdekében a csepegtető hegye nem érintkezhet semmilyen felülettel.
Ajánlott adagolás felnőtteknél (beleértve az idős betegeket is)
Az ajánlott adag egy csepp Combigan a kezelt szem (ek) be, naponta kétszer, körülbelül 12 óránként. Ha egynél több helyi szemészeti készítményre van szükség, a gyógyszereket legalább 5 perces időközönként kell beadni .
Mint minden szemcsepp esetében, az esetleges szisztémás felszívódás csökkentése érdekében ajánlatos a könnyzsákot összenyomni a középső canthusnál (a könnycsepp elzáródása), vagy két percig le kell zárni a szemhéjakat. Ezt minden csepp szemcsepp csepegtetése után azonnal meg kell tenni, ami a szisztémás mellékhatások csökkenéséhez és a helyi aktivitás növekedéséhez vezethet.
Alkalmazása vese- és májelégtelenségben
A Combigan -t nem vizsgálták máj- vagy veseelégtelenségben szenvedő betegeknél. Ezért óvatosan kell eljárni ezen betegek kezelésében.
Alkalmazása gyermekeknél és serdülőknél
A Combigan ellenjavallt újszülötteknél és (2 évesnél fiatalabb) gyermekeknél (lásd 4.3 pont, Ellenjavallatok, 4.4 pont, Különleges figyelmeztetések és az alkalmazással kapcsolatos óvintézkedések, 4.8 pont Nemkívánatos hatások és 4.9 Túladagolás).
A Combigan biztonságosságát és hatásosságát gyermekeknél és (2-17 éves) serdülőknél nem igazolták, ezért alkalmazása ezeknél az alanyoknál nem javasolt (lásd még 4.4 és 4.8 pont).
04.3 Ellenjavallatok
• Túlérzékenység a hatóanyagokkal vagy bármely segédanyaggal szemben.
• Légúti hiperreaktivitási betegségek, beleértve a jelenlegi vagy korábbi bronchiális asztmát, súlyos krónikus obstruktív tüdőbetegséget.
• Sinus bradycardia, beteg sinus szindróma, sino-pitvari blokk, második vagy harmadik fokú atrioventricularis blokk, amelyet nem szabályoznak pacemakerrel, nyilvánvaló szívelégtelenség, kardiogén sokk.
• Alkalmazása csecsemőknél és (2 évesnél fiatalabb) gyermekeknél (lásd 4.8 pont).
• Monoamin -oxidáz (MAO) inhibitorokkal kezelt betegek.
• A noradrenerg transzmissziót befolyásoló antidepresszánsokat szedő betegek (pl. Triciklusos antidepresszánsok és mianserin).
04.4 Különleges figyelmeztetések és a használathoz szükséges óvintézkedések
A kétéves és idősebb gyermekeket, különösen a 2 és 7 év közötti és / vagy ≤ 20 kg súlyú gyermekeket óvatosan kell kezelni, és gondosan ellenőrizni kell őket az aluszékonyság magas előfordulási gyakorisága és súlyossága miatt. "A Combigan hatékonysága gyermekeknél és serdülőknél (2 17 éves korig) nem bizonyított (lásd 4.2 és 4.8 pont).
A klinikai vizsgálatok során egyes betegek a Combigan -kezelés után szem allergiás reakciókról (allergiás kötőhártya és allergiás blepharitis) számoltak be.
Allergiás kötőhártya -gyulladást a betegek 5,2% -ánál találtak. Általában a reakció a 3. és a 9. hónap között jelentkezett, ami azt eredményezte, hogy a betegek abbahagyásának aránya a betegek 3,1% -a volt. Allergiás blepharitist nem jelentettek gyakran (az allergiás reakciókat a Combigan alkalmazásával abba kell hagyni.
Késleltetett túlérzékenységi reakciókról számoltak be a 0,2% -os brimonidin -tartarát szemészeti oldat bevételét követően, amelyek közül néhány a szemnyomás növekedéséhez kapcsolódik.
Más helyileg alkalmazott szemészeti szerekhez hasonlóan a Combigan szisztémásan is felszívódhat. Nem figyelték meg az egyes hatóanyagok szisztémás felszívódásának növekedését. A béta-adrenerg komponens, a timolol miatt ugyanaz a típusú kardiovaszkuláris, tüdő- és egyéb mellékhatás, mint a béta-szisztémás blokkolóknál. A szisztémás mellékhatások gyakorisága a helyi szemészeti gyógyszerek alkalmazása alacsonyabb, mint a szisztémás alkalmazást követő reakcióké. A szisztémás felszívódás csökkentésére lásd a 4.2 pontot.
Szív patológiák :
A szív- és érrendszeri betegségben (például koszorúér-betegségben, Prinzmetal-anginában és szívelégtelenségben) szenvedő és béta-blokkolókkal végzett hipotenzív kezelésben részesülő betegeket kritikusan értékelni kell, és meg kell fontolni más hatóanyagokkal történő kezelést. A szív- és érrendszeri betegségben szenvedő betegeket figyelemmel kell kísérni ezen állapotok súlyosbodásának jeleire és a nemkívánatos eseményekre.
Mivel negatív hatással van a vezetési időre, a béta-blokkolókat óvatosan kell alkalmazni az első fokú szívblokkban szenvedő betegeknél.
A szisztémás béta-blokkolókhoz hasonlóan, ha a kezelést a koszorúér-betegeknél le kell állítani, ezt fokozatosan kell elvégezni a ritmuszavarok, a szívinfarktus vagy a hirtelen halál elkerülése érdekében.
Érpatológiák :
Súlyos perifériás keringési zavarban / rendellenességben szenvedő betegeket (azaz a Raynaud -jelenség vagy a Raynaud -szindróma előrehaladott formáit) óvatosan kell kezelni.
Légúti patológiák :
Légzőszervi reakciókat, köztük asztmás betegek hörgőgörcs okozta halálát jelentették egyes szemészeti béta-blokkolók beadását követően. A Combigan -t óvatosan kell alkalmazni enyhe / mérsékelt krónikus obstruktív tüdőbetegségben (COPD) szenvedő betegeknél, és csak akkor, ha a várható előny meghaladja a lehetséges kockázatot.
Hipoglikémia / cukorbetegség :
A béta-blokkolókat óvatosan kell alkalmazni spontán hipoglikémiára hajlamos betegeknél vagy instabil cukorbetegeknél, mivel a béta-blokkolók elfedhetik az akut hipoglikémia jeleit és tüneteit.
Hyperthyreosis :
A béta -blokkolók elfedhetik a hyperthyreosis jeleit is.
A Combigan óvatosan alkalmazható metabolikus acidózisban és kezeletlen feokromocitómában szenvedő betegeknél.
A szaruhártya patológiái:
A szemészeti béta-blokkolók szemszárazságot okozhatnak. A szaruhártya -betegségben szenvedő betegeket óvatosan kell kezelni.
Egyéb béta-blokkoló szerek:
Az intraokuláris nyomásra gyakorolt hatás vagy a szisztémás béta-blokkoló ismert hatásai fokozódhatnak, ha timololt adnak azoknak a betegeknek, akiket már szisztémás béta-blokkolóval kezelnek. Ezen betegek válaszát szorosan figyelemmel kell kísérni. blokkoló szerek alkalmazása nem javasolt (lásd 4.5 pont).
Anafilaxiás reakciók:
A béta-blokkolókkal végzett kezelés során azok a betegek, akiknek kórtörténetében atópiát vagy különböző típusú allergének által okozott súlyos anafilaxiás reakciót mutattak, jobban reagálhatnak az ezekkel az allergénekkel történő ismételt stimulációra, és nem reagálnak az általában az anafilaxiás betegség kezelésére használt adrenalin adagra. reakciók.
A koroid leválása:
A koroid leválásáról beszámoltak olyan terápiák alkalmazásával, amelyek csökkentik a vizes humor képződését (pl. Timolol, acetazolamid) szűrőműtéti eljárások után.
Sebészeti érzéstelenítés:
A blokkoló szemészeti készítmények blokkolhatják az a -antagonisták szisztémás hatásait, például az adrenalint. Az aneszteziológust tájékoztatni kell, ha a beteg timololt szed.
A timolol -kezelést súlyos hipotenzióval hozták összefüggésbe dialízis alatt álló súlyos veseelégtelenségben szenvedő betegeknél.
A Combigan tartósítószere, a benzalkonium -klorid szemirritációt okozhat. A kontaktlencsét az instillálás előtt el kell távolítani, és legalább 15 perc múlva újra fel lehet használni.
A benzalkonium -klorid ismerten tompítja a lágy kontaktlencséket. Kerülje a puha kontaktlencsékkel való érintkezést.
A Combigan-t nem vizsgálták keskeny szögű glaukómában szenvedő betegeknél.
A sportolóknak tisztában kell lenniük azzal, hogy a Combigan timololt tartalmaz, ami pozitív eredményhez vezethet a doppingellenőrzésben.
04.5 Kölcsönhatások más gyógyszerekkel és egyéb interakciók
A brimonidin és a timolol fix kombinációjával nem végeztek interakciós vizsgálatokat. Bár a Combigan -nal nem végeztek specifikus interakciós vizsgálatokat, ennek ellenére figyelembe kell venni az additív vagy erősítő hatások lehetőségét, ha központi idegrendszeri depresszánsokkal (alkohol, barbiturátok, opiátok, nyugtatók vagy érzéstelenítők) együtt alkalmazzák.
A béta-blokkolók és az orális kalciumcsatorna-blokkolók, béta-adrenerg blokkoló szerek, antiaritmiás szerek (beleértve az amiodaront), a digitalis glikozidok, a paraszimpatomimetikumok vagy a guanetidin szemészeti oldatainak együttes alkalmazása additív hatásokhoz vezethet, például hipotenzióhoz és / vagy kifejezett bradycardiához. Ezenkívül nagyon ritka eseteket jelentettek (szisztémás vérnyomáscsökkentők.
Esetenként a szemészeti béta-blokkolók és az adrenalin (epinefrin) egyidejű alkalmazásából származó mydriasisról számoltak be.
A béta-blokkolók fokozhatják az antidiabetikumok vércukorszint-csökkentő hatását, és elfedhetik a hipoglikémia jeleit és tüneteit (lásd 4.4 pont).
A klonidin hirtelen abbahagyása által okozott hipertóniás reakció fokozódhat a béta-blokkolók szedése közben.
Fokozott szisztémás béta -receptor blokádról (pl. Csökkent pulzusszám, depresszió) számoltak be a CYP2D6 inhibitorokkal (pl. Kinidin, fluoxetin, paroxetin) és timolollal történő egyidejű kezelés során.
A béta-blokkoló érzéstelenítő szerekkel egyidejű alkalmazása csökkentheti a kompenzációs tachycardiát és növelheti a hipotenzió kockázatát (lásd 4.4 pont), ezért az aneszteziológust tájékoztatni kell, ha a beteget Combigan-nal kezelik.
Óvatosan kell eljárni, ha a Combigan-t jódalapú kontrasztanyaggal vagy intravénás lidokainnal együtt kezelik.
A cimetidin, a hidralazin és az alkohol növelheti a timolol plazmakoncentrációját.
A Combigan beadása után nincs adat a forgalomban lévő katekolaminok szintjéről. Mindazonáltal óvatosság ajánlott azoknál a betegeknél, akik olyan gyógyszereket szednek, amelyek megváltoztathatják a keringő aminok anyagcseréjét és felvételét (pl. Klórpromazin, metilfenidát, rezerpin).
Szintén ajánlott óvatosan eljárni olyan szisztémás gyógyszerekkel való együttes kezelés megkezdésekor (vagy dózismódosítások esetén) (gyógyszerformától függetlenül), amelyek kölcsönhatásba léphetnek az alfa-adrenerg agonistákkal vagy befolyásolhatják azok aktivitását, azaz agonisták vagy adrenerg receptor antagonisták (pl. izoprenalin, prazozin).
Bár a Combigan specifikus gyógyszerkölcsönhatási vizsgálatait nem végezték el, mérlegelni kell az elméleti lehetőségét annak, hogy prosztatamidokkal, prosztaglandinokkal, karboanhidráz inhibitorokkal és pilokarpinnal adható additív szemnyomáscsökkentő hatás.
A brimonidin alkalmazása ellenjavallt azoknál a betegeknél, akik már monoamin -oxidáz (MAO) gátló kezelést kapnak, és olyan betegeknél, akik olyan antidepresszáns kezelésben részesülnek, amelyek hatással vannak a noradrenerg transzmisszióra (pl. Triciklikus antidepresszánsok és mianserin) (lásd 4.3 pont).
Azoknak a betegeknek, akik MAO -gátló kezelést kaptak, a befejezés után 14 napot kell várniuk, mielőtt elkezdik a Combigan -kezelést.
04.6 Terhesség és szoptatás
Terhesség
Nincsenek megfelelő adatok a brimonidin / timolol fix kombináció terhes nőkön történő alkalmazásáról.
A Combigan -t terhesség alatt nem szabad alkalmazni, kivéve, ha egyértelműen szükséges. A szisztémás felszívódás csökkentésére lásd a 4.2 pontot.
Brimonidin -tartarát
Nincsenek megfelelő adatok a brimonidin -tartarát terhes nőkön történő alkalmazásáról.
Timolol
Az állatokon végzett vizsgálatok a klinikai gyakorlatban alkalmazottnál szignifikánsan nagyobb dózisoknál reprodukciós toxicitást mutattak (lásd 5.3 pont). Az epidemiológiai vizsgálatok nem tártak fel rosszindulatú hatásokat, de az intrauterin növekedés késleltetésének kockázatát mutatták ki orális béta-blokkolók alkalmazása során. Ezenkívül a béta-blokád jeleit és tüneteit (pl. Bradycardia, hypotensio, légzési nehézség és hipoglikémia) figyelték meg az újszülöttnél, amikor béta-blokkolót adtak az anyának a szülésig. Ha a Combigan -t terhesség alatt adják be a szülésig, az újszülöttet gondosan ellenőrizni kell az élet első napjaiban.
Etetési idő
Brimonidin -tartarát
Nem ismert, hogy a brimonidin kiválasztódik -e az anyatejbe, de kiválasztódik -e a patkányok anyatejébe.
Timolol
A béta-blokkolók kiválasztódnak az anyatejbe. Azonban a szemcseppekben alkalmazott timolol terápiás dózisa esetén nem valószínű, hogy elegendő mennyiségben van az anyatejben ahhoz, hogy az újszülöttben a béta-blokád klinikai tüneteit előidézze. A szisztémás felszívódás csökkentésére lásd a 4.2 pontot.
Ezért a Combigan -t nem szabad szoptató nőknek használni.
04.7 Hatások a gépjárművezetéshez és gépek kezeléséhez szükséges képességekre
A Combigan kismértékben befolyásolja a gépjárművezetéshez és gépek kezeléséhez szükséges képességeket.
A Combigan átmeneti látásromlást, látászavarokat, fáradtságot és / vagy álmosságot okozhat, ami befolyásolhatja a gépjárművezetéshez és gépek kezeléséhez szükséges képességeket.
04.8 Nemkívánatos hatások
A 12 hónapos klinikai adatok alapján a leggyakrabban jelentett mellékhatások (mellékhatások) a kötőhártya-hiperémia (a betegek kb. 15% -ánál) és a szem égő érzése (a betegek körülbelül 11% -ánál) voltak. Ezen esetek többségében hatásai enyheek voltak, a megszakítás aránya 3,4% -ra, illetve 0,5% -ra korlátozódott.
A Combigan -nal végzett klinikai vizsgálatok során a következő mellékhatásokat jelentették:
Szembetegségek
Nagyon gyakori (> 1/10): kötőhártya -hiperémia, égő.
Gyakori (> 1/100, allergiás kötőhártya -gyulladás, szaruhártya -erózió, felületes pontszerű keratitis, szemi viszketés, kötőhártya -follikulózis, látászavar, blefaritis, epifóra, szemszárazság, szemkisülés, szemfájdalom, szemirritáció, idegen test érzése.
Nem gyakori (> 1/1000, kötőhártya -ödéma, tüsző -kötőhártya -gyulladás, allergiás blefaritis, kötőhártya -gyulladás, légylegyek, aszthenópia, fotofóbia, papilláris hipertrófia, szemhéjfájdalom, kötőhártya -sápadtság, szaruhártya -ödéma, szaruhártya -beszivárgások, üvegtest -leválás.
Pszichiátriai rendellenességek
Gyakori (> 1/100,
Idegrendszeri betegségek
Gyakori (> 1/100, fejfájás.
Nem gyakori (> 1/1000, szédülés, ájulás.
Szív patológiák
Nem gyakori (> 1/1000, szívdobogás.
Érpatológiák
Gyakori (> 1/100,
Légzőrendszeri, mellkasi és mediastinalis betegségek
Nem gyakori (> 1/1000, nátha, orrszárazság).
Emésztőrendszeri betegségek
Gyakori (> 1/100, szájszárazság)
Nem gyakori (> 1/1000, ízérzékenység, hányinger, hasmenés).
A bőr és a bőr alatti szövet betegségei
Gyakori (> 1/100, szemhéj erythema).
Nem gyakori (> 1/1000, allergiás kontakt dermatitis.
Általános betegségek és az alkalmazás helyén fellépő állapotok
Gyakori (> 1/100, aszténia.
A Combigan forgalmazása óta a következő mellékhatásokat jelentették:
Szembetegségek
Nem ismert: homályos látás
Szív patológiák
Nem ismert: aritmia, bradycardia, tachycardia
Érpatológiák
Nem ismert: hipotenzió
Bőrbetegségek
Nem ismert: arcpír
Más mellékhatásokat figyeltek meg az egyik komponensnél, ezért előfordulhatnak a Combigan -nal is:
Brimonidin
Szembetegségek: iritis, iridocyclitis (elülső uveitis), miosis
Pszichiátriai rendellenességek: álmatlanság
Légzőrendszeri, mellkasi és mediastinalis betegségek: felső légúti tünetek, dyspnoe
Emésztőrendszeri betegségek és tünetek: emésztőrendszeri tünetek
Általános betegségek és az alkalmazás helyén fellépő állapotok: szisztémás allergiás reakciók
A bőr és a bőr alatti szövet betegségei és tünetei: bőrreakciók, beleértve a bőrpírt, az arc ödémáját, viszketést, kiütést és értágulatot
Azokban az esetekben, amikor a brimonidint a veleszületett glaukóma orvosi kezelésének részeként alkalmazták, a brimonidin túladagolásának tüneteit, például egészségvesztést jelentettek brimonidinnel kezelt csecsemőknél és (2 évesnél fiatalabb) gyermekeknél. Eszmélet, letargia, aluszékonyság , hypotensio, hypotonia, bradycardia, hipotermia, cianózis, sápadtság, légzésdepresszió és apnoe (lásd 4.3 pont).
Két éves és idősebb gyermekeknél, különösen 2-7 éves és / vagy súlyú gyermekeknél
Timolol
Más helyileg alkalmazott szemészeti gyógyszerekhez hasonlóan a Combigan (brimonidin -tartarát / timolol) felszívódik a szisztémás keringésbe. A timolol felszívódása a nem szisztémás béta-blokkolókhoz hasonló mellékhatásokat okozhat.
A helyi szemészeti gyógyszerek beadása után a szisztémás mellékhatások előfordulási gyakorisága alacsonyabb, mint a szisztémás beadást követő reakcióké.
Az alábbiakban felsoroljuk a szemészeti béta-blokkolóknál észlelt egyéb mellékhatásokat, amelyek szintén előfordulhatnak a Combigan alkalmazásával:
Immunrendszeri betegségek és tünetek: szisztémás allergiás reakciók, beleértve az angioödémát, csalánkiütést, lokalizált és általános kiütéseket, viszketést, anafilaxiás reakciókat
Anyagcsere- és táplálkozási rendellenességek: hipoglikémia
Pszichiátriai rendellenességek: álmatlanság, rémálmok, memóriavesztés
Idegrendszeri betegségek és tünetek: cerebrovaszkuláris baleset, agyi ischaemia, a myasthenia gravis jeleinek és tüneteinek súlyosbodása, paresztézia
Szembetegségek: keratitis, choroid leválás szűrőműtétet követően (lásd 4.4 pont Különleges figyelmeztetések és az alkalmazással kapcsolatos óvintézkedések), csökkent szaruhártya -érzékenység, szaruhártya -erózió, ptosis, diplopia
Szívbetegségek: mellkasi fájdalom, ödéma, atrioventricularis blokk, szívmegállás, szívelégtelenség
Érrendszeri betegségek és tünetek: Raynaud -jelenség, hideg érzés a végtagokban
Légzőrendszeri, mellkasi és mediastinalis betegségek: hörgőgörcs (főleg már meglévő hörgőgörcsös betegségben szenvedő betegeknél), dyspnoe, köhögés
Emésztőrendszeri betegségek: dyspepsia, hasi fájdalom, hányás
A bőr és a bőr alatti szövet betegségei és tünetei: alopecia, pikkelysömör alakú kiütés vagy a psoriasis súlyosbodása, bőrkiütés
A mozgásszervi és kötőszöveti betegségek és tünetek: mialgia
A reproduktív rendszer és az emlő betegségei: szexuális diszfunkció, csökkent libidó
Általános betegségek és az alkalmazás helyén fellépő állapotok: fáradtság
04.9 Túladagolás
Ritka jelentések a Combigan túladagolásáról emberekben nem mutattak káros hatást. A túladagolás kezelése tüneti támogató terápiát foglal magában; a beteg légútjait szabadon kell tartani.
Brimonidin
Szemészeti túladagolás (felnőttek) :
A beérkezett esetekben a bejelentett események általában azok voltak, amelyeket már mellékhatásoknak neveztek.
Véletlen lenyelés okozta szisztémás túladagolás (felnőttek) :
Nagyon kevés információ áll rendelkezésre a brimonidin felnőttek véletlen lenyeléséről. Az egyetlen mellékhatás, amelyről eddig beszámoltak, a hipotenzió volt. Más alfa-2-agonistákkal történő szájon át történő túladagolás olyan tüneteket eredményezett, mint a hypotensio, aszténia, hányás, letargia, szedáció, bradycardia, aritmia, miozis, apnoe, hypotonia, hipotermia, légzési depresszió és görcsök.
Gyermekpopuláció :
Az Allergannek számos jelentést tettek közzé súlyos mellékhatásokról, amelyek gyermekgyógyászati személyek véletlen lenyelését követően jelentettek brimonidint. Az alanyoknak a központi idegrendszeri depresszió tünetei voltak, jellemzően átmeneti kóma vagy alacsony tudatosság, letargia, aluszékonyság, hypotonia, bradycardia, hipotermia, sápadtság, légzésdepresszió és apnoe, és szükség esetén intubációval történő intenzív osztályra való felvételük. A teljes gyógyulásról minden alany esetében számoltak be 6-24 órán belül.
Timolol
A timolol szisztémás túladagolásának tünetei a következők: bradycardia, hypotensio, bronchospasmus, fejfájás, szédülés és szívmegállás. Néhány betegben végzett vizsgálat kimutatta, hogy a timolol nem gyorsan dializálódik.
05.0 FARMAKOLÓGIAI TULAJDONSÁGOK
05.1 Farmakodinámiás tulajdonságok
Farmakoterápiás csoport: Szemészet - Glaukóma elleni és miotikus készítmények - Béta -blokkoló szerek - timolol, kombinációk
ATC kód: S01 ED51
A cselekvés mechanizmusa
A Combigan két hatóanyagból áll: brimonidin -tartarátból és timolol -maleátból. Ez a két komponens csökkenti a megnövekedett intraokuláris nyomást (IOP) a kiegészítő hatásmechanizmusoknak köszönhetően, és a kombinált hatás nagyobb mértékű IOP -csökkenéshez vezet, mint az egyes összetevők. A Combigan gyorsan cselekszik.
A brimonidin-tartarát alfa-2-adrenerg receptor agonista, 1000-szer szelektívebb az alfa-2-adrenoreceptorokkal szemben, mint az alfa-1-receptor. Ez a receptor -szelektivitás azt jelenti, hogy a hatóanyag nem okoz mydriasisot, sem érszűkületet a humán retina xenograftban lévő erek mikrovérei szintjén.
Úgy gondolják, hogy a brimonidin -tartarát csökkenti az IOP -t azáltal, hogy növeli az uveoszklerális kiáramlást és csökkenti a vizes humor képződését.
A timolol nem szelektíven blokkolja a béta-1 és béta-2 adrenerg receptorokat, hiányzik belőlük a szimpatomimetikus aktivitás, valamint a szívizom közvetlen nyugtató hatása vagy helyi érzéstelenítő (membrán stabilizáló) hatása. A timolol csökkenti az IOP-t a vizes humusz képződésének csökkentésével. A pontos hatásmechanizmust nem egyértelműen megállapították, de valószínű, hogy gátolja a ciklikus AMP szintézist, amelyet endogén béta-adrenerg stimuláció okoz.
Klinikai hatások
Három kettős vak, kontrollált klinikai vizsgálatban a Combigan (naponta kétszer) klinikailag szignifikáns additív csökkenést eredményezett az átlagos napi IOP-ban, összehasonlítva a monoterápiában alkalmazott timolollal (napi kétszer) és brimonidinnel (naponta kétszer vagy háromszor).
Egy olyan betegekben végzett vizsgálatban, akiknél az IOP nem volt megfelelően kontrollálva, legalább háromhetes beavatkozási időszak után bármilyen monoterápiával, a három hónapos Combigan (napi kétszer), timolol (napi kétszeri) és brimonidin (napi kétszeri) kezelés további csökkenést mutatott napi átlagos IOP -ban 4,5, 3,3 és 3,5 Hgmm. Ebben a tanulmányban az alkalmazás előtt az IOP szignifikáns további csökkenése csak a brimonidinnel összehasonlítva, de a timolollal nem igazolható, bár az idő előrehaladtával minden más előre meghatározott kontroll elemzés pozitív tendenciát és fölényt mutat.
A másik két klinikai vizsgálat adatainak együttes összegyűjtésével és elemzésével minden mérés során statisztikai fölényt találnak a timolollal szemben.
Ezenkívül a Combigan -nal mért IOP csökkenés mértéke következetesen nem volt kisebb, mint a brimonidin és timolol kombinációval (mindkettő naponta kétszer).
Kettős vak vizsgálatok kimutatták, hogy a Combigan-nal kapott szemnyomás csökkenése legfeljebb 12 hónapig tart.
05.2 Farmakokinetikai tulajdonságok
Kombinált
A brimonidin és a timolol plazmakoncentrációit egy keresztezett vizsgálatban, valamint a monoterápiával és a Combigan kezeléssel való összehasonlítással határozták meg egészséges önkéntesekben. A Combigan és a hozzájuk tartozó monoterápiás kezelések összehasonlításakor nem volt statisztikailag szignifikáns különbség a brimonidin vagy a timolol AUC -értékei között.
A Combigan beadása után a brimonidin és a timolol átlagos plazma C -értéke 0,0327, illetve 0,406 ng / ml volt.
Brimonidin
A brimonidin plazmakoncentrációja emberben alacsony, 0,2% -os szemcseppek szemészeti beadása után. A brimonidin nem metabolizálódik szignifikánsan az emberi szemben, és a plazmafehérjékhez való kötődése megközelítőleg 29%. Ezt követően. Helyi alkalmazás emberekben, szisztémás keringése körülbelül 3 óra volt.
Az orális adagolást követően a brimonidin jól felszívódik és gyorsan eliminálódik.A dózis nagy része (kb. 74%) öt nap alatt metabolitok formájában ürül a vizelettel; nincs módosítatlan gyógyszer a vizeletben. Az állati és emberi májon végzett in vitro vizsgálatok azt mutatják, hogy az anyagcserét nagyrészt az aldehid -oxidáz és a citokróm P450 közvetíti, így a szisztémás eliminációt főként a máj metabolizmusára bízzák.
A szemszövetekben a brimonidin jelentősen és visszafordíthatóan kötődik a melaninhoz anélkül, hogy ez nemkívánatos hatásokat okozna. A melanin hiányában nincs felhalmozódás.
A brimonidin metabolizmusa az emberi szemben nem releváns.
Timolol
A szürkehályog -műtéten átesett személyeknél a 0,5% -os szemcseppek maximális koncentrációja a vizes humorában emberben körülbelül 898 ng / ml volt körülbelül 1 órával a beadás után. Az adag egy része szisztémásan felszívódik, majd elsősorban a májban metabolizálódik. A timolol plazma felezési ideje körülbelül 7 óra. A timolol részben a májban metabolizálódik, és változatlan timololként és metabolitokként ürül a vesén keresztül. A timolol nem kötődik jelentősen a plazmafehérjékhez.
05.3 A preklinikai biztonságossági adatok
Az egyes összetevők szem- és szisztémás biztonsága jól megalapozott. A hagyományos farmakológiai biztonságossági, ismételt dózistoxicitási, genotoxicitási és karcinogén potenciális vizsgálatok alapján a nem klinikai adatok nem mutatnak különleges veszélyt az emberre.
Brimonidin
A brimonidin -tartarát nem mutatott teratogén hatást állatokban, de abortuszokat okozott nyulakban, és csökkentette a posztnatális növekedést patkányokban, ha a szisztémás expozíció szintje megközelítőleg 37, illetve 134 -szerese volt a kezelés során tapasztalt embereknek.
Timolol
Állatkísérletekben kimutatták, hogy a béta-blokkolók csökkent köldökvéráramlást, csökkent magzati növekedést, késleltetett csontképződést és fokozott magzati és születés utáni halált okoznak, de nem teratogén hatásúak. Az anyának adott nagy dózisú timolollal embrionális toxicitást (reszorpció) mutattak ki nyulakban és magzati toxicitást (késleltetett csontosodás) patkányokban. A teratogenitási vizsgálatok egereken, patkányokon és nyulakon, a timolol orális dózisának, a Combigan napi humán dózisának legfeljebb 4200 -szoros dózisának megfelelően, nem mutattak magzati rendellenességet.
06.0 GYÓGYSZERÉSZETI INFORMÁCIÓK
06.1 Segédanyagok
Benzalkónium-klorid
Egybázisú nátrium -foszfát -monohidrát
Dinátrium -foszfát -heptahidrát
Sósav vagy nátrium -hidroxid a pH beállításához
Tisztított víz
06.2 Inkompatibilitás
Nem releváns.
06.3 Érvényességi idő
21 hónap
Első felbontás után: 28 napon belül fel kell használni
06.4 Különleges tárolási előírások
Tartsa a palackot a külső dobozban, hogy megvédje a fénytől.
06.5 A közvetlen csomagolás jellege és a csomagolás tartalma
Fehér kis sűrűségű polietilén palackok polisztirol csavaros kupakkal.
Minden palack 5 ml -es töltési térfogattal rendelkezik.
A következő csomagok állnak rendelkezésre: doboz 1 vagy 3 5 ml -es palackot tartalmaz. Nem feltétlenül mindegyik kiszerelés kerül kereskedelmi forgalomba.
06.6 Használati utasítás
Nincsenek speciális utasítások.
07.0 FORGALOMBA HOZATALI ENGEDÉLY
Allergan Pharmaceuticals Írország
Castlebar Road
Westport
Co. Mayo
Írország
08.0 A FORGALOMBA HOZATALI ENGEDÉLY SZÁMA
037083019 / M 0,2% + 0,5% szemcsepp oldat, 5 ml -es üveg
037083021 / M 0,2% + 0,5% szemcsepp oldat 3 üveg 5 ml
09.0 Az első forgalomba hozatali engedély kiadásának időpontja
Az első engedélyezés időpontja: december 5
2006 Az utolsó megújítás dátuma: 2010. március 30
10.0 A SZÖVEG FELÜLVIZSGÁLÁSÁNAK DÁTUMA
02/2012