Annak érdekében, hogy érthetően beszélhessünk a "hemoglobin (Hb), hasznos gondoskodni az elsőről mioglobin (Mb) amely nagyon hasonlít a hemoglobinhoz, de sokkal egyszerűbb. A hemoglobin és a mioglobin között szoros rokonsági kapcsolatok vannak: mindkettő konjugált fehérje, és protéziscsoportjuk (nem fehérje része) a csoport heme.
A mioglobin egy gömb alakú fehérje, amely körülbelül százötven aminosavból álló láncból áll (ez a szervezettől függ), és molekulatömege körülbelül 18 Kd.
Amint említettük, hem-csoporttal van ellátva, amely a fehérje hidrofób (vagy lipofil) részébe van beépítve, és a rostos fehérjék α-hélix szerkezetének tulajdonítható redőkből áll.
A mioglobin főleg α-hélix szegmensekből áll, amelyek száma nyolc, és szinte kizárólag nem poláris maradékokból (leucin, valin, metionin és fenilalanin) áll, míg a poláris maradékok gyakorlatilag nincsenek (aszparaginsav, glutaminsav, lizin) és arginin); az egyetlen poláris maradék két hisztidin, amelyek alapvető szerepet játszanak az oxigén kötődésében a hemcsoporthoz.
A hemcsoport egy kromofórcsoport (a láthatóan felszívódik), és a mioglobin funkcionális csoportja.
Lásd még: glikált hemoglobin - hemoglobin a vizeletben
Egy kis kémia

A protoporfirin és a vas közötti kötés a koordinációs vegyületek tipikus kötése, amelyek olyan kémiai vegyületek, amelyekben egy központi atom (vagy ion) kötéseket képez más vegyi anyagokkal az oxidációs számánál (elektromos töltés) nagyobb számban. A hem esetében ezek a kötések reverzibilisek és gyengék.
A vas koordinációs száma (koordinációs kötéseinek száma) hat: a vas körül hat molekula lehet, amelyek megosztják a kötőelektronokat.
A koordinációs vegyület kialakításához két, megfelelő irányú pályára van szükség: az egyik képes elektronokat "szerezni", a másik pedig adományozni.
A hemben a vas négy sík kötést képez a négy nitrogénatommal a proto-porfirin gyűrű közepén és egy ötödik kötést egy proximális hisztidin-nitrogénnel; a vas rendelkezik a hatodik szabad koordinációs kötéssel, és képes kötődni az oxigénhez.
Ha a vas szabad ion formájában van, akkor a típusa kering d mindegyiknek ugyanaz az energiája; a mioglobinban a vasion protoporfirinhez és hisztidinhez kötődik: ezek a fajok mágnesesen zavarják a pályákat d némi vas; a zavarás mértéke a különböző pályákon eltérő lesz d térbeli orientációjuktól és a zavaró fajoktól függően. Mivel a pályák teljes energiájának állandónak kell lennie, a zavarás energetikai elválasztást okoz a különböző pályák között: egyes pályák által megszerzett energia egyenértékű a többi által elveszett energiával.
Ha a pályák közötti távolság nem túl nagy, akkor előnyös a nagy spinű elektronikus elrendezés: a kötőelektronok a lehető legtöbb alszinten párhuzamos pörgésekben igyekeznek elrendezni magukat (maximális többszörösség); ha viszont a zavarás nagyon erős, és nagy a távolság a pályák között, akkor kényelmesebb lehet a kötéselektronok párosítása az alacsonyabb energiájú (alacsony spinű) pályákon.
Amikor a vas kötődik az oxigénhez, a molekula alacsony spin -elrendezést feltételez, míg ha a vas hatodik koordinációs kötése szabad, akkor a molekula nagy spin -elrendezésű.
Ennek a centrifugálási különbségnek köszönhetően a mioglobin spektrális elemzésén keresztül képesek vagyunk megérteni, hogy az oxigén (MbO2) kötődik -e hozzá vagy sem (Mb).
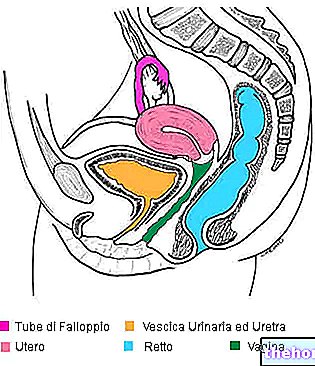
A mioglobin egy tipikus izomfehérje (de nem csak az izmokban található meg).
A mioglobint kivonják a bálnából, amelyben nagy mennyiségben van jelen, majd megtisztítják.
A cetek légzése olyan, mint az embereké: a tüdő birtokában a levegőt el kell szívniuk a légzési folyamaton keresztül; a spermabálnának a lehető legtöbb oxigént kell bejuttatnia az izmokba, amelyek képesek felhalmozni az oxigént azáltal, hogy megkötik azt a bennük lévő mioglobinhoz; azután az oxigén lassan felszabadul, amikor a cet elmerül, mert anyagcseréje oxigént igényel: annál nagyobb mennyiségű az oxigén, amelyet a spermabálna képes felvenni, és minél több oxigén áll rendelkezésre a merülés során.
A myoglybin reverzibilis módon megköti az oxigént, és annál nagyobb százalékban van jelen a perifériás szövetekben, annál inkább, ahogy a szövetek hozzászoktak ahhoz, hogy időben távoli oxigénellátással dolgozzanak.
<--- A mioglobin az izmokban jelen lévő fehérje, amelynek funkciója éppen az oxigéntartályé.
A húst többé -kevésbé vörösvé teszi a hemoproteinek tartalma (ez a hem, ami vörössé teszi a húst).
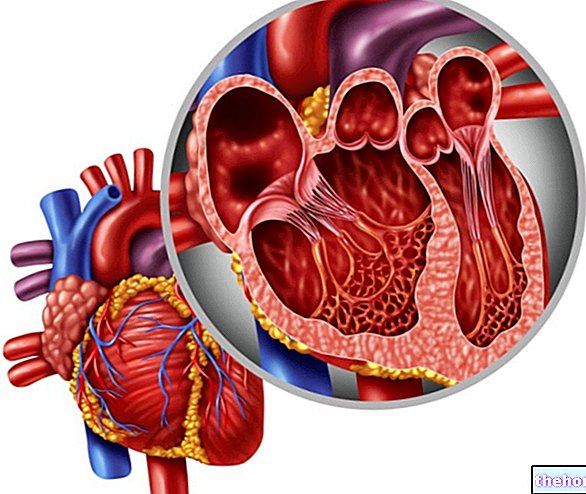
A hemoglobin sok szerkezeti hasonlóságot mutat a mioglobinnal, és képes molekuláris oxigént reverzibilis módon megkötni; de míg a mioglobin az izmokra és általában a perifériás szövetekre korlátozódik, a hemoglobin megtalálható az eritrocitákban vagy a vörösvértestekben (álsejtek, vagyis nem valódi sejtek), amelyek a vér 40% -át teszik ki.
A mioglobinnal ellentétben a hemoglobin feladata, hogy oxigént vegyen be a tüdőbe, engedje el a sejtekbe, ahol szükség van rá, vegyen be szén -dioxidot és engedje el a tüdőbe, ahol a ciklus újra kezdődik.
L "hemoglobin ez egy tetraméter, azaz négy polipeptidláncból áll, amelyek mindegyike hemecsoporttal rendelkezik és kettő kettővel azonos (emberben két alfa és két béta lánc van).
A hemoglobin fő funkciója az oxigén szállítása; a vér másik funkciója, amelyben a hemoglobin részt vesz, az anyagok szövetekbe történő szállítása.
A tüdőből (oxigénben gazdag) a szövetekbe vezető úton a hemoglobin oxigént szállít (ugyanakkor a többi anyag eléri a szöveteket), míg a fordított úton a szövetek által gyűjtött hulladékot, különösen a szenet az anyagcserében képződő dioxid.
Az ember fejlődésében vannak olyan gének, amelyek csak egy bizonyos ideig expresszálódnak; ezért különböző hemoglobinok léteznek: magzati, embrionális, a felnőtt férfi.
A különböző hemoglobinokat alkotó láncok szerkezete eltérő, de némi hasonlósággal valójában a funkciójuk többé -kevésbé azonos.
Több különböző lánc jelenlétének magyarázata a következő: a szervezetek evolúciós folyamata során még a hemoglobin is kifejlődött, amely az oxigén szállítására specializálódott a gazdag területekről a hiányos területekre. az evolúciós lánc l "hemoglobinja oxigént szállított kis szervezetekben; az evolúció során a szervezetek nagyobb méreteket értek el, ezért a hemoglobint úgy módosították, hogy képes legyen oxigént szállítani a távolabbi területekre attól a ponttól, ahol gazdag volt benne; ezt az evolúciós folyamat során a hemoglobinot alkotó láncok új struktúráiba kódolták.
A mioglobin mérsékelt nyomáson is megköti az oxigént; a perifériás szövetekben körülbelül 30 Hgmm nyomás (PO2) van: a mioglobin ezen a nyomáson nem bocsát ki oxigént, ezért oxigénhordozóként hatástalan lenne. A hemoglobin viszont , rugalmasabb viselkedésű: megköti az oxigént a magas nyomásokhoz, és felszabadítja, amikor a nyomás csökken.
Ha egy fehérje funkcionálisan aktív, akkor kissé megváltoztathatja alakját; például az oxigénnel telített mioglobin más alakú, mint a nem oxigénnel telített mioglobin, és ez a mutáció nem érinti a szomszédokat.
Más a helyzet a kapcsolódó fehérjék, például a hemoglobin esetében: amikor egy lánc oxigenizálódik, akkor megváltoztatja alakját, de ez a módosítás háromdimenziós, így a tetraméter többi lánca is érintett. azt sugallja, hogy az egyik módosítása más mértékben is érinti a többi szomszédot; ha egy lánc oxigenizál, a tetraméter többi lánca "kevésbé ellenséges hozzáállást" feltételez az oxigénnel szemben: a lánc nehézsége Az oxigenizáció csökken, amikor a hozzá közeli láncok sorra oxigénelnek. Ugyanez vonatkozik a deoxigenizációra is.
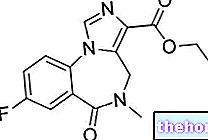
A dezoxihemoglobin negyedik szerkezetét T (feszült) formának, míg az oxihemoglobinét R (felszabadult) formának nevezik; feszült állapotban meglehetősen erős elektrosztatikus kölcsönhatások sorozata van a savas aminosavak és a bázikus aminosavak között, amelyek a dezoxihemoglobin merev szerkezetéhez vezetnek (ez az oka a "feszült formának"), míg amikor az oxigén kapcsolódik, ezek egysége interakciók csökkennek (innen a "felszabadult forma"). Továbbá oxigén hiányában a hisztidin töltését (lásd a szerkezetet) az aszparaginsav ellentétes töltése stabilizálja, míg oxigén jelenlétében a fehérje hajlamos a proton elvesztésére; Mindez azzal jár, hogy az oxigénnel telített hemoglobin erősebb sav, mint a dezoxigenizált hemoglobin: bohr hatás.
A pH -tól függően a hem -csoport többé -kevésbé könnyen kötődik az oxigénhez: savas környezetben a hemoglobin könnyebben bocsátja ki az oxigént (a feszült forma stabil), míg bázikus környezetben az oxigénnel való kötés nehezebb.

Minden hemoglobin 0,7 protont bocsát ki a belépő oxigén (O2) móljára.
A Bohr -hatás lehetővé teszi, hogy a hemoglobin javítsa oxigénszállító képességét.
A tüdőből a szövetekbe jutó hemoglobinnak egyensúlyban kell lennie a nyomás, a pH és a hőmérséklet függvényében.
Lássuk a hőmérséklet hatását.
A pulmonalis alveolusok hőmérséklete körülbelül 1-1,5 ° C-kal alacsonyabb, mint a külső hőmérséklet, míg az izmokban a hőmérséklet körülbelül 36,5-37 ° C; a hőmérséklet növekedésével a telítettségi faktor csökken (ugyanazon nyomáson): ez azért történik, mert a kinetikus energia növekszik, és a disszociáció előnyben részesül.

Vannak más tényezők is, amelyek befolyásolhatják a hemoglobin oxigénhez való kötődési képességét, amelyek egyike a 2,3 -biszfoszfoglicerát koncentrációja.
A 2,3-biszfoszfoglicerát metabolikus jelenléte az eritrocitákban 4-5 mM koncentrációban (a szervezet egyetlen részében sem található meg ilyen magas koncentrációban).
Fiziológiai pH -n a 2,3 -biszfoszfoglicerát deprotonálódik, és öt negatív töltés van rajta; a két hemoglobin béta lánc közé ékelődik, mert ezekben a láncokban magas a pozitív töltések koncentrációja. A béta -láncok és a 2,3 -biszfoszfoglicerát közötti elektrosztatikus kölcsönhatások bizonyos merevséget kölcsönöznek a rendszernek: feszült szerkezetet kapunk, amely kevés affinitást mutat az oxigénhez; az oxigénellátás során a 2,3 -biszfoszfoglicerát kiürül.
Az eritrocitákban a c "egy speciális készülék, amely az 1,3-biszfoszfoglicerátot (anyagcsere útján előállítva) 2,3-biszfoszfogliceráttá alakítja át úgy, hogy eléri a 4-5 mM koncentrációt, és ezért a hemoglobin képes az oxigén cseréjére a szövetekben.
A szövetbe érkező hemoglobin felszabadult állapotban van (oxigénhez kötött), de a szövet közelében karboxilezett, és átmegy feszült állapotba: ebben az állapotban a fehérje kevésbé hajlamos az oxigénhez való kötődésre. a felszabadult állapotba, ezért a hemoglobin oxigént bocsát ki a szövetbe; ezenkívül a víz és a szén -dioxid reakciója következtében H + -ionok keletkeznek, tehát a bohr -hatás következtében további oxigén.
A széndioxid a plazmamembránon keresztül diffundál a vörösvértestbe; mivel az eritrociták a vér mintegy 40% -át teszik ki, ezért azt kell várnunk, hogy a szövetekből diffundáló szén -dioxidnak csak 40% -a kerül beléjük, valójában a szén -dioxid 90% -a kerül az eritrocitákba, mert tartalmaznak egy szén -dioxidot átalakító enzimet szénsavban azt eredményezi, hogy a vörösvértestekben a szén -dioxid stacionárius koncentrációja alacsony, és ezért magas a belépési sebesség.

Egy másik jelenség, amely akkor fordul elő, amikor egy eritrocita eléri a szövetet, a következő: gradiens szerint a "HCO3- (szén-dioxid-származék) elhagyja az" eritrocitát, és a negatív töltés kimenetének kiegyensúlyozásához "kloridok lépnek be" meghatározza az ozmotikus nyomás növekedését: ennek az eltérésnek a kiegyenlítésére víz is belép, ami az eritrocita duzzadását okozza (HAMBURGER -hatás). Ezzel ellentétes jelenség fordul elő, amikor egy eritrocita eléri a tüdő alveolusait: az eritrociták deflációja (HALDANE -hatás) Ezért a vénás vörösvértestek (a tüdőbe irányítva) kerekebbek, mint az artériák.